Материал: Процессы получения наночастиц и наноматериалов, нанотехнологии
Сказанное выше означает, что наноконструкция представляет собой новый тип биоматериала, свойства которого можно регулировать в широких пределах.
Учитывая стабильность наноконструкции, ее частицы были визуализированы при помощи атомного силового микроскопа [16]. Частицы по форме близки к вытянутым цилиндрам. Оценка размера 400 частиц показывает, что хотя размер частиц меняется в пределах от 0.4 до 0.8 мкм, средняя величина составляет около 0.5 мкм. Это означает, что размер полученных нами частиц жидкокристаллических дисплеев, в составе которых молекулы ДНК «сшиты» наномостиками (т.е. наноконструкций, существующих в отсутствии осмотического давления раствора), совпадает с размером исходных частиц ЖКД из двухцепочечных молекул ДНК, рассчитываемым теоретически в случае растворов с постоянным осмотическим давлением [18].
Таким образом, технология, основанная на
«энтропийной конденсации» исходных двухцепочечных нуклеиновых кислот, приводит
к созданию наноконструкций, обладающих уникальными свойствами.
. ПРОСТРАНСТВЕННОЕ УПОРЯДОЧЕНИЕ КОМПЛЕКСОВ ДВУХЦЕПОЧЕЧНЫХ МОЛЕКУЛ НУКЛЕИНОВЫХ КИСЛОТ С ПОЛИКАТИОНАМИ В РЕЗУЛЬТАТЕ «ЭНТАЛЬПИЙНОЙ КОНДЕНСАЦИИ» И НАНОКОНСТРУКЦИИ НА ОСНОВЕ МОЛЕКУЛ ЭТИХ ПОЛИКАТИОНОВ
С этой точки зрения внимание привлекают полиаминосахара, в частности природный биодеградируемый полимер - хитозан (поли[β(1->4)-2-амино-2-деокси- D-глюкопираноза]). Показано, что взаимодействие этого поликатиона с двухцепочечным ДНК приводит к образованию холестерических жидкокристаллических дисплеев [20], имеющих аномальные полосы в спектре. На кривых рассеяния рентгеновских лучей на фазе, сформированной из частиц ЖКД дисперсии комплекса (ДНК-Хи), присутствует один брэгговский рефлекс (d Брэгг ~ 26 A °). Величина брэгговского рефлекса, характеризующая среднее расстояние между соседними молекулами комплексов (ДНК-Хи) в образованной фазе, существенно меньше по сравнению с величиной d Брэгг, характерной для частиц ЖКД «чистой» ДНК, и соответствует переходной области между холестерической и гексагональной жидкокристаллической фазами [19].
Ряд свойств молекул хитозана (Хи) в составе комплексов (ДНК-Хи) интересен с точки зрения наноконструирования. Во-первых, в силу стерической структуры молекул Хи только часть аминогрупп этих молекул взаимодействует с фосфатными группами ДНК, другая часть аминогрупп оказывается экспонированной во «внешнюю» среду. Во-вторых, амино- и гидроксильные группы соседних сахарных остатков молекул Хи могут образовывать прочные комплексы с ионами металлов [21]. В частности, константа связывания иона двухвалентной меди составляет около 1014 М [21,22], причем образующийся хелатный комплекс имеет планарную структуру. Такой комплекс, в принципе, может служить местом «начала» («окончания») наномостиков, которые в этом случае соединят не молекулы ДНК, а молекулы Хи, фиксированные на поверхности ДНК. Наконец, аномальная полоса в спектре ЖК дисплея комплексов (ДНК-Хи), имеющая в зависимости от целого ряда условий либо положительный, либо отрицательный знак, позволит следить за изменениями в пространственной структуре частиц ЖК дисплеев.
Имея на руках данные, характеризующие свойства наноконструкций на основе двухцепочечных молекул ДНК, и учитывая свойства частиц ЖК дисплея комплексов (ДНК-Хи), была предпринята попытка создания наномостиков между соседними молекулами Хи, фиксированными в структуре частиц их ЖК дисплеев.
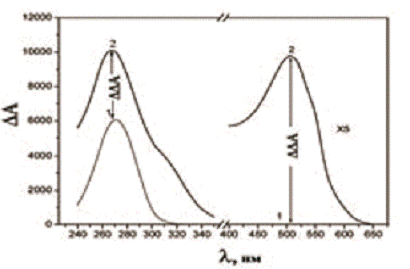
При добавлении CuCl2 к ЖК дисплею комплекса (ДНК- Хи), имеющей положительный знак полосы в спектре и последующей ее обработке ДАУ, возникает интенсивная положительная полоса при λ~ 500 нм (рис. 4), соответствующая оптическим свойствам хромофора комплекса [ДАУ- Cu2+].
молекула наноконструкция нуклеиновый энтальпийный
Аналогичная амплификация наблюдается также при обработке ЖК дисплея, сформированной из комплекса (ДНК-Хи), в котором молекулы Хи имеют другое содержание аминогрупп, и ЖК дисплей этого комплекса (ДНК-Хи) характеризуется отрицательной полосой в спектре.
Амплификация полосы в области поглощения хромофора [ДАУ- Cu2+] показывает, что этот хромофор пространственно фиксирован по отношению к молекулам Хи в любых ЖК дисплеях, сформированных из комплексов (ДНК-Хи).
Эффективность нарастания аномальной полосы в спектре ЖК дисплея комплексов (ДНК-Хи) зависит также, как и в случае «чистой» ДНК, от концентрации молекул ДАУ и ионов меди.
Не исключено, что, также как и в случае чистой ДНК, часть молекул ДАУ может интеркалировать между парами оснований ДНК в составе комплекса (ДНК-Хи), но этот процесс быстро достигает своего равновесия.
Отсутствие «критической» концентрация в случае ионов меди означает, что в отличие от случая «чистой» ДНК в молекулах Хи, фиксированных в структуре комплекса (ДНК-Хи), всегда имеются химические группы, стерически доступные для реакции хелатообразования. Такими группами могут быть аминогруппы и гидроксильные группы сахарных остатков Хи, образующие хелатные комплексы с ионами меди с высокой константой связывания [21,22].
Сопоставление полученных результатов (рис. 6) с результатами формирования наномостиков в случае «чистой» ДНК (рис. 2) свидетельствует об их качественном соответствии. На основании этого можно утверждать, что амплификация полосы при λ ~ 500 нм в спектрах ЖК дисплеев разных комплексов (ДНК-Хи) обусловлена возникновением наномостиков типа […- Cu2+ - ДАУ- Cu2+ -...] между соседними молекулами Хи, связанными в комплексы с молекулами ДНК в составе частиц ЖК дисплея.
Учитывая тот факт, что в этом случае, так же как и в случае «чистой» ДНК, наномостики могут возникать между соседними молекулами Хи, расположенными как в одном слое, так и молекулами Хи в соседних слоях, амплификация полосы λ ~ 500 нм отражает возникновение пространственной наноконструкции. Это означает, что формирование наноконструкций на основе ЖК дисплеев молекул ДНК комплексов (ДНК - Хи) имеет во всех случаях одно и тоже оптическое «проявление».
Интересным результатом, указывающим на то, что конформация молекул Хи важна для наноконструирования, является зависимость величины аномальной амплитуды полосы (λ 505 нм) в спектрах КД ЖКД комплексов (ДНК-Хи) от содержания аминогрупп в молекулах Хи. Данные, приведенные в работе [23], показывают, что имеется минимальное (предельно малое) расстояние между аминогруппами (около 12 Ǻ, что приблизительно соответствует расстоянию между этими группами «через одну»), на котором могут находиться соседние наномостики […- Cu2+ - ДАУ- Cu2+-... ]. Малая величина аномальной оптической активности в этих условиях может быть обусловлена двумя причинами. Во-первых, не исключено, что, несмотря на высокую концентрацию потенциальных мест образования наномостиков, т.е. высокую концентрацию амино- и гидроксильных групп в молекулах Хи, стерическая структура молекул Хи не является оптимальной для образования наномостиков. Во-вторых, не исключено, что при малом расстоянии между потенциальными местами образования наномостиков […- Cu2+ - ДАУ- Cu2+ -..] стерическое взаимодействие между компонентами наномостиков, в частности между объемными аминосахарными остатками молекул ДАУ, запрещает их близкое расположение. По мере увеличения расстояния между аминогруппами в молекулах Хи стерическая структура молекулы Хи меняется таким образом, что ориентация соседних амино- и гидроксильных групп в сахарных остатках Хи оказывается достаточной для оптимальной ориентации соседних наномостиков в создаваемой наноконструкции, и в этих условиях обеспечивается высокая аномальная оптическая активность наноконструкции.
С этой точки зрения интересно сопоставить значения максимальных амплитуд полос, наблюдаемых при создании наноконструкции на основе ЖК дисплеев чистой ДНК и комплексов (ДНК-Хи). При использованных нами условиях (мол. масса ДНК ~ 8х105 Да, концентрация ДНК ~ 15 мкг/мл) максимальная амплитуда полосы при λ ~ 500 нм, характерная для ЖКД комплексов (ДНК-Хи), не превышает 2500 единиц ∆А, несмотря на разные препараты Хи. Если сопоставить это значение со значением амплитуды, измеренным ранее для ЖК дисплея ДНК и учесть корреляцию между концентрацией ДНК и амплитудой аномальной полосы в спектре для ЖКД, то можно утверждать, что в случае ЖКД комплексов (ДНК- Хи) амплитуда максимальной полосы приблизительно в 3 раза меньше по сравнению с амплитудой полосы, характерной для наноконструкций, сформированных из ЖК дисплея «чистых» двухцепочечных ДНК. Такое различие может быть следствием нескольких причин. Во-первых, оно может отражать меньшее число наномостиков, во-вторых, оно может отражать меньшую физическую длину (размер) наномостиков, поскольку расстояние между молекулами комплекса (ДНК-Хи) меньше по сравнению с расстоянием между «чистыми» молекулами ДНК, и, наконец, оно может быть связано с тем, что угол наклона наномостиков между молекулами Хи в составе комплекса (ДНК-Хи) в ЖК дисплеях отличается от угла наклона в случае наномостиков между «чистыми» молекулами ДНК, что может быть связано с конформацией молекул Хи, расположенных на соседних молекулах ДНК.
Тот факт, что в случае ЖКД комплексов (ДНК-Хи)
физический размер наномостиков может быть небольшим, в сочетании с тем, что
ионы меди могут образовывать очень прочные хелатные комплексы с соседними
амино- и гидроксильной группами сахарных остатков Хи [24,25], позволяет
предполагать, что структура и свойства полученных наноконструкций могут заметно
отличаться от свойств наноконструкций на основе «чистой» ДНК. Действительно,
как показывают предварительные опыты, амплитуда аномальной полосы (λ
505 нм) в спектрах ЖК дисплеев наноконструкций на основе разных комплексов
(ДНК-Хи) практически не меняется при увеличении температуры. Это означает, что
пространственная структура ЖКД комплексов (ДНК-Хи) остается неизменной при
использованных условиях нагревания, т.е. тепловая стабильность наноконструкций
на основе ЖКД комплексов (ДНК-Хи) заметно превышает стабильность не только
наноконструкций на основе «чистой» ДНК, но и ЖК дисплеев, сформированной из
комплексов (ДНК-Хи).
![]()
Очевидно, что для построения конкретной модели наномостиков между соседними молекулами комплексов (ДНК-Хи) в частицах ЖК дисплея, а следовательно, для построения пространственной модели наноконструкции требуется проведение дополнительных исследований.
Таким образом, независимо от предлагаемых способов пространственного упорядочения соседних молекул нуклеиновых кислот (или их комплексов), для образования наномостиков можно использовать один и тот же прием, основанный на образовании протяженных хелатных комплексов («сшивок») между упорядоченными в структуре ЖК дисплея молекулами нуклеиновых кислот или молекулами поликатионов.
Приведенные выше результаты показывают, что,
пользуясь разными технологиями упорядочения молекул двухцепочечных ДНК в
частицах ЖК дисплеев, можно создавать наноконструкции, различающиеся по
свойствам. Использованные технологии открывают возможность их модификации с
учетом требований, возникающих при решении конкретных задач.
. ОБЛАСТИ ПРИМЕНЕНИЯ НАНОКОНСТРУКЦИИ НА ОСНОВЕ
ДВУХЦЕПОЧЕЧНЫХ МОЛЕКУЛ ДНК
Комбинация свойств молекул нуклеиновых кислот и молекул антибиотика, участвующего в образовании наномостика, открывает ряд возможностей для практического применения наноконструкций.
. Наноконструкции, концентрация ДНК в которых превышает 200 мг/мл, могут быть использованы в качестве «носителей» генетического материала или различных БАС, вводимых в состав этих структур. (Области применения - медицина, биотехнология.)
. Наноконструкции на основе частиц ЖК дисплеев двухцепочечных ДНК (РНК) - это чувствительные элементы (биодатчики) оптических биосенсоров, позволяющих определять наличие БАС, в частности генотоксикантов, в физиологических жидкостях. (Области применения - медицина, экология, биотехнология).
. Наноконструкции с управляемыми физико-химическими свойствами, включенные в состав полимерных пленок (гидрогелей), могут быть использованы в технике, в частности, в качестве оптических фильтров. (Области применения - оптика, электроника.)
Таким образом, приведенные выше данные
показывают, что двухцепочечные молекулы нуклеиновых кислот - это важный,
полифункциональный объект нанобиотехнологии. Направленное и регулируемое
изменение свойств этих молекул обеспечивает широкие возможности для создания
нанобиоструктур, которые могут найти применение в различных областях науки и
техники.
. ДНК - ОРИГАМИ
С помощью химического синтеза можно напрямую синтезировать цепи ДНК длиной до 120 нуклеотидов. То есть в 21 веке можно легко и дешево делать ДНК любой последовательности, какой только захотеть. Для этого есть принцип комплементарности - как только в последовательности ДНК появляются комплементарные зоны, они слипаются и образуют двухцепочечный участок. Очевидно, если делать структуры, стабильные при комнатной температуре, значит, нужно рассчитать температуру плавления для данных участков и сделать ее достаточно большой. При этом на одной цепи ДНК возможно сделать много разных областей с разными последовательностями и слипаться будут только комплементарные. Так как комплементарных областей может быть несколько, в результате молекула может свернуться достаточно сложным образом!
Так же, помимо положительного дизайна (создание
областей, способных образовывать нужную нам структуру), при разработке структур
с самосборкой нельзя забывать и о негативном дизайне - нужно проверять
получившуюся последовательность ДНК на потенциальное наличие паразитных
взаимодействий (когда части созданных областей оказываются способными
взаимодействовать по-другому, образуя ненужные нам паразитные структуры) и от
этих паразитных структур и взаимодействий избавляться, меняя нуклеотидную
последовательность ДНК. Как получить простейшие структуры ДНК типа «шпильки»
достаточно очевидно, но скучно и неинтересно. Можно ли из ДНК сделать что-то
посложнее? Здесь уже без компьютерных вычислений не обойтись. Если нужно
сделать некую структуру и теперь должны подобрать последовательность ДНК,
которая в эту структуру свернется за счет взаимодействия комплементарных
областей, но при этом в последовательности не должно быть паразитных
взаимодействий, непредусмотренных комплементарных областей, образующих
альтернативные структуры. Плюс структура должна отвечать другим критериям,
например, иметь температуру плавления выше некоторой заданной величины.
.1 ДВУХМЕРНЫЕ СТРУКТУРЫ ИЗ ДНК
Методологический прорыв устроил Paul Rothemund
(Калифорнийский Технологический Институт) в 2006 году, именно он и придумал
термин «ДНК-оригами». В своей статье в «Nature» он представил множество
забавных двухмерных объектов, сделанных из ДНК. Принцип, предложенный им,
достаточно прост: взять длинную (примерно 7000 нуклеотидов )«опорную»
одноцепочечную молекулу ДНК и затем с помощью сотни коротких ДНК-скрепок,
образующих двухцепочечные области с опорной молекулой, согнуть опорную ДНК в
нужную двухмерную структуру. Для начала (а) надо нарисовать нужную нам форму
красным цветом и прикинем, как заполнить ее ДНК (представим ее на этом этапе в
виде труб). Далее (b) представить, как провести одну длинную опорную молекулу
по нужной форме (показана черной линией). На третьем этапе (с) подумать, где
разместить «скрепки», стабилизирующие укладку длинной опорной цепи. Четвертый
этап (d): больше деталей, как будет выглядеть вся нужнаяструктура ДНК и,
наконец, (e) схема нужной нам структуры, можно заказывать ДНК нужной
последовательности!
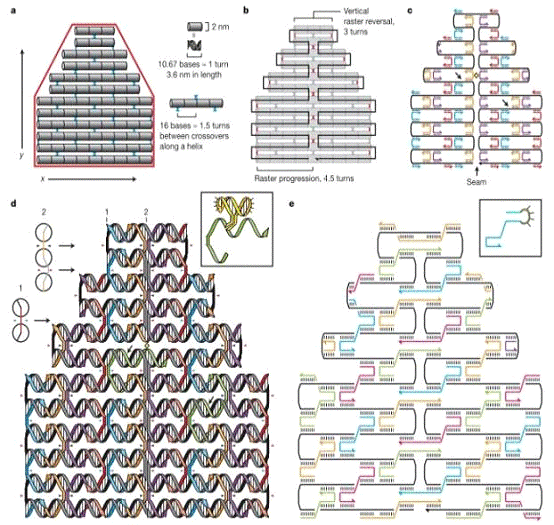
Рисунок 6 - этапы получения двухмерных объектов.
Как же из химически синтезированных ДНК собрать нужную структуру? Здесь на помощь приходит процесс плавления. Нужно взять пробирку с водным раствором, бросить в нее все фрагменты ДНК и нагревать до 94-98С, температуры, которая гарантировано плавит всю ДНК (переводит ее в одноцепочечную форму). Далее просто очень медленно (в течении многих часов, в некоторых работах - в течении нескольких дней) охлаждать пробирку до комнатной температуры (эта процедура называется «отжиг», annealing). При этом медленном охлаждении, когда температура оказывается достаточно низкой, постепенно образуются нужные нам двухцепочечные структуры. В оригинальной работе в каждом эксперименте примерно 70% молекул успешно собирались в нужную структуру, остальные имели дефекты.
Далее, после того, как структура рассчитана,
неплохо бы доказать, что она собирается именно так, как надо. Для этого чаще
всего используют атомно-силовую микроскопию, которая как раз прекрасно
показывает общую форму молекул, но иногда используют и cryo-EM (электронную
микроскопию). Автор сделал множество веселых форм из ДНК.

Рисунок 7 - примеры ДНК - оригами.
.2 ТРЕХМЕРНЫЕ СТРУКТУРЫ ИЗ ДНК
После того, как разобрались с конструированием сложных плоских объектов, почему бы не перейти к третьему измерению? Здесь пионерами была группа ребят из Института Скриппса в Ла-Холле, Калифорния, которые в 2004 году придумали, как из ДНК сделать нано - октаэдр. Хотя эта работа и сделана на 2 года раньше плоского ДНК-оригами, в тот раз был решен лишь частный случай (получение октаэдра из ДНК), а в работе по ДНК-оригами было предложено общее решение, поэтому именно работа 2006 года по ДНК-оригами считается основополагающей.
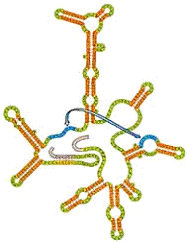
Октаэдр был сделан из одноцепочечной молекулы
ДНК длиной примерно 1700 нуклеотидов, имеющей комплементарные области и к тому
же скрепленной пятью 40-нуклеотидными ДНК-адаптерами, в результате был получен
октаэдр с диаметром 22 нанометра.