Материал: Применение плоскостной хроматографии в фитохимическом анализе
При бумажной хроматографии неподвижной жидкой фазой служит вода, адсорбируемая волокнами бумаги в количестве до 20%, ил другой полярный растворитель; в качестве подвижной фазы чаще всего применяют бутиловый спирт, коллидин, фенол, крезолы. Носителем служит хорошая фильтрованная бумага, достаточно однородная по толщине и плотности.
Для разделения смеси способом бумажной
хроматографии каплю исследуемого раствора наносят на полоску фильтрованной
бумаги шириной 15-20 мм и длиной 300-500 мм на расстоянии 20-30 мм от конца.
Конец полоски погружают в соответствующий органический растворитель,
предварительно насыщенной водой, а весь прибор помещают в герметическую камеру,
атмосфера в которой насыщена парами органического растворителя и воды. Движение
растворителя вдоль полоски бумаги, происходящее вследствие капиллярных сил,
обеспечивает проявление хроматограммы, причем отдельные зоны перемещаются с
различной скоростью.
2.2 Двумерная хроматография на бумаге
Еще более точные результаты получаются при
помощи так называемой двухмерной хроматографии на бумаге. Для этого варианта
применяют не полоски фильтрованной бумаги, а прямоугольники размером примерно
400Х500 мм. Каплю исследуемого раствора наносят вблизи одной из вершин
прямоугольника, а Хроматограмму проявляют дважды различными растворителями,
например фенолом и коллидином, сперва одним растворителем, а затем, после
поворота на 90◦, -другим.
2.3 Методы проявления хроматограмм
Восходящая хроматография. Бумага погружается нижним концом в подвижную фазу. Подъём жидкости происходит под действием капиллярных сил.
«+» Прибор прост, возможна количественная оценка результатов;
«-» Сила тяжести и капиллярные силы действуют в противоположных направлениях; скорость всасывания после подъема до 20 см сильно падает. Применима для веществ, имеющих достаточно большие различия в значениях Rf
Нисходящая хроматография. Бумага погружается в подвижную фазу верхним концом. Стекание жидкости происходит под действием силы тяжести.
«+» - быстрое прохождение подвижной фазы; отсутствие ограничения длины пробега пятен (проточная хроматограмма); возможно разделение веществ с незначительно отличающимися значениями Rf и количественная оценка результатов.
«-» - Прибор сложнее, чем для восходящей хроматографии.
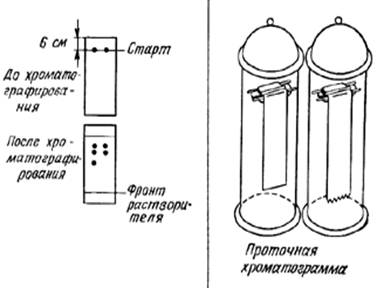
Рис. 5. Нисходящая хроматография
Радиально-горизонтальная хроматография. Подвижная фаза непрерывно наносится в центр круглого листа бумаги.
«+» - Быстрое выполнение, зоны узки и резко очерчены; большая полнота разделения, чем для первых методов.
«-» - Возможна только качественная
оценка результатов; применение «свидетелей» возможно только лишь при так
называемом «секретном методе» (т.е. при делении бумаги на секторы).
2.4 Приготовление подвижной фазы
Ниже описан простейший случай хроматографии на бумаге - восходящая хроматография с водой в качестве восходящей фазы.
Компоненты выбранной системы
растворителей смешивают в указанном соотношении в делительной воронке. Две
несмешивающиеся фазы доводят при помощи встряхивания до взаимного насыщения; в
качестве подвижной фазы выступает органическая.
2.5 Нанесение вещества
Из бумаги определенного сорта вырезают полоску, размер которой соответствует размерам применяемого для хроматографии цилиндра. На расстоянии 3 см от нижнего края карандашом наносят маркировочную линию. На этой линии через 2 - 2,5 см друг от друга и от краев полоски помечают точки старта. Специальной пипеткой наносят каждую точку старта; при этом образуются пятна около 1 см в диаметре. Затем растворителю дают испариться.
тонкослойный
хроматография растворитель бумага
2.6 Проявление
На дно цилиндра наливают подвижную фазу и
подвешивают полоску бумаги. Оставляют ее так висеть в течение ночи, а затем
нижний край полоски погружают на 0,5 см в подвижную фазу. После того как
растворитель поднимется на 20 - 25 см, полоску вынимают, отмечают карандашом
положение фронта растворителя и Хроматограмму высушивают.
Глава 3.Примеры применения плоскостной
хроматографии в фитохимическом анализе
.1 Фитохимическое исследование сырья Рыжика
озимого
С целью предварительной оценки компонентного состава надземной части рыжика озимого были проведены качественные реакции , в результате которых в траве, плодах и семенах рыжика были обнаружены флавоноиды. Качественные реакции с реактивом Драгендорфа, раствором танина, фосфорно-молибденовой и пикриновой кислот не дали осадков, что свидетельствует об отсутствии алкалоидов в надземной части рыжика. Как известно, для обнаружения кумаринов в растениях используются лактонные свойства кумаринов, их способность давать окрашенные растворы со специальными реактивами, а также флуоресцировать при ультрафиолетовом освещении . Для проведения качественных реакций получали извлечение из сырья 96% этиловым спиртом в соотношении 1:10 путем кипячения на водяной бане в течение 15-20 мин с обратным холодильником. С профильтрованным извлечением провели качественные реакции . В результате эксперимента мы обнаружили некоторые аналитические эффекты, поэтому предполагаем присутствие кумаринов в надземной части рыжика в следовых количествах. Проведенные качественные реакции на сапонины с водно-спиртовыми извлечениями из надземной части рыжика озимого дали отрицательный результат. В ходе выполнения эксперимента визуально было установлено наличие полисахаридов (слизей) в семенах рыжика, которые локализованы в клетках эпидермиса семян. С целью подтверждения их наличия, а также оценки количественного содержания были проведены соответствующие исследования. С использованием методик, установлено, что содержание полисахаридов в семенах рыжика составляет от 20,50±0,92% до 22,68±0,98 %. 63 Для более детального анализа содержания БАВ в надземной части рыжика использовались такие методы анализа, как ТСХ, спектрофотометрия. Сравнительное ТСХ-исследование надземных органов рыжика озимого. Оценка качественного состава компонентов сырья рыжика озимого проводилась методом тонкослойной хроматографии (ТСХ). Исследовались водно- спиртовые извлечения стеблей, листьев, плодов, семян рыжика. При этом в качестве оптимального экстрагента был выбран 50% спирт этиловый. На хроматограмме обнаруживается три вещества, в том числе в виде доминирующего пятна желто-оранжевого цвета с величиной Rf около 0,4, а также другие пятна. На основе результатов хроматографического исследования органов надземной части растения (стебли, листья, цветки, плоды, семена) выявлено присутствие флавоноидов, в частности, нарциссина, как характерного доминирующего компонента, во всех сравниваемых органах, а также еще трех веществ флавоноидной природы. Ввиду того, что доминирующий флавоноид нарциссин содержится во всех органах надземной части ,в качестве сырья как источника флавоноидов целесообразно применение травы рыжика, т.е. всей его надземной части, в том числе плодов. Так как основным сырьем рыжика являются семена, дальнейшие исследования были направлены на изучение их химического состава. Для качественного определения флавоноидов в семенах рыжика озимого предложен метод тонкослойной хроматографии, УФ-спектроскопии. В ходе разработки методики качественного анализа семян рыжика были проведены исследования по подбору оптимальных условий хроматографирования, позволяющих эффективно разделить и идентифицировать доминирующие БАС - нарциссин, изорамнетин, никотифлорин, кемпферол. В результате проведенных опытов с различными хроматографическими системами, содержащими в различных соотношениях хлороформ, этанол, воду, было установлено, что наиболее четкое разделение компонентов удается достичь в системе растворителей хлороформ - спирт этиловый - вода (26:16:3). При просмотре хроматограммы в УФ-свете при длине волны 254 нм обнаруживаются пятна с фиолетовой флуоресценцией на уровне пятен растворов нарциссина (величина Rf около 0,4), изорамнетина, никотифлорина (величина Rf около 0,45). Хроматограмму проявляли щелочным раствором диазобензолсульфокислоты (ДСК), затем хроматографические пластинки нагревали при температуре 100-105 оС в течение 2-3 мин в сушильном шкафу. В 71 результате обнаруживались пятно желто-оранжевого цвета с величиной Rf около 0,4 - нарциссин .
Методика качественного ТСХ-анализа семян рыжика
озимого. В колбу со шлифом вместимостью 50 мл помещают около 1 г (точная
навеска) измельченного сырья (пробу сырья измельчают до размера частиц,
проходящих сквозь сито с отверстиями диаметром 1 мм), приливают 50 мл спирта
этилового 50% и взвешивают на тарирных весах с точностью до ±0,01. Колбу с
содержимым присоединяют к обратному холодильнику и нагревают на кипящей 72
водяной бане в течение 1 ч. После охлаждения колбу взвешивают, доводят ее
содержимое спиртом 50% до первоначальной массы, перемешивают и фильтруют через
бумажный фильтр (красная полоса). На линию старта пластинки «Сорбфил
ПТСХ-АФ-А-УФ» микропипеткой наносят 0,02 мл извлечения и 0,02 мл 0,1% раствора
нарциссина в виде пятен диаметром около 5 мм. Пластинку с нанесенными пробами
помещают в камеру со смесью растворителей: хлороформ - спирт этиловый - вода
(26:14:3) и хроматографируют восходящим способом. Когда фронт растворителей
пройдет около 8 см, пластинку вынимают из камеры, сушат на воздухе в течение 10
мин и просматривают в УФ-свете. При просмотре хроматограммы в УФ-свете при
длине волны 254 ннм обнаруживается пятно фиолетового цвета на уровне пятна
нарциссина с величиной Rf около 0,4; допускается наличие других пятен. Затем
пластинку опрыскивают раствором диазобензолсульфокислоты и помещают в сушильный
шкаф на 2 мин при 100-105 оС. При этом на уровне пятна нарциссина
обнаруживается доминирующее пятно желто-оранжевого цвета с величиной Rf около
0,4 (нарциссин); допускается наличие других пятен. Примечание: 1. Подготовка
пластинок. Пластинки «Сорбфил ПТСХ-АФ-А-УФ» разрезают поперек линий накатки на
3 части размером 10х5 см и перед использованием активируют в сушильном шкафу
при 100-105 оС в течение 1 ч. 2. Приготовление раствора диазобензолсульфокислоты.
0,01 г диазобензолсульфокислоты (ГФ Х, стр. 876) растворяют в 10 мл 10%
раствора натрия карбоната. Раствор используют свежеприготовленным.
3.2 Определение качественного состава
биологически активных веществ в листьях Калины
В настоящее время актуальным является
комплексное использование различных частей лекарственных растений. Объектом
изучения было выбрано растение калина обыкновенная (Viburnum Opulus L.,
семейство жимолостные - Caprifoliaceae). Калина давно используется в качестве
лекарственного растительного сырья. О лечебном значении калины имеются сведения
в древних травниках (XVI в.), в которых ей приписываются ценные целебные
свойства: улучшает работу сердца, оказывает мочегонное действие, полезна при
неврозах, со- судистых спазмах и гипертонии . В настоящее время в качестве
лекарственного растительного сырья используются такие части растения, как кора
и плоды. Кора содержит дубильные вещества пирокатехиновой группы (около 2%),
флобафены, флавоноиды, иридоиды, гликозид вибурнин, кроме того, калины кора
накапливает достаточно большое количество липофильных веществ. При этом в
состав омыляемой части входят органические кислоты - муравьиная, уксусная,
изовалериановая, каприновая и др. В состав неомыляемой - фитостеролин,
фитостерин, тритерпеновые сапонины (около 6%) . Так же, в калины коре
содержатся хлорогеновая, неохлорогеновая, кофейная, урсоловая и олеаноловая
кислоты, соли валериановой и каприловой кислот, витамины, сахара. Калины кора
улучшает функции желудка, кишечника, понижает кровяное давление, оказывает
противоспазматическое, успокаивающее, кровоостанавливающее,
противовоспалительное, антисептическое действие, тонизирует, повышает
трудоспособность. Кора оказывает сосудосуживающее действие, связанное с
гликозидом вибурнином, находящимся в коре растения. Как кровоостанавливающее и
противовоспалительное средство препараты из калины коры применяют при геморрое
и заболеваниях желудочно-кишечного тракта . Калины плоды содержат сахара (до
32%), пектиновые вещества, фитостерины, аминокислоты, танниды (3%),
каротиноиды, витамины Р, К, каротиноиды, дубильные вещества (до 3%),
аскорбиновую кислоту, анто- цианы, изовалериановую и уксусную кислоты, жирное
масло. Плоды назначают как общеукрепляющее средство, в особенности для
выздоравливающих больных, их применяют при кожных заболеваниях, отеках
сердечного и почечного происхождения, при гипертонической болезни, гастритах, и
заболеваниях печени . Калины плоды усиливают работу сердца, оказывают вяжущее,
антисептическое, кровоостанавливающее, желчегонное, мочегонное действие,
понижают кровяное давление, ускоряют заживление ран, язв. Цветки и плоды
используют для лечения гипертонии, одышки, склероза, туберкулеза легких,
злокачественных опухолей, болезней почек. Отвар из корней помогает от
бессонницы . Представляется интересным исследование калины листьев в качестве
потенциального источника биологи чески активных веществ. В качестве объекта
исследования использовали листья калины обыкновенной. Листья высушивали на
воздухе при температуре 22±2°С в хорошо проветриваемом
помещении, исключая попадания прямых солнечных лучей. Проводили определение
качественного и количественного состава биологически активных веществ,
содержащихся в калины листьях. Для определения качественного состава
биологически активных веществ использовали метод цветных реакций и тонкослойной
хроматографии. Тонкослойную хроматографию проводили в тонком слое сорбента на
пластинах ―Sorbfil‖ в системе
растворителей бутанол - ледяная уксусная кислота - вода в соотношении 4:1:5.
Длина пробега фронта составила 105 мм. На хроматограмму наносили извлечения,
полученные на основе воды очищенной и спирта этилового 40%. Полученные
хроматограммы проявляли двумя способами - в парах аммиака и 2% раствором
нингидрина в спирте.
3.3 Идентификация дубильных веществ из клубней
Георгины простой
Род георгина (Dahlia Cav.) относится к семейству
сложноцветных (Asteraceae). Георгина простая или од- норядная (Dahlia single
L.) - сорт георгины разнообразной (Dahlia variabilis), который длительно
культивируется в Ставропольском крае и широко используется для озеленения
парков и садов. Объектом исследования служили воздушно-сухие измельчѐнные
клубни георгины простой. Из литературных источников известно, что клубни
георгины богаты инулином (до 43%), низкомолекулярными полифруктанами (20-22%),
содержат фитин (смесь кальциевых и магниевых солей различных инозит- фосфорных
кислот), алкалоид тригонеллин, ванилин (0,01%) . Однако данные о комплексном
изучении химического состава данного объекта достаточно скудны. Целью данного
исследования являлось установление дубильных веществ клубней георгины простой.
Дубильные вещества, как и другие фенольные соединения, образуют окрашенные
комплексы с солями тяжелых металлов, вступают в реакции сочетания с
диазониевыми соединениями, дают осадки с высокомолекулярными веществами . Для
проведения качественных реакций из растительного сырья готовили водное
извлечение. Приготовление извлечения: 1 г измельченного растительного сырья
заливают 100 мл воды. Нагревают на водяной бане в течение 20-30 мин, процеживают
через вату и полученное извлечение используют для проведения соответствующих
качественных реакций. В результате проведения качественных реакций установлено,
что при взаимодействии с 1% раствором желатина появлялась муть, исчезающая от
избытка реактива; с 1% раствором хинина гидрохлорида возникал аморфный осадок;
с 1% раствором антипирина - аморфный осадок; с раствором железоаммониевых
квасцов (ЖАК) - чѐрно-зелѐное окрашивание (конденсированные
дубильные вещества) и осадок; при добавлении смеси кислоты хлороводородной и
40% раствора формальдегида после кипячения образовался осадок (конденсированные
дубильные вещества), осадок отфильтровывали и к фильтрату добавляли раствор ЖАК
и кристаллический свинца ацетат, фиолетовое окрашивание не образовалось (предположительно
гидролизуемые дубильные вещества отсутствуют); при добавлении 10% раствора
кислоты уксусной, 10% раствора средней соли свинца ацетата не образовался
осадок (предположительно гидролизуемые дубильные вещества отсутствуют); в
извлечение прибавляли натрия нитрат и 0,1 М кислоты хлороводородной - бурое
окрашивание (конденсированные дубильные вещества). На основании проведѐнных
качественных реакций можно сделать предположение, что в клубнях георгины
простой содержится конденсированная группа дубильных веществ и отсутствует
гидролизуемая группа. Для идентификации дубильных веществ из клубней георгины
простой получали спиртовое (95% спирт этиловый) и водное извлечения, проводили
бумажную хроматографию на бумаге марки ―Filtrak‖ и
тонкослой- 8 Фармакогностическое и ботаническое изучение лекарственных растений
ную хроматографию на пластинках ―Silufol‖. В
качестве стандартных образцов использовали СО эпикатехина (конденсированные
дубильные вещества), СО танина и СО галловой кислоты (гидролизуемые дубильные веще-
ства). Разделение осуществляли в системах растворителей н-бутанол - уксусная
кислота - вода (4:1:5) и (4:1:2), 15% и 60% уксусная кислота. Обнаружение зон
веществ на хроматограмме проводили в УФ свете, с последую- щей обработкой 1%
раствором железоаммониевых квасцов или 1% раствором ванилина в
концентрированной кислоте хлороводородной . В ходе исследований по
идентификации дубильных веществ выявлена лучшая разделяющая способность ТСХ в
системе растворителей БУВ (4:1:5). Водное извлечение из клубней георгины
простой разделилось на 4 пятна, спиртовое извлечение из клубней георгины
простой - на 5 пятен. После хроматографического анализа спиртового и водного
извлечения из клубней георгины простой вы- явили пятно со сходными
характеристиками: в водном извлечении - пятно № 3, в спиртовом - пятно № 5,
идентифицированное как эпикатехин. Для спектрофотометрического определения зону
вещества, предварительно идентифицированную как эпи- катехин, элюировали со
слоя сорбента спиртом этиловым 95%, измеряли спектр поглощения в интервале
250-420 нм. Параллельно измеряли спектр СО эпикатехина. Конфигурации
спектральных кривых идентичны, УФ спектр исследуемого вещества имеет максимумы
поглощения при 272 и 380 нм.
Заключение
ТСХ незаменима в анализе растительного сырья и
растительных препаратов. Метод ТСХ легок в исполнении и не требует дорогого
оборудования. В испытаниях на подлинность ТСХ используют для сравнения
поведения природных соединений в анализируемом ЛРС и стандартного образца,
который аутентичен одному из действующих веществ в экстракте. Одной из
характеристик разделения веществ является величина удержания (Rf), которая
используется для установки подлинности. Она показывает положение зоны вещества
на хроматографической пластине. На полученной хроматограмме отношение
расстояния, пройденного на адсорбенте данным веществом к расстоянию,
пройденному передним фронтом движущей фазы, является величина Rf, которая
характерна для данного вещества в данной хроматографической системе. Отношение
расстояний, пройденных испытуемым веществом и стандартным образцом, принимают
за величину Rf. Величину удержания (Rf) рассчитывают по следующей формуле:Rf =
b/a, где a - расстояние от линии старта к линии фронта, пройденной системой
растворителей, мм; b- расстояние от линии старта до верхнего края пятна, мм; с-
расстояние от линии старта до верхнего края пятна стандартного образца, мм.Для
количественных изменений пятно возможно удалять с пластинки, элюируя вещество
подходящим растворителем, а потом определить его достаточно чувствительным
методом, например, спектрофотометрическим.Хроматограммы изучают визуально при
дневном и УФ свете. Отмечают границы и окраску пятен. Отмечают расстояние между
линией старта до верхней границы каждого пятна. Основное пятно на
хроматограмме, которая получена для испытуемого раствора, сравнивают с
соответствующим пятном на хроматограмме, которая получена для раствора
стандартного образца.При этом обязательно проверяют чувствительность -
чувствительность вычисляется любым способом, если пятно четко видно на
хроматограмме, полученной из наиболее растворенным раствором сравнения.
Список литературы
Борисова, А.Г. Флора СССР / А.Г. Борисова, В.П. Бочанцев, И.Т. Васильченко. - М.: Издательство Академии наук СССР, 1959. - С. 548-551.
Берлин А.Я. «Техника лабораторной работы в органической химии» - М. : ГХИ, 1952
Гринкевич, Л.И. Химический анализ лекарственных растений / Л.И. Гринкевич, Л.М. Сафронич. - М.: Мир, 1983. - С. 111-122.
Государственная фармакопея СССР: Общие методы анализа. Лекарственное растительное сырьѐ / МЗ СССР. - 11-е изд., доп. - М.: Медицина, 1990. - Вып. 2. - 400 с.
Государственная фармакопея Российской Федерации. - 12 изд. - М., 2007. - Ч. 1. - 596 с.
Запрометов, М.Н. Основы биохимии фенольных соединений / М.Н. Запрометов. - М.: Медицина, 1974. - 214 с.
Калинин, Ф.Л. Справочник по биохимии / Ф.Л. Калинин, В.П. Лобов, В.А. Жидков. - Киев: Наукова думка, 1971. - 1116 с.
С. А. Кибардин, К.А.Макаров «Тонкослойная хроматография в органической химии» - М. : Химия, 1978
Органикум; Практикум по органической химии : пер. с нем. / Г. Беккер, В. Бергер, Г. Домшке и др. - М. : Мир, 1979
Федосеева, Г.М. Способы определения полифенольных соединений в растительном сырье / Г.М. Федосеева // Химия раст. сырья. - 1981. - № 9. - С. 28-37.