Материал: Поведение хромосом в клеточном цикле
Конъюгация или синапсис - попарный контакт
параллельно расположенных и слабо конденсированных гомологичных хромосом.
Конъюгация и формирование синаптонемального комплекса (СК) отсутствует у
низшего гриба Aspergillusnidulans, дрожжей Sc. Pombe и у самцов некоторых мух,
например Drosophilamelanogaster.
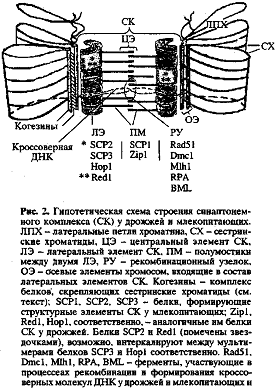
Рисунок 2. Строение синаптонемального комплекса
После премейотическойS-фазы две сестринские хроматиды хромосомы формируют общий осевой элемент. Осевые элементы гомологичных хромосом включаются в виде латеральных (боковых) элементов в СК. Формируется синаптонемный комплекс (СК) - из белковых осей двух гомологичных хромосом и центрального элемента. Ширина боковых элементов составляет 30-60 нм, ширина центрального элемента - 60-120 нм. Боковые элементы состоят из мейоз-специфичных белков. Между ними формируются белковые перемычки. Первым специфическим белком СК (появляется еще в интерфазу) является белок REC8. ДНК гомологичных хромосом в виде петель отходят от боковых (латеральных) элементов СК. Большая часть ДНК локализована вне СК, лишь 0,5% геномной ДНК входит в СК, прочно связываясь с белками. Небольшое количество ДНК проходит через центральное пространство СК. ДНК СК состоит их уникальных и умеренно повторяющихся последовательностей, которые могут взаимодействовать с белками СК и белками, участвующими в рекомбинации и сегрегации гомологичных хромосом.
На 90% СК состоит из белков. Выделяют 5-10 мажорных белков с молекулярной массой от 26 до 190 кДа. У млекопитающих хорошо изучены 3 белка СК - SCP1, SCP2, CSP3 (synaptonemalcomplexprotein). Белки СК дрожжей назвали Zip1, Zip2, Red1, Hop1.
Белок SCP1 - основной белок поперечных филаментов СК. С-концы этого белка «заякорены» на латеральных элементах СК и взаимодействуют здесь с ДНК, N-концы достигают центрального пространства СК и соединяют противоположные латеральные элементы СК с помощью белок-белковых взаимодействий.
У дрожжей белок Zip1 является основным белком поперечных филаментов СК. Белок Zip2 действует как инициатор синапсиса, образуя центры полимеризации белка Zip1.
Белки SCP2, SCP3- белки латеральных элементов СК. Совместно локализуются вдоль осевых элементов хромосом и латеральных элементов СК. После диплотены концентрируются в центромерах хромосом, хотя небольшое их количество обнаруживается вдоль плеч хромосом. Т.о. эти белки участвуют в сцеплении - когезии сестринских хроматид. К белкам когезинам относятся и митоз-специфические белки - Smc1p, Smc3p, Scc1p, Scc3p.
У дрожжей белок Red1 образует центры формирования осевых элементов. Он взаимодействует с белком Hop1, который тоже является компонентом латеральных элементов СК у дрожжей.
Основа протяженных латеральных элементов- комплекс из четырех белков когезинов. Накануне мейоза в хромосомах появляется специфичный белок когезин Rec8, который заменяет соматический когезин Rad21. Затем к нему присоединяются три других белка-когезина, присутствующие и в соматических клетках, новместо соматического когезина SMC1 появляется специфический для мейоза белок SMC1b (его N-конец на 50% отличается от N-конца соматического белка SMC1). Этот когезиновый комплекс располагается внутри хромосомы между двумя сестринскими хроматидами, удерживая их вместе. Скомплексом когезинов связываются мейоз-специфичные белки, которые становятся мажорными белками хромосомных осей и превращают их в латеральные элементы синаптонемного комплекса.
Регуляция сборки белков в СК происходит с помощью фосфорилирования-дефосфорилирования. Многие белки СК содержат по несколько сайтов фосфорилирования протеин-киназой р34.
В составе СК выделяют рекомбинационные узелки: ранние - на стадии лептотены и зиготены, локализуются в боковых элементах СК на участках инициации рекомбинации. В состав ранних рекомбинационных узелков входят ферменты, которые необходимы для инициации двунитевых разрывов в ДНК и формирования однонитевых концов. Например белок Spo11p (топоизомераза) - основная мейоз-специфичная эндонуклеаза, которая осуществляет двойные разрывы в ДНК. Поздние рекомбинационные узелки обнаружены на стадии пахитены, локализуются в центральном элементе СК. Обнаружена связь между числом и распределением поздних рекомбинационных узелков и числом и распределением хиазм в биваленте. Таким образом, поздние узелки - мультиферментные комплексы, катализирующие кроссинговер.
Инициация формирования СК у дрожжей и растений происходит в нескольких точках по всей длине бивалента (6 сайтов инициации у кукурузы, до 36 у лилии); у животных формирование СК начинается с теломер и распространяется по типу застежки «молнии». Завершение формирования СК - пахитена, его разрушение - диплотена.
Функции СК: - удерживает гомологичные хромосомы строго напротив друг друга;
препятствует слипанию гомологичных хромосом - обратимая конъюгация;
обязательная предпосылка для кроссинговера.
У мутантов с отсутствием конъюгации отсутствует и кроссинговер.
Рожь. 3 группы рецессивных мутаций, нарушающих формирование СК.
мутации сильногоасинапсиса. Мутации блокируют конъюгацию хромосом при переходе от лептотены к зиготене.
Мутации слабогоасинапсиса или десинапсиса - самая многочисленная группа. У ржи данные мутации нарушают конъюгацию в 1-3 парах хромосом из 7. Наблюдаются как диваленты, так и униваленты; подавление формирования СК на концах хромосом; внутренние участки асинапсиса или десинапсиса. Снижается частота появления хиазм, частота кроссинговера.
Мутации индискриминантного синапсиса - одновременное присутствие гомологичного и негомологичного синапсиса, что приводит к появлению мультивалентов и унивалентов. Латеральные элементы СК могут сформировать складки из-за синапсиса «на себя».
Синапсис Х и Y хромосом
У слепушонки (род полевок) Х и Y хромосомы формируют короткий СК в ранней пахитене (конъюгируют короткими плечами), в диплотене происходит десинапсис и половые хромосомы становятся унивалентами.
Для ХY-бивалента большинства млекопитающих характерна концевая конъюгация половых хромосом (длинные плечи Х и Y хромосом), отсутствие которой нарушает расхождение половых хромосом в мейозе. Конъюгируют Х и Y хромосомы за счет гомологичного участка, содержащего такие гены как ген общей цветовой слепоты, пигментной ксеродермы, геморрагического диатеза.
ХY-бивалент выключается из метаболизма клетки путем образования полового пузырька, внутри которого неконъюгированные участки хромосом находятся в конденсированном состоянии.
Х хромосома может ассоциироваться с аберрантными
хромосомами (транслоцированными, инверсионными). Это защитный механизм - если Х
хромосома тесно ассоциирована с аберрантной, то вокруг полового бивалента не
образуется половой пузырек. Это служит сигналом для остановки мейоза на стадии
пахитены. Это предотвращает попадание поврежденных хромосом в половые клетки.
.2 Реципрокная
рекомбинация и конверсия
В ходе синапсиса гомологичные хромосомы
обмениваются фрагментами. В световом микроскопе последствия этого обмена видны
как перекресты, или хиазмы.
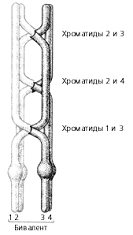
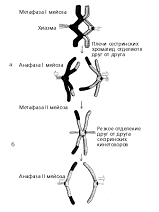
Рисунок 3. Хиазмы в результате трех отдельных
перекрестов хроматид обеих хромосом и последующее расхождение хромосом
Частота рекомбинаций определяется по формуле 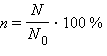 ,
где N - количество рекомбинантов,
,
где N - количество рекомбинантов, ![]() -
общее количество потомков. В то же время частота рекомбинаций определяет число
рекомбинаций, происходящих при образовании гамет.
-
общее количество потомков. В то же время частота рекомбинаций определяет число
рекомбинаций, происходящих при образовании гамет.
Частота рекомбинаций генов показывает относительное расположение сцепленных генов в хромосоме: чем дальше друг от друга находятся гены, тем выше частота рекомбинации. Это обстоятельство используется при составлении генетических карт. Условное «расстояние» между локусами двух генов считается прямо пропорциональным частоте рекомбинации. Взаимное расположение локусов трёх и более генов определяется методом триангуляции. При этом сначала берутся гены с наименьшей частотой рекомбинации. Далее выбирают следующую по величине частоту рекомбинации и указывают два возможных положения нового гена; одно из этих положений будет отсеяно на следующем шаге, когда берётся третья частота. В реальных экспериментах генетические карты могут искажаться благодаря двойному кроссинговеру, когда рекомбинация происходит одновременно в двух точках. Двойной кроссинговер особенно характерен для генов, локусы которых разделены большими расстояниями
В настоящее время общепризнаны две модели
рекомбинации, приводящие к конверсии. Одна из них - модель Р. Холлидея, вторая
- Дж. Жостака и др., в которой рекомбинация начинается с двуцепочечного разрыва
в одном из гомологов. Для краткости изложения ограничимся демонстрацией
конверсии на примере модели Холлидея. В рисунок 23 включены только те ее этапы,
которые непосредственно относятся к конверсии. Если в тетраде произошел
кроссинговер в участке гена В, то соотношение аллелей генов А и С, внешних
(фланговых) по отношению к участку кроссинговера, не изменяется и остается
равным 2А : 2а и 2С : 2с, то есть рекомбинация по ним реципрокна. Напротив,
рекомбинация маркеров, попавших непосредственно в участок кроссинговера, то
есть в гетеродуплекс, обычно нереципрокна из-за коррекции неспаренных
оснований, внесенных разными аллелями (B и b). Протяженность гетеродуплекса в
мейотической рекомбинации достигает 1 т.п.н., в случае митотической
рекомбинации она еще больше. Все гетерозиготные маркеры, попавшие в
гетеродуплекс, обычно конвертируют совместно, что является следствием
существования участка конверсии. Этот факт основан на работе рассмотренной выше
системы коррекции с вырезанием и застройкой длинных брешей.
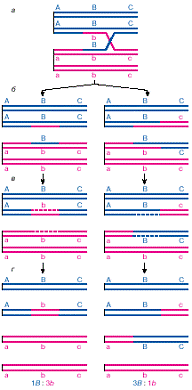
Рис. 4 Упрощенная схема конверсии гена по модели Холлидея. Линии соответствуют цепям ДНК, две параллельные линии - хроматиде. Синий и красный цвета позволяют различать гомологов. Вертикальные линии слева обозначают центромеры, удерживающие сестринские хроматиды. Пара синих и пара красных сестринских хроматид образует тетраду. а - полухиазмаХоллидея, сформированная в результате обмена цепями между двумя хроматидами с последующей миграцией ветвления; б - два типа продуктов рекомбинации, возникшие в результате двух способов разрешения полухиазмы. Слева структуры с гетеродуплексом, но без кроссинговера по внешним маркерам. Справа структуры с гетеродуплексом и кроссинговером по внешним маркерам; в - в левой тетраде происходит конверсия от В к b, в правой - от b к В. Направление конверсии в тетрадах выбрано произвольно. Также произвольно выбрана и стадия, на которой происходит конверсия. Она может осуществляться и раньше, до разрешения полухиазмы; г - продукты рекомбинации клеточный цикл хромосома синапсис
А теперь выделим другие основные закономерности
процесса конверсии. Конверсия обычно равнонаправленна. Выбор удаляемого основания
из двух неспаренных случаен, поэтому тетрады 3B : 1b и 1B : 3b равновероятны.
Конверсия полярна. Это проявляется в том, что частоты конверсии разных аллелей
одного гена закономерно снижаются, начиная с определенной точки, чаще всего от
одного конца гена к другому. У дрожжей они обычно варьируют от 18% до долей
процента. Так как частота конверсии аллеля зависит от вероятности его попадания
в гетеродуплекс, то полярность указывает на наличие в хромосомах фиксированных
сайтов, в которых инициируется рекомбинация. В последние годы у дрожжей
идентифицировано несколько таких сайтов. Их называют горячими точками
рекомбинации.
Литература
Башкиров В.Н. Происхождение гетерохроматина уэукариот // Генетика. 2002. № 6. С. 789
Беридзе Т. Сателлитная ДНК. М.: Наука. 1982. 121с.
Бужиевская Т., Выговская Т.. Анеуплоидия у человека (факты и гипотезы).// Цитология и генетика.- 1990.-24.-66-72.
Вершинин А. Эпигенетика специфических районов хромосом // Генетика. 2006. Т. 42. № 9. С. 1200-1214.
Ворсанова С., Казанцева Л., Демидова И., Юров Ю.. Использование методов молекулярно-цитогенетической диагностики в практике генетического консультирования.// Информационное письмо.-1990.- 10.
Ворсанова С., Юров Ю., Демидова И., Вехова Н.. Хромосомные аномалии у детей с недифференцированными формами умственной отсталости по данным молекулярно-цитогенетических исследований.// Цитология и генетика.- 1993. - 27. - 3. - 72-78
Гайцхоки В., Паткин Е. Сателлитные ДНК и болезни - возможные механизмы // Генетика. 2000. № 7. С. 869
Геномика - медицине. М.: ИКЦ «Академкнига». 2005. 392С.
Давиденкова Е., Верлинская Д., Тысячнюк С.. Клинические синдромы при аномалиях половых хромосом.// Л.- Медицина.-1973.-198.
Ершикова Ю. Половой хроматин. Методы выявления и значение в клинической практике. М, 1971. 26с.
Жимулев И. Гетерохроматин и эффект положения гена. Новосибирск, Наука, 1993. 490с.
Жимулев И., Беляева Е. Гетерохроматин, эффект положения гена и генетический сайленсинг // Генетика. 2003. Т. 39. № 2. С. 187-201.
Иллариошкин С.Н. ДНК-диагностика и медико-генетическое консультирование. М.: Медицинское информационное агентство. 2004. 207с.
Козлова С., Демикова Н., Семанова Е., Блинникова О. Наследственные синдромы и медико-генетическое консультирование.//М. Практика, 1996.-305.
Коряков Д.Е. Модификация гистонов и регуляция работы хроматина // Генетика. 2006. Т. 42. № 9. С. 1170-1185.
Лазюк Г. Тератология человека.//М. Медицина, 1991.- 434.
Лазюк Г.И., Лурье И.В., Черствой Е.Д. Наследственные синдромы множественных пороков развития.-М.:Медицина,1983. 441с.
Лильин Е.Т., Богомазов Е.А., Гоман-Кадошников П.Б. Генетика для врачей- М., Медицина, 1990. 257с.
Льюин Б. Гены. М. «Мир». 1987. 544с.
Прокофьева-Бельговская А. Гетерохроматические районы хромосом. М.: Наука. 1986. 432с.
Фогель Ф., Мотульски А. Генетика человека. М. «Мир». 1989. Т.1. 312с.
Ченцов Ю.С. Современные представления о строении митотических хромосом // Соросовский образовательный журнал. 1996. № 8. С. 14-22.
Черных В., Курило Л. Генетический контроль дифференцировки пола у человека // Генетика. 2001. Т. 37. № 10. С. 1317-1329.
Черных В., Чухрова А., Бескоровайная Т., Гришина Е. Типы делецийY-хромосомы и их частота у мужчин с бесплодием // Генетика. 2006. Т. 42. №. 8. С. 1130-1136.
Шевченко А., Павлова С., Дементьева Е., Голубева Д., Закиян С. Модификации хроматина в процессе инактивации Х-хромосомы у самок млекопитающих // Генетика. 2006. Т. 42. № 9. С. 1225-1234.
Шишкина Г., Дыгало Н. Гены, гормоны и факторы риска формирования мужского фенотипа // Успехи физиологических наук. 1999. Т. 30. № 3. С. 49-61.F.J., Coluzzi M. Chromosome speciation: human, Drosophila, and mosquitoes // Proc. Natl Acad. Sci. USA. 2005. V. 102. P. 6535-6542.C., Zoghbi H. Fourteen and counting: unraveling trinucleotide repeat diseases // Hum. Mol. Genet. 2000. V. 9. P. 909-916.Y., Linardopoulou E., Friedman C. Genomic structure and evolution of the ancestral chromosome fusion site in 2q13-2q14.1 and paralogous regions on other human chromosomes // Genome Res. 2002. V. 12. № 11. P. 1651-1662.J., Hochstenbach R., Hauschten-Jungen E., Beukeboom L. Is the Y chromosome of Drosophila an evolved supernumerary chromosome? // BioEssays. 1996. V. 18. P. 317-323.S.B., Kumar S. Genomics. Vertebrate genomes compared // Science. 2002. V. 297. № 5585. P. 1283-1285.P., Warren S. Understanding the molecular basis of fragil X syndrome // Hum. Mol. Genet. 2000. V 9. P. 901-908.B. Genes. OxfordUniversity Press. 1994. 1272p. W.J., Larkin D.M., Everts-van der Wind A. et al. Dynamics of mammalian chromosome evolution inferred from multispecies comparative maps // Science. 2005. V. 22. № 309. P. 613-617.J.H., Taylor B.A. Lengths of chromosomal segments conserved since divergence of man and mouse // Proc. Natl. Acad. Sci. USA. 1984. V. 81. № 3. P. 814-818.D.W., de Bruyn B., Lovin D.D. Comparative genome analysis of the yellow fever mosquito Aedesaegyptiwith Drosophila melanogaster and malaria vector mosquito Anopheles gambiae// J. Heredity.2004. V. 95. P. 103-113.R.H., Lindblad-Toh K., Birney E. et al. Initial sequencing and comparative analysis of the mouse genome // Nature. 2002. V. 5. № 420. P. 520-562.A., Pruss D. Deviant nucleosomes: the functional specialization of chromatin // Trends in Genetics. 1996. V12. P. 58-62.