Материал: Потенциометрический анализ лекарственного препарата: фенибут
На основе этих данных построены кривые потенциометрического титрования. А
именно графики зависимости: рН от объема титранта (Рис.5.), ЭДС от объема
титранта (Рис.6.), ∆E/∆V от объема титранта(Рис.7.), ∆V/∆E от объема титранта (Рис.8.).
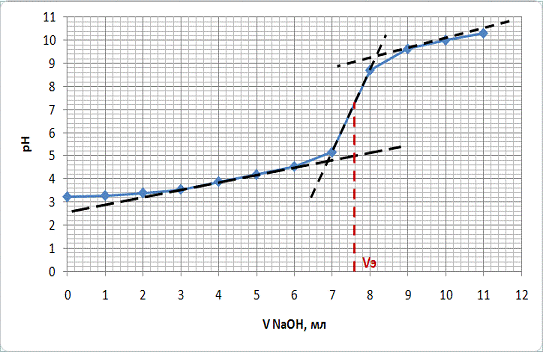
Рисунок 5 - Интегральная кривая. График зависимости рН от объема титранта
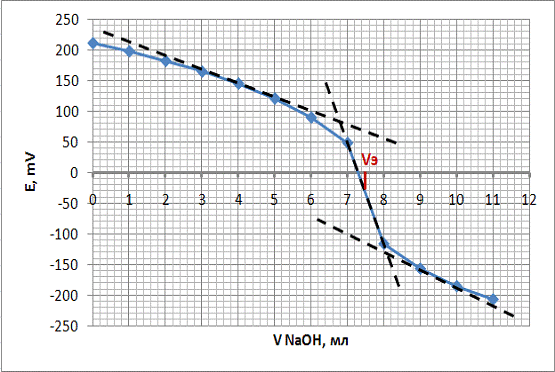
Рисунок 6 - Интегральная кривая. График зависимости ЭДС от объема
титранта
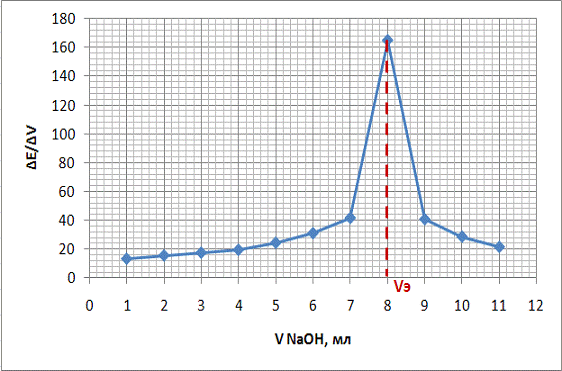
Рисунок 7 - Дифференциальная кривая. График зависимости ∆Е/∆V от объема титранта
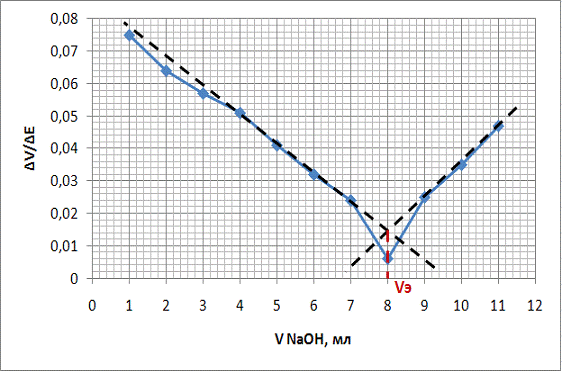
Рисунок 8 - Кривая титрования Грана. График зависимости -∆V/∆E от объема титранта.
Расчет содержания активного вещества по экспериментальным данным
Прямая потенциометрия.
Была измерена ЭДС 100 мл раствора 1 таблетки препарата, которая составила
201,6 мВ. По графику зависимости E от -lgC кислоты можно определить
концентрацию активного вещества (Рис. 9)
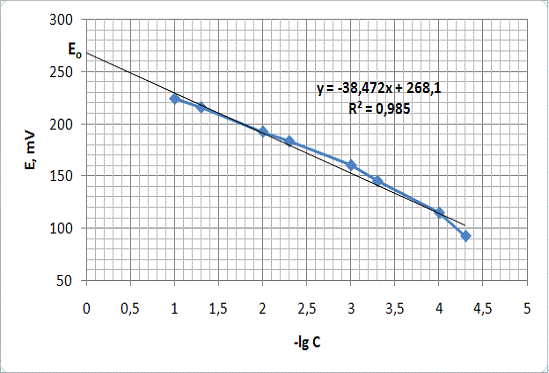
Рисунок 9 - Определение концентрации вещества методом прямой
потенциометрии
Из уравнения прямой:
=-38,473x+268,1
x =
(268,1-201,6)/38,473 = 1,73
отсюда концентрация активного вещества:
С = 10-1,47 = 0,018 М
Был также измерен pH 100
мл раствора 1 таблетки препарата, который составил 3,234. По графику
зависимости pH от -lgC кислоты (Рис.10):
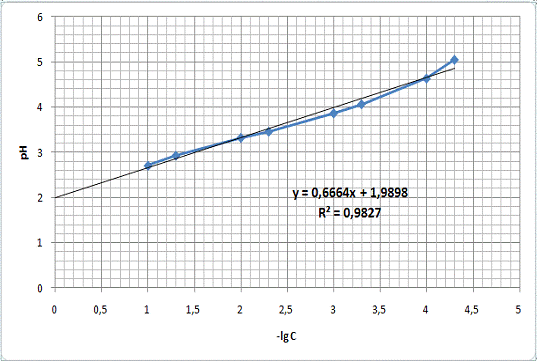
Из уравнения прямой:
=0,6664x+1,9898
x =
(3,234-1,9898)/0,6664 = 1,868
отсюда концентрация активного вещества:
С = 10-1,868 = 0,013 М
Средняя концентрация по данным pH и E для прямой потенциометрии:
Сср = (0,018+0,013)/2 = 0,015 М
Масса активного вещества в 100 мл:
= [(0,015 М * 100 мл) / 1000 мл]*179,216 г/моль = 0,26 г
Потенциометрическое титрование
Найдем концентрацию активного вещества исходя из количества затраченного титранта.
Данные, полученные из графиков:
э интегр E = 7,6 мл
Vэ интегр pH = 7,5 мл
Vэ дифф = 8,0 мл
Vэ гран = 8,0 мл
Vэ ср = (7,6 + 7,5 + 8,0 + 8,0)/4 = 7,775 мл
В 7,775 мл 0,0909 М раствора щелочи содержится:
n = (0,0909 М *7,775 мл) /1000 мл = 0,706*10-3 моль
Отсюда масса оттитрованного вещества:
m = 0,706*10-3 моль * 179,216 г/моль = 0,1265 г
Тогда масса вещества в 100 мл этого раствора:
m =
0,1265*2 = 0,253 г
Расчет относительной погрешности
Относительная погрешность определяется по следующей формуле:
δ = ![]() · 100%,
· 100%,
где стеор - теоретическое (расчетное) значение величины; Δ - абсолютная погрешность,
рассчитываемая по формуле:
Δ = |спрак - стеор|
· для прямой потенциометрии
Δ (фенибут) = |0,26 г - 0,25 г| = 0,01 г
δ (фенибут) = ![]() · 100% =
4%
· 100% =
4%
· для потенциометрического титрования
Δ (фенибут) = |0,253 г - 0,25 г| = 0,003 г
δ (фенибут) = ![]() · 100% = 1,2%
· 100% = 1,2%
Заключение
В ходе данной работы были освоены методы потенциометрического титрования и прямой потенциометрии, был проведен анализ лекарственного препарата - фенибута.
На нейтрализацию 100 мл раствора 1 таблетки, содержащей по данным фармацевтической компании 0,25 г активного вещества, был затрачено 7,775 мл 0,0909 М раствора щелочи. По экспериментальным данным были построены интегральная, дифференциальная кривые титрования, а также кривая титрования Грана. Были построены прямые потенциометрии.
По графикам были определены точки эквивалентности и на основании полученных данных рассчитано содержание активного вещества в 1 таблетке.
Полученные результаты:
Потенциометрическое титрование:
m = 0,253±0,003 г
Относительная погрешность δ = 1,2%
Прямая потенциометрия:
m = 0,26±0,01 г
Относительная погрешность δ = 4%
раствор
хлороводородный фенибут кислота
Литература
1. Большая советская энциклопедия: в 30 т. - М. : Советская энциклопедия, 1969-1978
2. Евстратова, К.И. Физическая и коллоидная химия: Учеб. для фарм. вузов и факультетов/К.И.Евстратова, Н.А, Купина, Е.Е. Малахова; под ред. К. И. Евстратовой. М. : Высш. шк., 1990. 487 с.
. Конспект лекций по аналитической химии. Количественный анализ: Учеб. пособие для студ. вузов /В.В. Болотов, Е.Н. Свечникова, Т.А. Костина и др.; под ред. В.В. Болотова. Харьков : Изд-во НФаУ; Оригинал, 2005. 200 с.
. Лопатин, Б.А. Теоретические основы электрохимических методов анализа. Учеб. пособие для ун-тов. М. : Высш. школа, 1975. 295 с.
. Физическая химия [Электронный ресурс]: учебное пособие / В.И. Грызунов, И.Р. Кузеев, Е.В. Пояркова и др. М. : ФЛИНТА, 2014. 251 с.