Материал: ОТВЕТЫ НИКИТИНА







![]()




10.Сравнительная оценка алкилирования бензола на катализаторах
AlCl3 Хлорид алюминия поступает на реакцию в виде жидкого каталитического комплекса, который готовят в аппарате с мешалкой при небольшом нагревании из технического AICI3, диэтилбензола или примерно равных количеств бензола и диалкилбензола (только из бензола комплекс не получается) с небольшой добавкой хлорпроизводного (например, C2H5Cl) или иногда воды. При наличии на предприятии безводного HCI его тоже можно использовать для получения комплекса.
В последнее время рекомендовано готовить комплекс централизованно— из отходов металлического алюминия, ароматических углеводородов и безводного НCl.
H2SO4 . Возможно побочное алкилирование в ароматическое ядро. применяют 86÷90% H2SO4 при 20÷50ºС. Процесс проводят при 5÷12 атм., мольном соотношении бензола к пропилену 5:1 и объёмном соотношении H2SO4 и углеводородной фазы 1:1. Этот способ алкилирование уступил место AlCl3.
Безводный HF .Из-за высокой токсичности и коррозионной активности на практике используется мало.
Фосфорная кислота – проводят при 200-300 ºС, 2-6 Мпа. Процесс в газовой фазе (гетерогенный). Используют в виде твёрдого катализатора, который готовят пропитывая ею кизельгур. нашла применение для производства ИПБ и от части ЭБ
Алюмосиликатный катализатор – активен в отношении алкилирования бензола олефинами при 350÷400ºС в газовой фазе и при 200÷310ºС жидкой фазе. В обоих случаях реакцию осуществляют при 20÷60 атм. и значительном избытке бензола.
11.Производство этил бензола и изопропилбензола.(схему).Слайды как допол-е
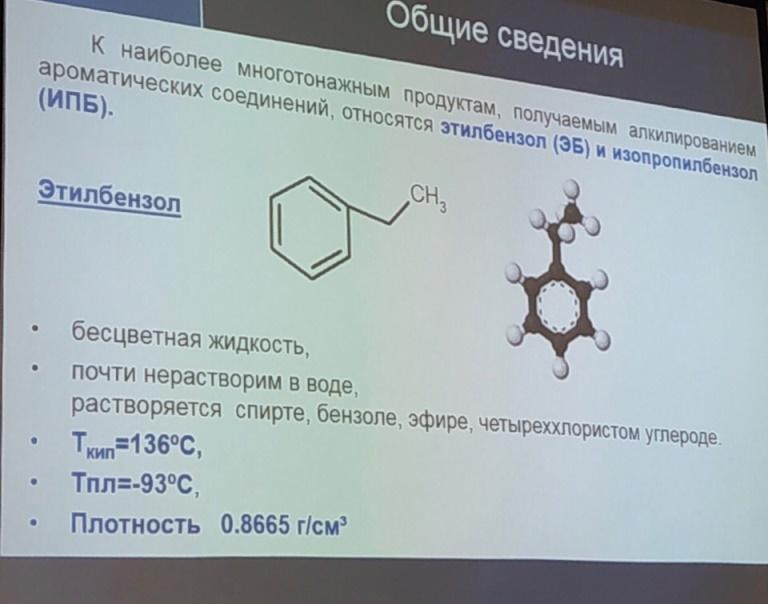
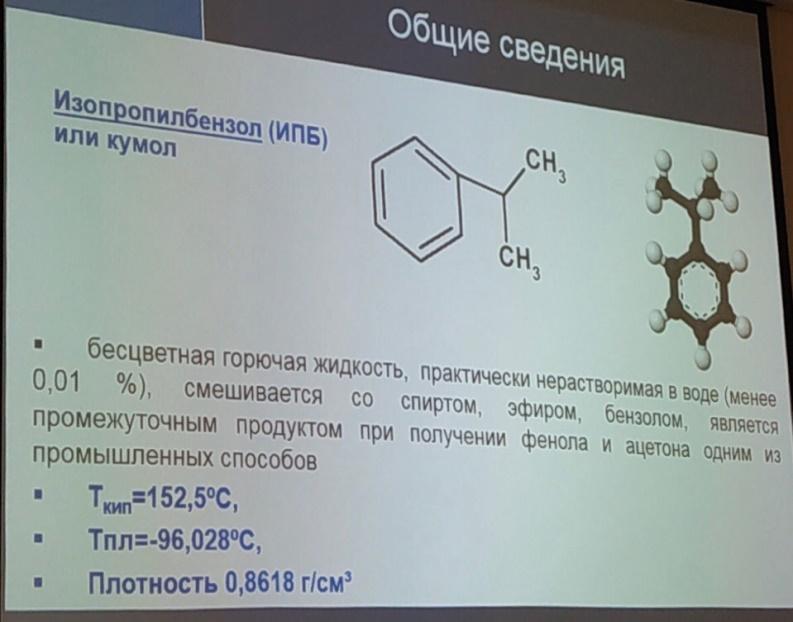
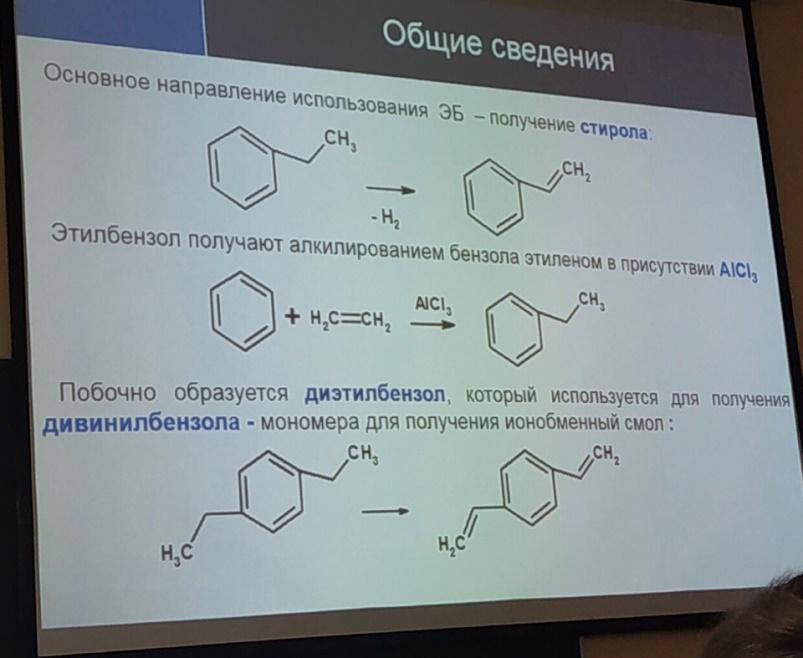
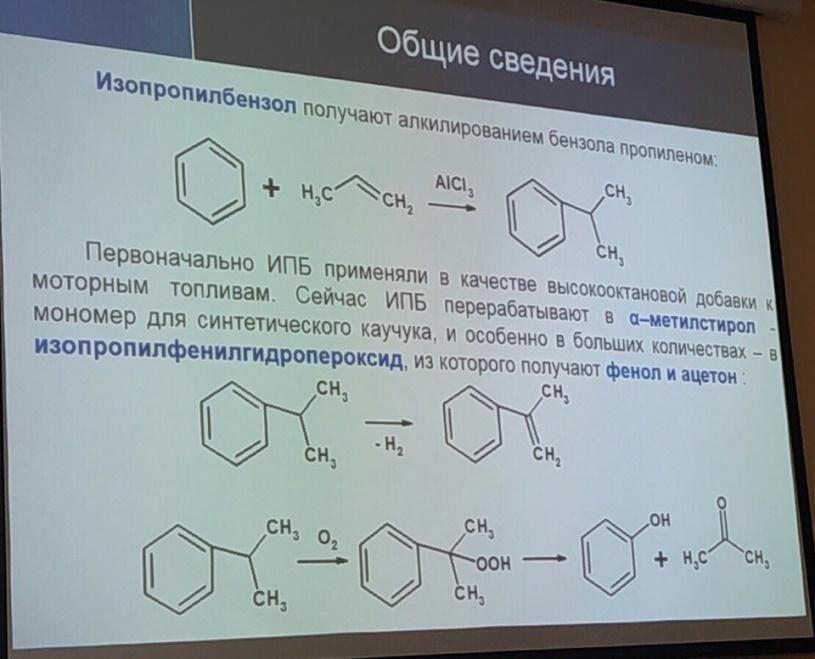
12.Зеленая химия.
Зеленая химия - новый подход к сокращению или полному отказу от использования опасных и токсичных химических веществ.
Цель– отбор исходных материалов и схем процессов, которые вообще исключает использование вредных веществ на самых начальных стадиях планирования и осуществления химических процессов.
пути синтеза.
1.использование катализатора, который снижает энергетический барьер реакции. 2. использование локальных источников энергии для активации молекул позволяющих снизить затраты энергии.
3.использование биомассы вместо нефти
выделяют 4 основных Принципа «зеленой химии».
1 лучше предотвратить образование загрязнений, чем потом от них избавляться.
2. эффективность химических реакций .Синтез веществ следует планировать так, чтобы максимальное количество исходных материалов вошло в конечный продукт, а число отходов уменьшилось.
3. энергия. Стремиться минимизировать энергетические затраты, (химические процессы следует проводить по возможности при низких температурах и давлениях.) Подбор подходящих катализаторов.
4. безопасность химических производств. Вещества и процессы следует выбирать так, чтобы несчастных случаев –стало меньше.
Сверхкритическим флюидом (СКФ) называют состояние вещества, при котором исчезает различие между фазами. Любое вещество, находящееся при температуре и давлении выше критической точки, является сверхкритической жидкостью. В критической точке две фазы, жидкая и газовая, становятся неразличимы.
Вещества в ск состоянии могут применяться в качестве заменителей органических растворителей (сверхкритическая вода и сверхкритический диоксид углерода)
Одно из наиболее важных свойств сверхкритического состояния — это способность к растворению веществ. Изменяя температуру или давление флюида, можно менять его свойства в широком диапазоне Так, можно получить флюид, по свойствам близкий либо к жидкости, либо к газу.
Сверхкритическая область начинается в критической точке , которая характеризуется непременно двумя параметрами — температурой и давлением. Понижение либо температуры, либо давления ниже критического выводит вещество из сверхкритического состояния.
В критической точке плотность жидкости и её насыщенного пара становятся равны, а поверхностное натяжение ( термодинамическая характеристика поверхности раздела двух фаз) жидкости падает до нуля, поэтому исчезает граница раздела фаз жидкость-пар.
14.Применение ионных жидкостей .
«Ионные жидкости» -вещества, которые являются жидкостями при температуре ниже 100 °С и состоят из органических катионов и разнообразных анионов (например, 1,3-диалкилимидазолия)
Ионные жидкости относятся к так называемым «зелёным растворителям», которые соответствуют принципам зелёной химии.
Ионные жидкости в твёрдом состоянии представляют собой порошки либо воскообразные субстанции белого, либо желтоватого цвета. В жидком состоянии бесцветны, либо с желтоватым оттенком, который обусловлен небольшим количеством примесей.
Перспективно использование ионных жидкостей в качестве катализаторов и реакционных сред в синтезе органических, металлорганических и высокомолекулярных соединений; электролитов в электрохимическом синтезе, химических источниках тока и процессах электроосаждения металлов и сплавов; эффективных и экологически чистых растворителей.
Из-за их высокой стоимости ионные жидкости вряд ли найдут широкое применение в многотоннажных процессах
Ионные жидкости состоят из объемных органических катионов и органических или неорганических анионов. Несимметричность строения, а также пространственная изолированность зарядов препятствует организации кристаллической структуры и обусловливает ионный характер жидкой фазы.
СВОЙСТВА ИОННЫХ ЖИДКОСТЕЙ
1)широкий интервал жидкого состояния (>300 °C) и низкая температура плавления(Тпл<100 °C);
2)высокая удельная электропроводность;
3)хорошая растворяющая способность по отношению к разнообразным органическим, неорганическим, металлоорганическим соединениям и полимерам природного и синтетического происхождения;
4)нелетучесть, возможность многократного использования;
5)негорючесть, невзрывоопасность, нетоксичность;
6)каталитическая активность, обуславливающая повышение селективности органических реакций и выхода целевого продукта;
7)безграничные возможности в направленном синтезе ионных жидкостей с заданными свойствами.
ПРИМЕНЕНИЕ иж
Наиболее значимые перспективные ионные жидкости как каталитические среды в катализе и органическом синтезе:
алкилирование и ацетилирование; олигомеризация и димеризация олефинов; реакции образования С–С-связей; карбонилирование и гидроформилирование; гидрирование; галогенирование; окисление органических соединений; изомеризация различных ув.
Ионные жидкости в синтезе полимеров:
Одним из свойств ИЖ является способность пластифицировать различные полимеры, что позволяет получать композиционные материалы с улучшенными физ. и мех. характеристиками.
По физическим характеристикам полимеры, пластифицированные ИЖ, сопоставимы с полимерами, пластифицированными традиционными пластификаторами (например, диоктифталатом) , но являются более термически стабильными.
Кроме того, ИЖ снижают горючесть полимеров, что позволяет применять их в качестве огнезащитного состава
Применение ИЖ в алкилировании:
ИЖ используется в качестве катализатора алкилирования для получения высокооктановых моторных топлив в качестве альтернативы традиционным фтористоводородной или серной кислотам.
Этот жидкий катализатор имеет малое давление насыщенных паров и может регенерироваться непосредственно на объекте, а значит, оказывает меньшее воздействие на окружающую среду, чем кислоты.
15.Ресурсоэнергосберегающие и энергосберегающие технологии в нп и нх.
в качестве приоритетных направлений в области энерго- и ресурсосбережения выделены следующие: 1) утилизация попутного нефтяного газа, в настоящее время сжигаемого в факелах 912 млрд. м3 в год; способы утилизации ПНГ: А)
-
Фракционный способ. заключается в разделении ПНГ на непосредственно сухие газы и ШФЛУ.
-
· Закачка ПНГ обратно в пласт. Это делают с целью увеличения нефтеотдачи месторождения. проблема не решается , тк происходит лишь простая перекачка.
· 2. Установка энергоблоков. позволяет использовать в качестве источника электричества и тепла для электростанций энергию попутного нефтяного газа, вырабатывающуюся за счет его сжигания в газотурбинных установках.
· 3.Мембранный способ. На выходе имеются сухой отбензиненный газ и ШФЛУ, которые можно отправить на дальнейшую переработку.
4. Переработка в сжиженный газ. Сжижение подготовленного ПНГ происходит через его взаимодействие с азотом в искусственно созданных условиях.
Б) Выбор энергоэффективного технологического режима с точки зрения минимизации энергетических затрат при заданном качестве выпускаемой продукции и экологической безопасности:
В) Замена устаревших контактных устройств на более эффективные
Г) Модернизация или замена вспомогательного оборудования на тепломассообменных установках для обеспечения высокой степени энергоэффективной очистки теплоносителей, технологических потоков, газовых и жидких выбросов.
-
16.Технологии переработки полимерных отходов (еще сократить) не все способы писать
Основные виды полимерных отходов:
из полиэтилена – 34% ПЭТ (Полиэтилентерефталат) – 20%
Основные способы переработки полимерных отходов:
1) Механический способ (рециклинг) Суть метода состоит в механическом дроблении отходов с целью их дальнейшего повторного термического формования.
7) Метод гидролиза заключается в расщеплении отходов полимерных материалов водно-кислотными растворами под воздействием высокой температуры.
9) Метанолиз Способ подразумевает расщепление отходов пластика метанолом. Процесс протекает в реакторе под давлением в условиях высоких температур.
10) Пиролиз метод термической деструкции полимерных отходов при отсутствии доступа воздуха. В результате данного процесса сырьевой материал разлагается на мономеры
11) Переработанные отходы полимеров широко используются в производстве строительных материалов.
12) Применение отходов полимерных материалов в качестве вторичного сырья помогает не только уменьшить объемы складируемого мусора на полигонах, но и значительно сократить количество потребляемой электроэнергии и продуктов нефтяного производства, применяемых для изготовления полимерной продукции.
17. Проблемы экологичности нефтеперерабатывающих предприятий.
Выбросы и загрязнения. Предприятия нефтеперерабатывающей и нефтехимической промышленности оказывают негативное влияние на состояние окружающей среды, что обусловлено их деятельностью и сжиганием продуктов переработки нефти.
В состав продуктов сгорания топлива входят: * углеводородные соединения; оксид азота; * оксид серы; * сероводород; * оксид углерода; * технический углерод.
Основной экологической проблемой в нашей стране является низкий уровень утилизации ПНГ !!!(попутного нефтяного газа).
К мероприятиям по снижению выбросов вредных веществ относят:
*совершенствование технологических процессов и внедрение малоотходных и безотходных технологий;
*комплексное использование сырья
*изменение состава и улучшение качества выпускаемой продукции.
*очистку сбрасываемых промышленных газов.
Загрязнение почвы. Происходит в результате нефтяных и нефтепродуктовых разливов, происходящих при порывах трубопроводов и утечках,в процессе открытого фонтанирования природного сырья.
Загрязнение воды. Загрязнение воды происходит при переработки нефти и газа для получения синтетических продуктов, в процессах обессоливания и обезвоживания итд. Также в результате бурения образуются загрязненные буровые воды. Они очень опасны для окруж сред.
Алкилирование – введение алкильных групп в молекулы органических и некоторых неорганических соединений. Эти реакции имеют большое практическое значение для синтеза: этилбензола (ЭБ) и изопропилбензола (ИПБ). Немаловажное значение имеют алкилароматические пластификаторы, смазочные масла и присадки, получаемые алкилированием ароматических углеводородов.
Исходные вещества:
Технический бензол или другой ароматический углеводород, фракции низших олефинов. Хлорид алюминия в виде жидкого каталитического комплекса.
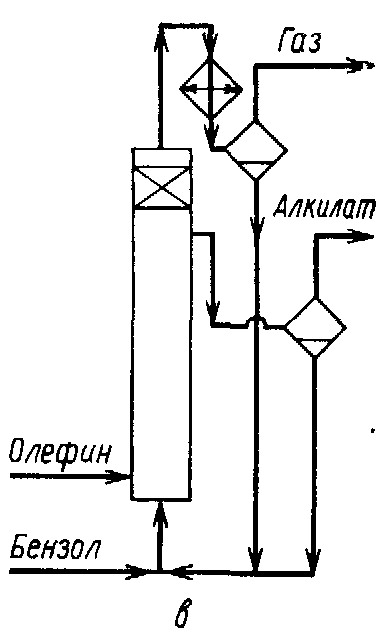
Алкилирование ароматических углеводоро-дов газообразными опефинами проводят в барботажных колоннах, внутренняя поверхность которых защищена от коррозии кислотостойкими плитками.
В нижнюю часть колонны подают сухой бензол и олефиновую фракцию, которая барботирует через жидкость, интенсивно ее перемешивая. Жидкая реакционная масса стекает через боковой перелив в сепаратор, где отстаивается более тяжелый каталитический комплекс, возвращаемый в низ алкилатора, а алкилат поступает на дальнейшую переработку
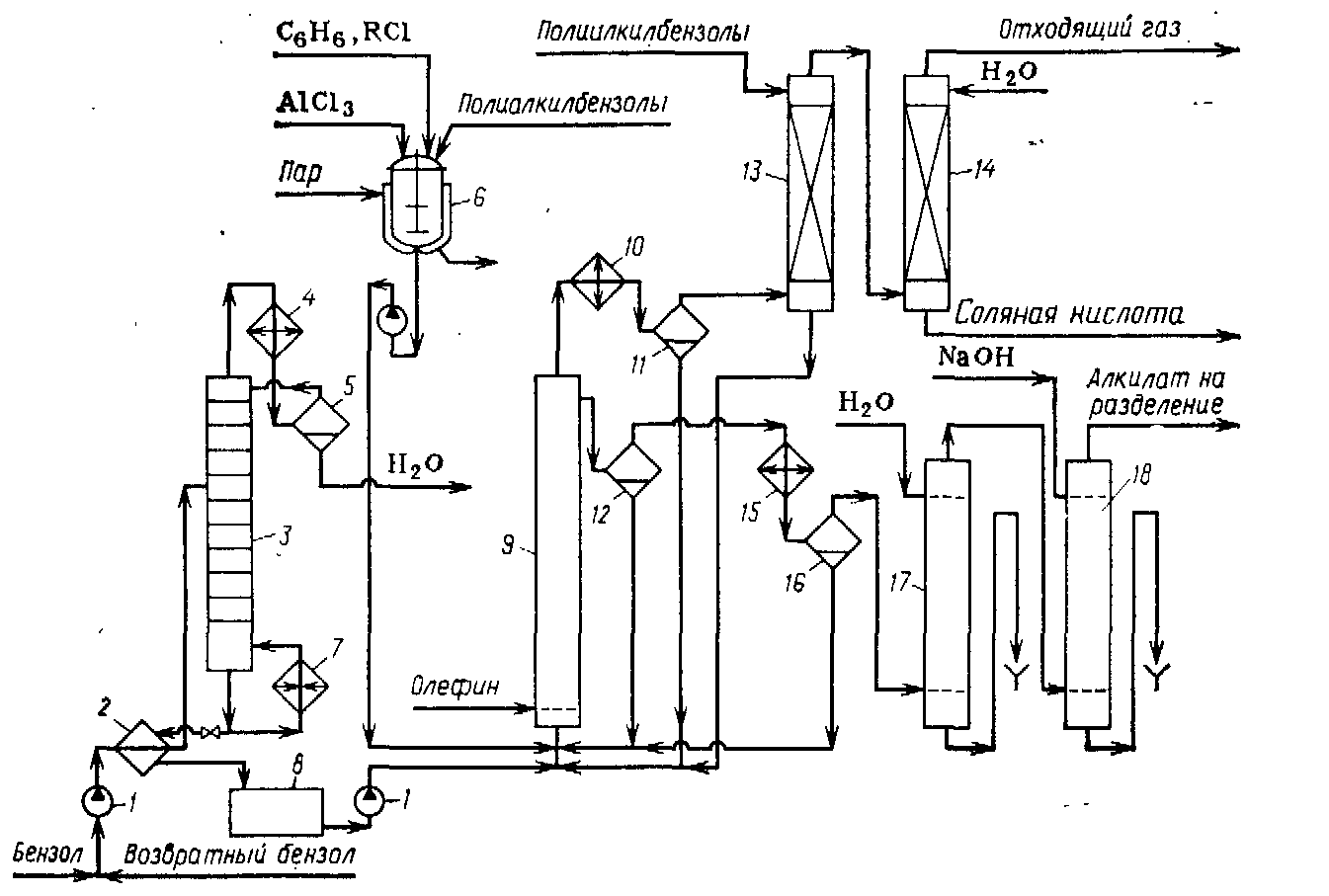
Свежий бензол вместе с бензолом, возвращенным со стадии разделения, поступает в колонну 3, предназначенную для осушки бензола азеотропной ректификацией. Низкокипящая азеотропная смесь бензола с водой конденсируется в конденсаторе 4 и разделяется в сепараторе 5 на два слоя. Воду с растворенным в ней бензолом отводят, а бензольный слой стекает на верхнюю тарелку колонны 3, создавая орошение. Осушенный бензол из куба колонны 3 в теплообменнике 2 подогревает бензол, идущий на осушку, и попадает в сборник 8, откуда насосом непрерывно закачивается в алкилатор 9.
Каталитический комплекс готовят в аппарате с мешалкой и рубашкой для обогрева паром. Приготовленный комплекс периодически вводят в алкилатор. Реакция проводится в непрерывно действующей колонне-алкилаторе 9 с горячим сепаратором 12 для отделения каталитического комплекса и обратным конденсатором 10 для возвращения испарившегося бензола и отвода тепла. Олефин поступает в низ колонны, предварительно проходя расходомер. Бензол из емкости 8 поступает в низ алкилатора, как и конденсат из конденсатора 10.
Газы, отходящие после конденсатора 10, содержат значительное количество легколетучего бензола. Для улавливания бензола эти газы направляют в абсорбер 13, который орошается полиалкилбензолами. Собирающийся в нижней части абсорбера раствор поступает в реакционный аппарат 9 для переалкилирования. Газы после абсорбера 13 промывают водой в скруббере 14 для удаления HCl и выводят. Углеводородный слой, отбираемый после сепаратора 12, проходит водяной холодильник 15 и дополнительно отстаивается в холодном сепараторе 16, откуда каталитический комплекс периодически возвращают в алкилатор. Алкилат направляют после этого на очистку. С этой целью смесь промывают в системе противоточных колонн 17 и 18 вначале водой, а затем водной щелочью. Нейтрализованная смесь углеводородов (алкилат) поступает на ректификацию