Материал: Отримання формальдегіду методом окислювального дегідрування метанолу
Тому що абсорбція йде з виділенням тепла, а температура газів, що відходять із абсорбера (викидів) не повинна перевищувати 30 С°, рідина на тарілках абсорбера прохолоджується за допомогою виносних холодильників по трьох контурах.
У процесі абсорбції стандартний формалін, що утвориться, з куба колони крізь холодильник направляється на склад.
Не поглинений газ із верхньої частини колони направляється на
природоохоронний комплекс і далі на утилізацію [4].
1.2 Теоретичні основи процесу
1.2.1 Механізм, хімізм, кінетіка та термодінамікка процесів окислювального дегідрування
Під дегідруванням розуміють хімічні процеси, пов'язані із
відщепленням атомів водню від органічної сполуки, зокрема від спиртів [1]:

Наведені вище перетворення можна проводити за допомогою
реакцій окиснення:
![]()
У зв'язку із цим широке поширення одержали процеси окисного
дегідрування, коли відщеплення водню здійснюється у присутності молекулярного
кисню й кінцеві речовини утворюються як наслідок розвитку процесів окиснення,
так і дегідрування:
![]()
Ці реакції займають проміжне положення між окисненням і дегідруванням і іноді настільки близько примикають до окиснення, що важко стає провести точну межу між окисненням і окисним дегідруванням [1].
Механізм утворення формальдегіду основан на паралельно- послідовних реакціях, тобто частина продуктів утворюється по первинним хімічним реакціям, а друга частина - по наступним хімічним реакціям за участю продуктів, отриманих у первинних реакціях [2].
Найбільш вірогідним механіхм утворення формальдегіда це окислювально-дегідрогєнізійний. Механізм утворення формальдегіда протікаєчерез адсорбцію кисня на каталізаторі із наступною десорбцією його, при хімічній реакції окиснення метанолу у формальдегід, поміжні продукти реакції - воду та діоксид вуглецю із виділенням молекулярного металлу каталізатора (срібла). Молекулярний каталізатор далі знову адсорбує кисень і знову вступає у реакцію[2].
При заглибленному вивченні хімізма реакцій, протікаючих на каталізаторі по окислювально-дегідрруючому механізму утворення формальдегіду із метанолу, за проведення реакціїокиснення відповідальність несе кисень, адсорбований на срібло у формі Ag(O-)адс., за реакцію дегідрування - зв' язаний атомарний двухзарядний Ag(O2-)адс., а слабо зв' я-заний молекулярний кисень у формі Ag(O-2)адс., забезпечує реакції глубокого окиснення метанолу до СО2 і Н2О (1.5).
Швидкість процессу окислювального дегідрування метанолу у формальдегід при прийнятих виробничих температурних режимах лімітується підводом реагентів до поверхні каталізатора, що вказує на протікання процессу у зовнішньодифузійній області. Швидкість процесу описується рівнянням першого порядку по концентрації кисня. Температурний коефіцієнт швидкості реакції відповідає температурному коефіцієнту дифузії кисня[3].
Окиснення метанолу на окисних каталізаторх протікає по
окислювально-відновлювальному механізму, наприклад [3]:
СН3ОН+ 2МоО3→ СН2О + Н2О + МоО5 (1.17)
2МоО3 + 0,5О2 → 2МоО 3 (1.18)
або
СН3ОН+0,5О2→ СН2О
+ Н2О+ 147,4кДж (1.20)
Лімітуюча стадія як основної, так і побочної реакції- взаємодія метанолу із поверхневим киснем, тобто основний хімічний акт. Утворюющаяся вода оказує гальмуючу дію на обидві реакції. Крім того, метанол гальмує окиснення формальдегіда до окису вуглецю і води.
Окисні каталізатори менш чутливі до домішок, ніж срібляний і його аналоги.
Вираз для швидкості реакції (1.4) та (1.5)-(1.7) при постій
ній температурі мають вигляд[3]:
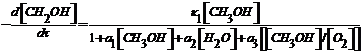 (1.21)
(1.21)
та
![]() ,
(1.22)
,
(1.22)
Де ![]() та
та![]() - константи швидкості лімітуючої стадії,1, a2, a3,b1,
b2, b3 - кінетичні коеффіцієнти.
- константи швидкості лімітуючої стадії,1, a2, a3,b1,
b2, b3 - кінетичні коеффіцієнти.
Рівняння Аррєніуса для ![]() та
та
![]() у мл/(м2с) та зерен каталізатора
визначеного розміру запропоновані у формі [3]:
у мл/(м2с) та зерен каталізатора
визначеного розміру запропоновані у формі [3]:
1=2,33*108exp(-18500/RT)
(1.23)2=2,05 exp(-3600/RT) (1.24)
Для підтримки активності каталізатора реакцію необхідно проводити у надлишку кисня, оскільки у протилежному випадку під дією метанолу і формальдегіду каталізатор швидко руйнується. Із цього, з урахуванням меж взриву реакційних сумішей, випливає важливіша відмінність отримання формальдегіду на окисних контактах: реакцію проводять при співвідношенні реагентів і повітря нижче нижньої межі взриву, тобто при складі метанолу в вихідній суміші не більше 7-8%. Із порівняння рівнянь k1 та k2 бачимо, що енергії активації головної реакції більш ніж у п'ять разів перевищує той же показник побочної реакції і, тому, вихід формальдегіду повинен збільшуватись при підвищенні температури. Але було доведено, що при температурі вище 400 0С каталізатор втрачає активність. Крім того, при перевищенні цієї межі, з'являються значні втрати формальдегіда через термічний розпад. З урахуванням ціх співвідношень, робоча температура процесу підтримується на рівні 350-390 0С [3].
Процеси окисного дегідрування мають тепловий ефект, що залежить від частки реакцій окиснення й властно дегідрування. Оскільки окиснення завжди протікає з виділенням тепла, введенням тих або інших кількостей кисню можна широко вар’їрувати тепловий ефект сумарної реакції. Це є одним з переваг окисного дегідрування - усуваються эндотермічність процесу й необхідність у постійному підігріві реакційної системи [3].
Дуже важливою особливістю реакцій дегідрування є їхня оборотність.
Очевидно, що для ендотермічних реакцій дегідрування підвищення температури буде
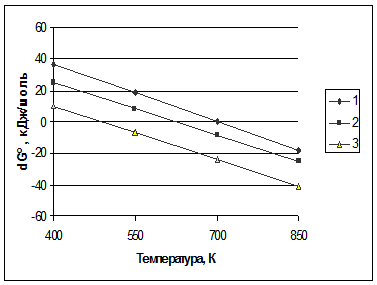
сприяти зсуву рівноваги вправо. Температурні залежності вільної енергії
дегідратації спиртів зображені на мал. 1 [1]. Близькі до нуля або негативні
значення ДG° указують на можливість практичного здійснення й на зсув рівноваги
у відповідності рівнянням:
![]()
Як видно з (мал. 1), рівновага більше зміщена вправо у вторинних спиртів (при утворенні кетонів), а менше - для первинних спиртів (особливо для метанолу), що дають при дегідруванні альдегіди.
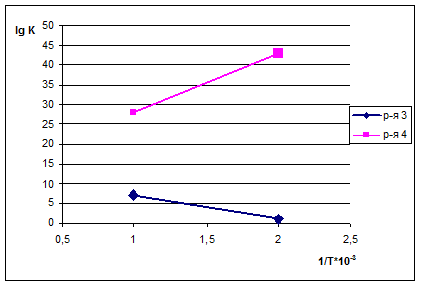
Як видно з (мал. 2), рівновага реакції дегідрування (1.3) і окислювання (1.4) істотно зрушена у бік утворення продуктів реакції [3]. Значення констант рівноваги для реакцій окисного дегідрування значно вище, ніж для простого дегідрування. Це означає, що реакція (1.4) може розвиватися до практично повного вичерпування реагенту, узятого в недоліку, у цьому випадку кисню, невитрачений метанол може піддаватися лише простому дегідруванню або побічним перетворенням.
При дегідруванні через відщіплення водню завжди відбувається
збільшення обсягу газів, і, отже, підвищенню ступеня конверсії сприяє низький
тиск, тому ці процеси здійснюють при атмосферному тиску, а в деяких випадках
під вакуумом, або, розбавляючи реакційну масу газом або парою, що веде до
зниження парціальних тисків реагентів і росту рівноважного ступеня конверсії.
Зниження парціального тиску реагентів дозволяє також знизити температуру
процесу й тим самим зменшити утворення побічних продуктів.


Застосування каталізаторів дозволяє досягти високої швидкості процесів при порівнянно низькій температурі, коли ще не одержують значного розвитку побічні реакції.
Каталізатори реакцій дегідрування й гідрування [1] можна розділити на наступні групи:
1. метали VIII групи (Fe, Co, Ni, Pd, Pt) і I групи (Cu, Ag);
2. окисли деяких металів (MgO, Cr2O3, Fe2O3, ZnO, MoO3, WO3 і ін.);
. сульфіди кобальту,нікелю,
. молібдену й вольфраму;
. складні каталізатори, що складаються із двох і більше металів (Ni + Cu), з окислів різних металів (особливо хроміти ZnO·Cr2O3 и CuО·Cr2O3) або сульфідів (NiS∙WS3; CoS∙MoS3 и др.)
Всі вони є або провідниками струму (метали) або
напівпровідниками, здатні каталізувати реакції, пов'язані з електронними
переходами. Вони дезактивуються контактними отрутами, до яких належать
галогени, сірчисті з'єднання, деякі метали, що спричиняється необхідність
очищення сировини від цих з'єднань. Сульфіди металів, окисли молібдену й
вольфраму стійкі проти дії каталітичних отрут (активність окисів навіть
підвищується в присутності сірки) [1].
.2.2 Селективність процесу окислювального дегідрування
Для дегідрування, завжди здійснюваного при високій температурі, щоб уникнути небажаних побічних реакцій використовують [1] менш активні каталізатори - мідь, срібло, окисли цинку, хрому, заліза й ін.
Дезактивація каталізатора у процесі роботи може бути обумовлена не тільки домішками в сировину, але й розвитком побічних реакцій, що викликають відкладення на його поверхні смолистих речовин і коксу. Регенерацію каталізатора проводять у реакторі або в спеціальному регенераторі окислюванням відкладень повітрям або водяною парою.
При температурах, характерних для виробництва, швидкість перетворення метанолу у формальдегід лімітується підведенням реагентів до поверхні зерен каталізатора, тобто процес протікає у зовнішньодифузійній області [3].
З переходом у зовнішньодифузійну область різко зростає активність і селективність каталізатора, що призводить до значного підвищення продуктивності каталізатора (на 1,5 - 2 порядки). При наявності внутрідифузійного гальмування в тонких порах відбувається неповне згоряння метанолу й формальдегіду до диоксида вуглецю й води.
З підвищенням температури конверсія метанолу монотонно зростає селективність формальдегіду, що утвориться, практично постійна при збільшенні температури від 400 до °700 С, а з подальшим ростом різко знижується [3].
Селективність процесів дегідрування залежить від розвитку послідовних і паралельних реакцій, зв'язаних високою температурою проведення процесу. Наприклад, відбувається крекінг сировини, гидрогеноліз під дією водню, що утвориться, а також реакції полімеризації, циклізації й дегідроконденсації, ведучі, в остаточному підсумку, до виділення смолистих речовин і коксу, дезактивуючих каталізатор.
На тому самому каталізаторі селективність процесу залежить від ряду факторів, у тому числі від відносної реакційної здатності органічних речовин або окремих функціональних груп і від їхньої здатності адсорбуватися на поверхні каталізатора. Часто обоє фактора впливають одночасно або перший з них превалює над другим[3].
Незалежно від вибору каталізатора й інших умов на
селективність дегідрування сильно впливає температура. Звичайно чим нижче
температура, тим селективніше можна провести процес по більше реакційно здатних
групах або зупинити його на певній проміжній стадії. Навпаки, підвищення
температури сприяє глибоким перетворенням. Істотно, що небажані побічні реакції
гидрогеноліза, крекінгу, дегідроконденсації й інші мають більше високу енергію
активації, чим дегідрування. Оскільки при зменшенні температури одночасно
зменшуються швидкість процесу й продуктивність реактора, те практично в кожному
випадку можна знайти область оптимальних температур, що відповідає мінімуму
економічних витрат. Додаткові обмеження на вибір цього оптимуму накладає
оборотність реакції дегідрування. Нарешті, за інших рівних умов оборотність
залежить від часу контакту, що визначає фактичний ступінь конверсії вихідної
речовини. Чим ближче вона до рівноважного, тим значніше розвиток послідовних
реакцій крекінгу або конденсації, що ведуть до зниження селективності. При
дегідруванні ступінь конверсії становить іноді 20 - 40 %, а час контакту
перебуває в межах від часток секунди до декількох секунд [3].
.2.3 Вибір методу виробництва формаліну
При співставленні двох методів окислювального дегідрування метанолу - на металевих (срібляних) та окисних (залізомолібденових) каталізаторахможна виділити наступні переваги та недоліки :
на срібляному каталізаторі головною перевагою є висока продуктивність, низька металлоємкість, простота конструкції реактора і що дуже важливо для данного проекту, немає меж по потужності одиничної установки. Але є і недоліки: високий витратний коефіцієнт по сировині, домішкі у продукті, витрата драгоційного металлу;
на окисних каталізаторах перевагою є низький витратний коефіцієнт по сировині та та практично чистий готовий формалін, але низька продуктивність(8-10 тис. т/р), підвищена витрата енергії та повітря, підвищенна металлоємкість та межі по одиниці потужності установки.
Виходячи із цього у данному проекті розрбляєть схема
отримання формальдегіду на срібляному каталізаторі[3].
2. ТЕХНОЛОГІЧНА ЧАСТИНА
.1 Фізико-хімічна характеристика вихідної сировини, матеріалів і продуктів
Таблиця 2.1 - Фізико-хімічна характеристика вихідної сировини
й матеріалів
Найменування речовини
Молекулярна формула
Молярна маса, г/моль
Характеристика деяких фізичних властивостей
Стандарт
1. Метанол технічний
СН3ОН
32
Щільність при 20 °С с = 0,791ч0,792
ДСТУ 3057 - 95
2. Конденсат паровий
Н2О
18
Зміст NH3 1 мг/дм3,
хлорид-іонів 2 мг/л, рН = 7,9ч9,2
СТП 6 - 52 - 96 з изм. № 1
3. Пара
Н2О
18
Тиск Ризб = 0,55 МПа
-
4. Вода зворотнього циклу
Н2О
18
Тиск не менш 0,25 МПа температура не менш 28 °С
-
5. Азот газоподібний технологічний
N2
28
Тиск не менш 0,3 МПа частка кисню не більше 3 %
-
6. Повітря технологічне
-
29
Тиск 0,3ч0,5 МПа
-
7. Повітря СТОСІВ
-
29
Тиск 0,29ч0,31 МПа
СТП 3 - 161 - 2002
8. Розсіл
-
-
Тиск не більше 1,4 МПа, температура -10 ч -18 °С
-
9. Надсмольна вода
-
-
Масова частка СН2Про не більше 12 %,
сухого залишку не більше 0,03, рН не менш 7
-
10. Масло індустріальне 40А
-
-
-
ДЕРЖСТАНДАРТ 20799 - 88
Таблиця 1.2 - Фізико-хімічна характеристика продукту
Фізико-хімічна характеристика
Значення параметра
1. Марка
ФМ (стабілізований метанолом)
2. Зовнішній вигляд
Безбарвна прозора рідина, при зберіганні
допускається утворення каламуті або білого осаду, розчинного при температурі
вище 40 °С (ДЕРЖСТАНДАРТ 1625 - 89)
3. Масова частка формальдегіду, %
ВР 37,2 ± 0,3 ПС 37,0 ± 0,5
4. Масова частка метанолу, %
ВР 4 ± 8 ПС 4 ± 8
5. Масова частка кислот у перерахуванні на мурашину,
не більше %
ВР 0,02 ПС 0,04
6. Масова частка заліза, не більше %
ВР 0,0001 ПС 0,0005
7. Масова частка залишку після прожарювання, не
більше %
ВР 0,008 ПС 0,008
.2 Опис технологичного процессу та розробка технологічної
схеми
.2.1 Розробка технологічної схеми
Метанол з лінії нагнітання насосів беззупинно подається по
трубопроводу в спиртовипарювач СП з об'ємною витратою не більше 2200 л/г. У
трубопровід подачі метанолу подається конденсат паровиї з об'ємною витратою не
більше 1200 л/г. Масова частка метанолу у метанольно-водній суміші, що
надходить у спиртовипарювач, підтримується автоматично в межах від 60 до 80 % і
регулюється подачею конденсату в спиртовипарювач.
Спиртовипарювач являє собою вертикальний циліндричний апарат
з камерою, що гріє, краплеотбійником і барботером [19].
Температура рідкої фази в спиртовипарювачі підтримується в
межах від 72 до 82 °С шляхом безперервної подачі циркуляційного конденсату в
камеру, що гріє, спиртовипарювач й залежить від температури циркуляційного
конденсату, що повинна бути від 74 до °95 С.
Циркуляційний конденсат, безупинно циркулюючи за схемою:
теплообмінник спиртовипарювача - насос циркуляційного конденсату Н1 -
підконтактний холодильник - теплообмінник циркуляційного конденсату АТ6 -
теплообмінник спиртовипарювача, здійснює охолодження реакційних газів і
нагріває рідку фазу в спиртовипарювачі до заданих температур.
Температура циркуляційного конденсату регулюється шляхом
зміни кількості конденсату, що подається в теплообмінник і в байпас
теплообмінника циркуляційного конденсату. Тому що кількість теплоти, що
віддається реакційними газами, більше необхідного для підтримки робочого
значення температури рідкої фази в спиртовипарювачі, то надлишок тепла
знижується оборотною водою, що подається в теплообмінник циркуляційного
конденсату [19].
Повітря з напірного колектора надходить у спиртовипарювач СП.
Тиск повітря в напірному колекторі підтримується не більше 0,063 МПа. Об'ємна
витрата повітря в спиртовипарювачі підтримується в межах від 1400 до 2000 м3/г.
Барботируючи у спиртовипарювачі через метанольно-водну суміш, повітря
насичується парами метанолу й води. Отримана парогазова суміш надходить у
перегрівач АТ1, де нагрівається пором для попередження конденсації з її рідини
до температури не менш 100°С [19].
Після перегрівача парогазова суміш крізь вогнеприпинувач ОП,
призначений для запобігання проскакування полум'я з контактного апарата у
спиртовипарювач при аварійній ситуації, надходить у контактний апарат РТ.
Контактний апарат являє собою вертикальний циліндричний
апарат, змонтований на підконтактному холодильнику. На трубну дошку
подконтактного холодильника укладається мідна (або нержавіюча) сітка, потім
мідні перфоровані ґрати й мідна (або нержавіюча) сітка. На сітку засипається
каталізатор. Висота шару каталізатора 76 мм, термін служби - не менш 120 доби.
На верхній шар каталізатора укладається мідна (або нержавіюча) сітка.
Температура в зоні реакції підтримується в межах від 650 до
750 °С.
На виході із зони контакту реакційні гази різко охолоджуються
в підконтактному холодильнику до температури не більше 120 °С и надходять у
нижню частину поглинальної колони КЛ [19].
Проходячи знизу нагору по колоні, гази контактують із
рідиною, що рухається протитоком. При цьому формальдегід і метанол поглинаються
рідиною, а непоглинені гази з верхньої частини колони КЛ направляються на
додаткове поглинання в скрубер АР системи вловлювання.
При поглинанні формальдегіду й метанолу водою й при їхній
конденсації виділяється велика кількість тепла. Для відводу тепла передбачені
примусова циркуляція й охолодження формаліну у виносних холодильниках з
наступною його подачею в колону.
Поглинальна колона формаліну КЛ являє собою циліндричний
вертикальний зварений апарат з нержавіючої сталі висотою 16,850м і діаметром
1,812 м. По висоті колона має 37 ковпачкових тарілок і 3 (7, 22, 31) глухих
[19].
Примусова циркуляція формаліну по колоні здійснюється в такий
спосіб:
- формалін з кубової частини колони
поглинання формаліну надходить на всас насосів Н2. З лінії нагнітання насосів
формалін подається в холодильник АТ2, де охолоджується зворотньою водою.
Охолоджений формалін подається на 21-у тарілку, а надлишок як
готовий продукт направляється на склад.
- формалін із середньої (другий) глухої
тарілки надходить на всас насосів Н3, прокачується крізь холодильник АТ3, де
прохолоджується зворотньою водою й подається на 30-у тарілку колони.
- формалін з верхньої (третьої) глухої
тарілки надходить на всас насосів Н4, потім прокачується крізь холодильник АТ4,
де охолоджується зворотньою водою й подається на 37-ю тарілку колони [19].
Надлишок рідини з кожної глухої тарілки крізь переливні
пороги по зовнішніх переливах самопливом перетікає на нижчележащу ковпачковую
тарілку. Рідина, перетікаючи з тарілки на тарілку й насичуючись формальдегідом
і метанолом, попадає у кубову частину поглинальної колони. Рівень у кубі колони
підтримується шляхом відкачки частини формаліну на склад готової продукції.
Температура в кубі колони повинна бути від 60 до 90 °С [19].
У верхню частину колони подається охолоджена рідина системи
вловлювання або охолоджений паровий конденсат з об'ємною витратою не більше
1200 л/г залежно від концентрації формаліну у кубовій частині колони.
Перехід газу з однієї частини колони в іншу здійснюється по
зовнішніх газових трубопроводах, розташованим у глухих тарілках.
Скрубер АР являє собою вертикальний циліндричний апарат з
десятьма ковпачковими тарілками по висоті. Уловлювання метанолу й формальдегіду
з газу в скрубері здійснюється рідиною, що циркулює за схемою: збірник Е
(-холодильник АТ5 - насос Н5 - скрубер [19].
З нижньої частини скрубера АР рідина по «качці» зливається в
збірник Е. Рідина зі збірника Е подається на холодильник АТ5, де
прохолоджується оборотною водою, і далі надходить на всас насосів Н5.
З лінії нагнітання насосів рідина подається на зрошення
скрубера АР з об'ємною витратою 2 - 5 м3/г, а також на зрошення
поглинальної колони КЛ.
Гази, що відходять, з температурою не більше °40 С надходять
у циклон ВД, де відділяється краплинна волога, що втримується у газах, що
відходять.
Гази, що відходять, після циклона ВД скидаються в атмосферу
або подаються на утилізацію [19].
.2.2 Нове технологічне рішення
В наш час для отримання формальдегіда методом окислювального
дегідрування матанола використовуються каталізатори, які мають в якості
активного компонента срібло. Промислове використання отримали як нанесені
каталізатори, так і масивні каталізатори (крістали срібла, пористе срібло) [3].
Головною перевагою нанесених каталізаторів порівняно з
масивними є мала разова загрузка срібла і простота у виготовленні. Нанесені
каталізатори працюють на метанольно - водній суміші, яка складається з 60-85мас
метанола, при цьому отримують формалін концентрацієй не більше 40%.
Процес окислювального дегідрування метанолу на
сріблоскладаних каталізаторах протікає у зовнішньодифузійній області, тому
внутрішня поверхність порістого каталізатора, де обмін з потоком має
ускладнення, є причиною утворення продуктів утовщєння [4].
Спроби створення трегерних (нанесених) каталізаторів з
низьким складом срібла (нижче 10% мас) призводять до результу тільки спочатку
пробігу каталізатора. Довгий пробіг призводить к значному зниженню активності
та селективності каталізаторів, причиною чого є відкриття поверхні носія
внаслідок агретації часток срібла [4].
Існує спосіб отримання формальдегіда окислювальним
дегідруванням метанолу на каталізаторі, який складається зі срібла або золота
(склад активного компонента 0,5- 10%) на твердому непористому носії. Частки
каталізатора не мають пор і вкриті тонкою плівкою металу.
Внаслідок відсутності пор на каталізаторі знижується
утворення продуктів потовщєння, але в процесі експлуатації каталізатора тонка
плівка металу ушкоджується в результаті агрегірування активного компонента або
розтріскування носія. Загальна площа каталізатора мала, тому мінімальне її
ушкодження погано сказується на роботі каталізатора.
У данному дипломному проекті пропонується каталізатор
окислювального дегідрування метанолу у формальдегід, який має у своєму складі
срібло та алюмосилікатний носій, причому у якості носія він складається з
непористого алюмосилікату з молярним співвідношенням окису кремнію до окису
алюмінія від 1 до 10 і срібло у вигляді іона, зв’язане з алюмосилікатом у
кількості від 0,01 до 1 моль на 1 моль алюмінія, який знаходиться в
алюмосилікаті [4].
Запропонований катлізатор має наступні переваги:
висока диспестність срібла, що дозволяє використовувати
каталізатор зі зниженним його складом;
рівномірне розподілення срібла по об’єму;
стійкість часток срібла до агрегірування, що виключає
відкриття поверхні каталізатора впродовж тривалого строку роботи;
ввідсутність пор, в яких може відбуватись утворення
потовщєння.
Каталізатор наступного складу: SiO2 71,0, Al 2O3
22,75, Ag 6,25, який має молярне співвідношення SiO2/ Al 2O3
5,3, маючий у своєму складі срібло у кількості 0,13моль/моль алюмінія в
промисловому агрегаті синтезу формаліну при температурі 670-750 0С
має наступні результати: конверсія 60,4%, селективність 92,5%. У той час як
каталізатор «срібло на пемзі», який використовується у промисловості має
наступні показники: конверсія 60%, селективність 87%.
Порівняємо матеріальні баланси окислювального дегідрування
метанолу при вищеназваних каталізаторах.
Таблиця 2.1 - Матеріальний баланс з використанням
каталізатора «срібло на пемзі».
Прихід
кмоль/г
кг/г
Витрата
кмоль/г
кг/г
Спиртоповітряна суміш
Котактний газ
СН3ОН
3,161
101,136
СН3ОН
1,422
45,511
О2
0,795
25,448
СН2О
1,512
48,394
N2
2,992
83,768
СО
0,035
0,973
Н2О
0,074
1,331
СО2
0,183
8,031
N2
2,992
83,768
Н2
0,539
1,078
Н2О
1,496
23,929
Разом
7,021
211,684
Разом
8,178
211,684
Таблиця 2.2 - Матеріальний баланс з використанням
запропонованого каталізатора.
Прихід
кмоль/г
кг/г
Витрата
кмоль/г
кг/г
Спиртоповітряна суміш
Котактний газ
СН3ОН
2,765
88,469
СН3ОН
1,094
34,995
О2
0,693
22,192
СН2О
1,512
48,394
N2
2,609
73,047
СО
0,033
0,936
Н2О
0,064
1,160
СО2
0,125
5,514
N2
2,609
73,047
Н2
0,568
1,136
Н2О 20,845
Разом
6,131
184,868
Разом
7,09971
184,868
Виходячи з наведених даних таблиць, можна зробити висновки,
що при використанні запропонованого каталізатора знижується витрата метанолу на
6%. Це дозволяє значно знизити собівартість продукційного формальдегіду.
У результаті впровадження нового каталізатора, річний
економічний ефект при обсязі виробництва 43000 т/рік становить 2211920 грн.
Таблиця 2.1 - Норми технологічного режиму
Найменування стадії й потоків реагентів
Найменування параметра
Номінальні значення
Граничні значення
Стадія спиртовипарення й окисної конверсії
1
2
3
4
1. Метанольно-водна суміш із трубопроводу на вході у
спиртовипарювач
с при 15 °С, г/см3 w СН3ВІН, %
0,850 - 0,898 60 -80
2. Метанол технологічний на вході у спиртовипарювач
Об'ємна витрата л/г не більше
2154
2200
3. Конденсат на вході у спиртовипарювач
Об'ємна витрата л/г не більше
1172
1200
4. Рідина системи вловлювання на вході у
спиртовипарювач
Об'ємна витрата л/г не більше
390,63
400
5. Повітря на вході у спиртовипарювач Тиск, МПа не більше Об'ємна
витрата м3/г не більше Мольне співвідношення - 19630,06
- 2000
1,5 - 1,9
6. Рідка фаза у спиртовипарювачі
Рівень Температура, °С с при 15 °С, г/см3
не більше w СН3ВІН, % не менш
135- 175 73 - 81
130 - 180 72 - 82 0,9752 15
7. Парова фаза у спиртовипарювачі
Тиск, МПа не більше Температура, °С
0,059 71,5 - 78,5
0,06 70 - 80
8. Метанольно-водно-повітряна суміш після
перегрівача
Температура, °С не менш
101,5
100
9. Циркуляційний конденсат на вході у
спиртовипарювач
Температура, °З
74,5 ч 93,5
74 ч 95
10. Циркуляційний конденсат у лінії нагнітання
насосу
Тиск, МПа не менш
0,17
0,16
11. Напірний бак циркуляційного конденсату
Рівень % шкали приладу не менш
32,34
30
12. Зона контактування
Температура, °С
655,5 ч 744,5
650 ч 750
13. Гази на виході з подконтактного холодильника
Тиск, МПа не більше
0,0595
0,06
Стадія поглинання
14. Кубова частина поглинальної колони формаліну
Рівень % шкали приладу Тиск, МПа не більше
Температура, °С
32,34 - 77,66 0,059 61,5
30 ч 80 0,06 60
15. Гази на виході з поглинальної колони
Температура, °С не більше
38,5
40
16. Конденсат на зрошення поглинальної колони
Об'ємна витрата л/г не більше
1160
1200
17. Збірник конденсату
Рівень % шкали приладу
31,84 ч 78,16
30 ч 80
18. Формалін з поглинальної колони
с при 20 °С, г/см3 w СН2О, % w СН3ОН, %
(кислот у перерахуванні на мурашину, %
1,063 ч 1,13 30 ч 42 3 ч 14 0,02
19. Гази, що відходять, на виході з поглинальної
колони
Об'ємна частка, % С не більше С2 не
більше Н2 О2 не більше
7,0 3,0 12 ч 26 1,0
.1.1 Матеріальний розрахунок окислювального дегідрування
метанолу у формальдегід
- річна продуктивність агрегату по
формаліну 43000 т;
- річний фонд робочого часу 8400 год;
- масова частка формальдегіду в
товарному формаліні 0,370;
- масова частка формальдегіду у формаліні-сирці 0,290;
- втрати формаліну на всіх стадіях
виробництва 3 %;
- параметри подаваємого повітря:
температура 25 °С, тиск 0,17 МПа;
- ступінь конверсії метанолу 0,604;
- частка перетвореного метанолу, що
витрачається за реакцією(1.3) - 0,3, за реакцією(1.4) - 0,605, за реакцією(1.5)
- 0,075, за реакцією(1.6) - 0,02;
- масова частка води в технічному
метанолі 0,1;
Визначаєм загальну витрату метанолу на процес. Розраховуєм
витрату повітря на отримання формальдегіда, склад у ньому водної пари.
Годинна продуктивність агрегату по формальдегіду:
З урахуванням втрат необхідно одержати в контактному апараті формальдегіду:
Витрата метанолу за реакціями 3-4:
Витрата метанолу за реакцїями 3-6:
Де 0,605 та 0,3 - частка метанолу, перетвореного у формальдегід за реакціями
1.3 і 1.4.
Кількість метанола з урахуванням ступені конверсії: Кількість води у технічном метанолі: Залишок метанола у контактному газі:
,88-71,86=47,03 За реакцією 3 витрачається метанола:
,86*0,3=21,56 Утворюється:
Формальдегіда:21,56*30=646,697 Водня: 21,56 За реакцією 4 витрачається:
Метанола:71,86*0,605=43,472 Кисня: 43,472*0,5=21,736 Утворюється:
Формальдегіда:43,472 Водяної пари: 43,472 За реакцією 5 витрачається:
Метанола:71,86*0,075=5,389 Кисня: 5,389*1,5=8,084 Утворюється:
Діокису вуглецю:5,389 Водяної пари: 5,389*2=1078 За реакцією 6 витрачається:
Метанола:71,86*0,02=1,437 Утворюється:
Окису вуглецю:1,437 Водня: 1,437*2=2,874 Вссього утворюється:
Водня: 21,56+2,874=24,431 Водяної пари: 43,472+10,78=54,25 Загальна витрата кисня: 21,736+8,084=29,820 Молярне співвідношення 02: CH 3OH дорівнює:
Кількість сухого повітря :
Де 0,21 - об'ємна частка кисня у сухому повітрі.
Кількість азота у повітрі:
Об’ємна частка водяної пари у повітрі:
Де 3230- парціальний тиск водяних парів у повітрі при Т 25°, Па.
,17*106 - загальний тиск повітря, Па.
Кількість водяної пари у повітрі:
Сумарна кількість водяних парів:
У спиртоповітряній суміші:
У контактному газі:
Складаємо таблицю матеріального балансу.
Таблиця 3.1 - Матеріальний баланс стадії синтезу формальдегіду
Прихід
Витрата
компоненти
кг/год
кмоль/г
компоненти
кг/г
кмоль/г
1. Метанол технічний
Формальдегідний газ
СН3ОН
3804,17
118,88
СН2О
2080,93
65,029
Н2О
49,89
2,77
СН3ОН
1504,8
47,03
О2
954,24
29,82
СО
40,24
1,44
N2
3141,03
112,18
СО2
237,12
5,39
N2
3141,03
112,18
Н2
48,86
24,43
Н2О
896,34
49,80
Разом
7949,32
263,651
Разом
7949,32
305,287
Видатковий коефіцієнт по метанолу становить:
де 71,86 -витрата метенолу за реакціями 3-6, ,05- годинна продуктивність агрегату за формаліном, кг,
,999- масова частка метанолу в технічному метанолі.
Видатковий коефіцієнт по повітрю:
де 1,29-густина повітря при нормальних умовах, Видатковийкоєфіцієнт по воді:
де 2405- витрата води на зрошення, кг/г.
Вихідні дані:
· витрата парогазової суміші на вході в
контактний апарат 263,651 кмоль/г;
· температура парогазової суміші на
вході у контактний апарат 100-120°С;
· витрата формальдегідного газу 305,287
кмоль/г;
· температура формальдегідного газу на
виході з апарата 700 - 750 °С.
Загальне рівняння теплового балансу безперервного процесу має
такий вигляд:
Q1 + Q2 + Q3 = Q4
+ Q5 + Q6 + Q7,
(3.1)
де Q1 - тепловий потік вступник сировини;2
- тепловий ефект екзотермічних реакцій і фазових переходів;3 -
тепловий потік, що надходить в апарат з теплоносієм;4 - фізична
теплота продуктів реакцій;5 - тепловий ефект ендотермічних реакцій і
фазових переходів;6 - теплота, що відводиться від апарата
холодоагентом;7 - теплові втрати поверхнею апарата.
де Зм,i - молярна теплоємність, де нi - стехіометричний коефіцієнт;
ДHi - энтальпія утворення, Т - термодинамічна температура реакції, К.
Приймаємо Q3,6 = 0, тому що апарат є адіабатичним.
Втрати тепла Q7 приймаємо 3 % від приходу тепла (Q1
+ Q2).
З довідника [5] визначаємо коефіцієнти а, b, з і с', на підставі яких
визначаємо теплоємності за рівняннями:
· для неорганічних речовин · для органічних речовин Таблиця 3.2 - Значення коефіцієнтів а, b, з, с' і
теплоємкостей продуктів і реагентів
O2
CO
H2O
H2
CO2
N2
СН2О(г)
СН3ОН(г)
а
31,46
28,41
30
27,28
44,14
27,87
18,82
15,28
в*103
3,39
4,1
10,71
3,26
9,04
4,27
58,38
105,2
с*106
0
0
0
0
0
0
-15,61
-31,04
T, K
с' *10-5
3,77
-0,46
0,33
0,5
-8,54
0
0
0
110+273
Cp T, K
35,33
29,67
34,33
28,87
41,78
29,51
38,89
51,02
700+273
Cp T, K
35,16
32,35
40,46
30,50
52,03
32,02
60,85
88,25
Таким чином, тепло принесене з реагентами буде:
На підставі довідкових даних энтальпії утворення [5] і середньої
теплоємності [5] визначаємо теплоти реакцій:
Таблиця 3.3 - Визначення теплоти реакції (1.3)
СН3ОН(г)
= СН2О(г)
+ H2
D
niмоль
1
1
1
1
-201,2
-115,9
0
85,3
Cp 298-1000 K
69,22
49,5
28,77
9,05
Таблиця 3.4 - Визначення теплоти реакції (1.4)
СН3ОН(г)
+ 0,5O2
= СН2О(г)
+ H2O
D
niмоль
1 1
1
0,5
-201,2
0
-115,9
241,81
156,51
Cp 298-1000 K
69,22
32,43
49,5
37,07
1,135
Таблиця 3.5 - Визначення теплоти реакції (1.5)
СН3ОН(г)
+ 1,5O2
= СO2
+ 2H2O
D
1
1,5
1
2
0,5
-201,2
0
-393,51
-241,81
-675,93
Cp 298-1000 K
69,22
32,43
47,15
37,07
3,425
Таблиця 3.6 - Визначення теплоти реакції (1.6)
СН3ОН(г)
= CO
+ 2H2
D
ni , моль
1
1
2
2
-201,2
-110,53
0
90,67
Cp 298-1000 K
69,22
30,92
28,77
19,24
Таким чином, теплота реакції буде
Разом з реагентами з реактора вийде тепла:
Прихід тепла:1 + Q2 = 416,688 + 2744,678 =
3161,366 кВт.
Втрати тепла в навколишнє середовище складуть:7 = 0,03∙
3161,366 = 94,841 кВт.
Витрата тепла:
4
+ Q7 = 4,11·tx + 94,841.
Звідки температура формальдегідного газу на виході з реактора складе:
що відповідає прийнятому інтервалу температур.
Реактор (контактний апарат) призначений для окисного
дегідрування метанолу у формальдегід у газовій фазі на срібляному каталізаторі.
Для розрахунку обраний вертикальний циліндричний апарат з конусоподібним
ковпаком, змонтований безпосередньо над верхньою трубною дошкою підконтактного
холодильника. На трубну дошку укладаються перфоровані трубні ґрати із двома
нержавіючими або мідними сітками, на який засипається шар каталізатора.
Розігрів каталізатора проводять трьома ніхромовими
электроспіралями (d = 0,4 мм, U = 220 У).
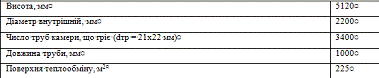
Технічна характеристика контактного апарата:
Продуктивність по формаліну т/рік (апарат№5 за
даними технологічного регламенту)
22176
Діаметр внутрішній, мм
1400
Висота шару каталізатора, мм
127
Апарат має штуцер входа спиртоповітряної суміші Dy
= 350, py = 0,6.
Необхідне кількість реакторів:
Таким чином, для забезпечення заданої продуктивності необхідно
встановити два апарата.
Об'ємна витрата спиртоповітряної суміші:
При об'ємній швидкості Vоб = 30000 год-1
необхідний обсяг каталізатора дорівнює:
У прийнятому стандартному апарату обсяг каталізатора дорівнює:
отже, запас продуктивності по каталізаторі становить:
Об'ємна витрата формальдегідного газу при температурі 973 К и тиску
0,06 МПа складе:
Лінійна швидкість газу в перетині апарата:
що відповідає оптимальному технологічному режиму [8].
Спиртовипарювач призначений для випару 60 - 70 %-ного
метанолу й одержання метанольно-водно-повітряної суміші. Спиртовипарювач являє
собою вертикальний сталевий циліндричний апарат із циркуляційною трубою
трависною камерою, що гріє, виконаної у вигляді кожухотрубчатого
теплообмінника. Гріюча камера, являє собою пучок труб, верхні й нижні кінці
яких завальцовані в трубні решітки, приварені до обечайки. Гріюча камера
з’єднується з циркуляційною трубою перехідною (зверху) та нижньою камерою.
Перехідна камера тангенціально з’єднана із барботером - целіндричною посудиною
із конічним дном, який з’єднан з нижньою камерою циркуляційною трубою і має
отвори діаметром 10 мм.. У верхній частині сепаратора розташован секційний
об’ємно-сітчастий краплеотбійник.
Циркуляція розчину в апараті здійснюється за замкнутим
контуром: барботер - циркуляційна труба - нижня камера - гріюча камера -
перехідна камера - барботер. Метанол, піднімаючись по трубам гріючої камери,
нагрівається і закіпає. У перехідній камері парорідинна суміш насичується
повітрям та направляється у барботер, де відбувається розподіл рідинної та
парової фаз.Спиртоповітряна суміш, прходячи краплеотбійник, звільняється від
крапель і виходить із апарата, а метанол повертається по циркуляційній трубі у
гріючу камеру, де відбувається його випаровування.
Технічна характеристика спиртовипарювача:
Апарат постачений штуцером введення метанольно-водної суміші
Dy = 450, py = 1, штуцером входу повітря Dy =
350, py = 1, штуцерами входу й виходу конденсату Dy =
100, py = 1, штуцером виходу метанольно-водно-воздушної суміші Dy
= 350, py = 0,6.
Приймаємо агрегатну схему компонування встаткування, по якій
на один контактний апарат доводиться один спиртовипарювач.
Вихідні дані:
· теплоносій - циркуляційний конденсат,
що утвориться при конденсації пари, отриманого при охолодженні контактного газу
в підконтактному холодильнику, тиск у лінії нагнітання насоса 0,16 МПа,
температура 75 ч 95 °С;
· температура метанольно-водної суміші
й повітря, що надходить у спиртовипарювач 25 °С;
· температура
метанольно-водно-воздушної суміші на виході зі спиртовипарювача70 ч 80 °С, витрата
- 3951,828 кг/г;
· у спиртовипарювач подають 3804,17
кг/г технічного метанолу, 49,89 кг/г води, сухого повітря - 4095,27 кг/г.
· Тепловий баланс спиртовипарювача в
загальному виді описується рівнянням:
Q1 + Q2 + Q3 = Q4
+ Q5 + Qпот,
(3.7)
де Q1, Q2, Q3, Q4
- теплові потоки метанольно-водної суміші, конденсату, повітря й
метанольно-водно-воздушної суміші відповідно, кВт;5 - теплота, що
витрачається на випар метанолу й води, кВт;пот - втрати в навколишнє
середовище, кВт.
Відомості про теплоємність компонентів
метанольно-водно-повітряної суміші зведені в табл. 3.7 [5].
Таблиця 3.7 - Теплоємність деяких речовин газоподібному стані
O2
H2O
N2
СН3ОН(г)
31,46
30
27,87
15,28
в*103
3,39
10,71
4,27
105,2
с*106
0
0
0
-31,04
T, K
с' *10-5
3,77
0,33
0
0
298
Cp T, K
36,72
-
29,14
-
348
Cp T, K
35,75
34,00
29,36
48,13
Таблиця 3.8- Деякі фізичні властивості метанолу й води [6]
H2O
СН3ОН(г)
Теплоємність ІЗ, Дж/(моль·К)
75,366
81,60
Теплота пароутворення r, кДж/кг
2297,0
1050,1
Тепловий потік метанольно-водної суміші:
Тепловий потік повітря:
Тепловий потік парогазової суміші:
Витрата тепла на випар води й метанолу:
Приймаємо Qпот = 1% витрати (приходу) тепла:
Таким чином, кількість тепла, підводима з теплоносієм, буде:
Витрата теплоносія:
де 85 і 80 - початкова й кінцева температури теплоносія відповідно,
°С;
,9 - КПД теплообмінника.
Таблиця 3.9 - Тепловий баланс спиртовипарювача
Прихід
кВт
%
Витрата
кВт
%
1. Тепловий потік метанольно-водної суміші
68,37
2,83
1. Тепловий потік парогазової суміші
209,119
8,66
2. Тепловий потік теплоносія
2317,15
95,92
2. Тепловтрати на випар
2182,787
90,35
3. Тепловий потік повітря
30,305
1,25
3. Тепловтрати в навколишнє середовище
23,919
0,99
Разом
2415,825
100
Разом
2415,825
100
Необхідну площу поверхні теплообміну визначають із рівняння
теплопередачі [7, (4.72), с. 168]:
Q = К·F∙ Дtср,
(3.8)
де Q - тепловий потік через поверхню теплообміну, Вт;
К - коефіцієнт теплопередачі, Вт/(м2·К);
Дtср - середня різниця температур гарячого й
холодного теплоносія,0С;- поверхня теплообміну, м2.
Метанольно-водна суміш нагрівається від 25 до 75 °С, а
теплоносій охолоджується з 85 до 80 °С:
°С 80 °С
°С 25 °С
Дtб = 80 - 25 = 55 °С,
Дtм = 85 - 75 = 10 °С.
Коефіцієнт теплопередачі визначається за формулою [7]:
де Коефіцієнт теплопередачі від конденсату до стінки труби
визначається по формулі [6]:
Таблиця 3.10 - Деякі фізичні властивості метанолу, парового
конденсату й метанольно-водної суміші [7]
Речовина
t, °З
с, кг/м3
м·106, Па·с
н·106, м2/с
с, кДж/(кг·К)
л·102, Вт/(м·К)
в·104, К-1
Конденсат паровий
55
985,5
509,5
0,517
4,18
65,35
4,8
82,5
365,5
85
970,25
344,5
0,345
4,19
67,75
6,64
Метанол
55
760,5
373,5
0,491
2,68
20,59
1,29
Метанольно-водна суміш
77,5
-
320,33
-
3,42
34,44
-
55
828
414,3
0,499
3,13
34,02
2,34
Швидкість руху конденсату у міжтрубному просторі:
При такій швидкості руху конденсату у міжтрубному просторі критерій
Рейнольдса:
Де Визначимо критерії Прандтля й Грасгофа [7]:
Де
Ре = Re*Pr
Таким чином, коефіцієнт тепловіддачі від конденсату трубі:
Приймаємо швидкість руху метанольно-водної суміші в трубному просторі
0,1 м/с, тоді критерій Рейнольдса:
Критерій Прандтля при температурі стінки:
режим руху перехідний; критерій Нуссельта визначаємо по графічній
залежності [7]:
Таким чином, коефіцієнт тепловіддачі від труби метанольно-водної
суміші:
Сума термічних опорів стінки труби з урахуванням шарів забруднень:
Уrст = r1 + д/л + r2,
(3.12)
де r1, r2 - опір шарів забруднень
по обидва боки стінки труби [7], м2·ДО/Вт;
д - товщина стінки труби, м;
л - теплопровідність нержавіючої сталі [7], Вт/(м·К).
Уrст = 0.0004 + 0,002/17,5 + 0,00017 = 0,00166 м2·К/Вт.
Таким чином, коефіцієнт теплопередачі буде:
Поверхню нагрівання визначаємо за рівнянням:
Запас поверхні теплообміну складе:
Підконтактний холодильник призначений для швидкого
охолодження контактного газу до 140 - 160 °С щоб уникнути формальдегіду, що
розклався.
Для установки обраний вертикальний сталевий кожухотрубчатий
теплообмінник із протиточним рухом теплоносія у міжтрубному просторі і
контактному газі у трубному просторі. Теплоносій - циркуляційний конденсат (р
= 0,3 МПа, t = 80 °С).
У холодильнику передбачене шахове розташування труб (по
вершинах правильних шестикутників). Температурні напруги, викликувані різницею
температур між кожухом і трубами, можуть привести до руйнування апарата; щоб
уникнути цього на корпусі встановлений лінзовий компенсатор.
Технічна характеристика холодильника:
Висота, мм
2500
Діаметр внутрішній, мм
1400
Число труб камери, що гріє (dтр = 2122 мм)
2800
Поверхня теплообміну, м2
460
Апарат постачений штуцером виходу контактного газу Dy
350, ру 0,6, двома штуцерами входу й двома штуцерами виходу
конденсату Dy 200, ру 0,6.
Вихідні дані:
· у холодильник подають 305,287 кмоль/г
формальдегідного газу;
· температура: на вході у холодильник
706 °С; на виході з холодильника 150 °С;
· витрата холодного конденсату 442713,6
кг/г.
Тепловий баланс спиртовипарювача в загальному виді описується
рівнянням:
Q1 = Q2 + Q3 + Qпот,
(3.13)
де Q1, Q2, - теплові потоки
формальдегідного газу на вході й на виході з холодильника, кВт;3 -
теплота, що відводиться конденсатом, кВт;пот - втрати в навколишнє
середовище, кВт.
Відомості про теплоємність компонентів формальдегідного газу
зведені в табл. 3.11 [5].
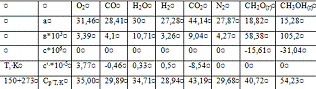
Таблиця 3.11- Значення коефіцієнтів а, b, з, с' і
теплоємкостей продуктів і реагентів
Тепловий потік формальдегідного газу на вході у холодильник
3067,929 кВт (визначений при розрахунку контактного апарата).
Тепловий потік формальдегідного газу на виході з холодильника
буде:
Приймаємо, що втрати тепла в навколишнє середовище рівняються 5% від
приходу тепла:
Кількість тепла, що відводиться циркуляційним конденсатом:
Кількість тепла, що відводиться конденсатом, описується рівнянням:
Таким чином, температура конденсату на виході з холодильника
буде:
Складаєм тепловий баланс підконтактного холодильника (табл. 3.12).
Таблиця 3.12- Тепловий баланс підконтактного холодильника
2.3
Норми технологічного режиму
![]() 0,059
0,059
3.
РОЗРАХУНКИ
.1
Матеріальні розрахунки стадій свиробництва формальдегіду
Вихідні
дані:
![]() .
Або 1894,048/30=63,135
.
Або 1894,048/30=63,135 ![]()
![]() .
.
![]()
![]() ,
,
![]() ,
,
![]() ,
,
![]() .
.
![]()
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]()
![]() .
.
![]() ,
,
![]() ,
,
![]() ,
,
![]() .
.
![]() .
.
![]() .
.
3.1.2
Розрахунок основних видаткових коефіцієнтів на одиницю продукції, що випускається
![]() ,
,
![]() ,
,
![]() ;
;
![]() .
.
![]() ,
,
3.2
Теплоенергетичні розрахунки основних технологічних стадій процесу
![]()
![]() ;i - молярний потік, кмоль/з;-
температура речовин, °С.
;i - молярний потік, кмоль/з;-
температура речовин, °С.

![]() ;
;
![]() (3.5)
(3.5)
![]() (3.6)
(3.6)
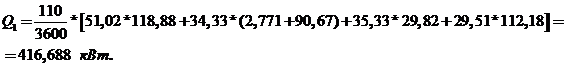
![]()
![]() .
.
![]()
![]() .
.
![]() моль
моль
![]() .
.
![]()
![]() .
.
![]()
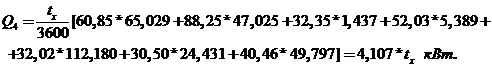
![]() ,
,
3.3
Технологічний розрахунок основного устаткування
.3.1
Технологічний розрахунок контактного апарата
![]() .
.
3.3.2
Розрахунок реактора
![]() .
.
![]() .
.
![]() ,
,
![]() .
.
![]() .
.
![]() ,
,
3.3.3
Технологічний розрахунок спиртовипарювача
3.3.3.1
Призначення, пристрій і основні розміри. Визначення кількості апаратів
3.3.3.2
Тепловий розрахунок
![]() .
.
![]() .
.
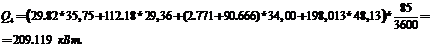
![]() .
.
![]() .
.
![]() .
.
![]() ,
,
3.3.3.3
Розрахунок спиртовипарювача
![]() .
.
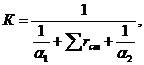 (3.9)
(3.9)
![]() - коефіцієнти тепловіддачі для гарячого й холодного
теплоносія, Вт/(м2·ДО);
- коефіцієнти тепловіддачі для гарячого й холодного
теплоносія, Вт/(м2·ДО);
![]() -
сума термічних опорів всіх шарів, з яких складається стінка, (м2·К)/Вт.
-
сума термічних опорів всіх шарів, з яких складається стінка, (м2·К)/Вт.
![]() (3.10)
(3.10)
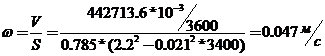 .
.
![]() ,
,
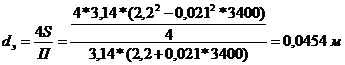 .
.
![]() ;
;
![]() ;
;
![]() ,
режим руху ламінарний; критерій Нуссельта розраховують по формулі [7]:
,
режим руху ламінарний; критерій Нуссельта розраховують по формулі [7]:
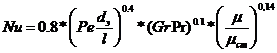 ,(3.11)
,(3.11)
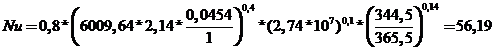 .
.
![]() .
.
![]() .
.
![]() .
.
![]() .
.
![]() ;
;
![]() ,
,
![]() .
.
![]() .
.
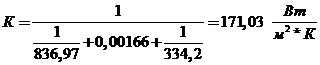 .
.
![]() .
.
![]() .
.
3.3.4 Технологічний розрахунок підконтактного холодильника
3.3.4.1
Призначення, пристрій і основні розміри
3.3.4.2
Тепловий розрахунок
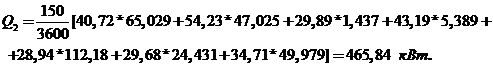
![]()
![]()
![]() (3.14)
(3.14)
![]()