Материал: Обладнання для виробництва інтерферону
Обладнання для виробництва інтерферону
1. Iнтерферон
.1 Загальна характеристика інтерферону
Інтерферон, точніше інтерферони, ─ глікопротеїди з молекулярною масою від 12 до 160 кДа, що володіють широким спектром біологічної активності: придушення репродукції вірусів; участь у регуляції імунологічних реакцій; мають радіозащитну дію, придушення розмноження пухлинних клітин і інші ефекти. "Багатоликість" інтерферонів дозволяє віднести їх до біорегуляторів.
Інтерферон виробляється клітинами тільки під впливом зовнішнього стимулу. Індукцію інтерферону можливо здійснити в клітинах різних видів тварин, починаючи з риб і кінчаючи ссавцями. При багатьох вірусних захворюваннях інтерферон знаходять у різних клінічних матеріалах: у виділеннях з носа, крові, в сечі хворих на грип, парагрип, при аденовірусній, респіраторно-синцитіальних інфекціях; в сльозах при пікорнавірусному епідемічному кон’юнктивіті; в крові при вірусному гепатиті В; в спинномозковій рідині хворих асептичним менінгітом ентеровірусної та паротитної етіології. Інтерферон є як би "побічним продуктом" вірусної інфекції, і йому приписують важливу роль в її обмеженні.
Інтерферони (IFN) - клас білків, що виділяються клітинами організмів більшості хребетних тварин у відповідь на вторгнення інородних агентів, таких як віруси, деякі інші паразити та ракові білки. Завдяки інтерферонам клітини стають несприйнятливими по відношенню до цих агентів. Механізм дії інтерферонів полягає у викликанні каскаду реакцій, що приводять до руйнування дволанцюжкових РНК та деяких інших молекул.
Інтерферони людини підрозділяють на групи залежно від типу клітин, в яких вони утворюються: α, β, γ і т. д. α-інтерферони включають кілька видів білків з молекулярною масою близько 20 000 Да. За типом рецепторів, через які відбувається сигнальна дія інтерферонів, інтерферони поділяють на типи I (IFN-α, IFN-β, IFN-ω), II (IFN-γ) і III (IFNLR1, IL10R2).
1.2 Історія відкриття інтерферону
Відкриття інтерферону починалося з вивчення відомого у вірусології явища інтерференції. Англійський вчений А. Айзекс і його помічник Дж. Лінденман в 1957 році, вводячи в курячі ембріони інактивований УФ-променями вірус грипу, виявили в аллантоісній рідині інгібітор, який володів широким спектром противірусної дії і придушував репродукцію різних РНК-геномних і ДНК-геномних вірусів. Вони показали, що інгібітор є білком, і назвали його інтерфероном.
За півстоліття з моменту відкриття інтерферону проведено величезну кількість досліджень його фізико-хімічних властивостей, механізмів утворення клітиною і противірусної, і непротівовірусногї дії, методів отримання та практичного застосування для профілактики вірусних хвороб людей і тварин. Тим часом інтерес до інтерферону як фактору противірусного імунітету і противірусного препарату не згасає і в даний час.
У культурі клітин інтерферон синтезують клітини самого різного типу, але особливо хорошими продуцентами його є лейкоцити крові. Ця обставина лягла в основу виробництва людського лейкоцитарного інтерферону. Перша вітчизняна лабораторія з виробництва лейкоцитарного інтерферону була організована з ініціативи академіків В.Д. Соловйова та З.В. Єрмольєвої в Москві в 1968 році. Для синтезу інтерферону використовувалася лейкоцитарна маса, одержувана зі станцій переливання крові.
У клітинах продукція інтерферону і формування противірусної резистентності знаходяться під жорстким генетичним контролем. Гени для утворення інтерферону локалізовані в 5, 9 і 13 хромосомах людини, а для дії ─ в 16 і 21 хромосомах. Втрата, наприклад, 21 хромосоми призводить до нечутливості клітин до інтерферону.
Вперше в 1975 році з фібробластів людини вдалося екстрагувати інтерферонову інформаційну РНК і в безклітинної рибосомальної системі відтворити її трансляцію з утворенням людського інтерферону з молекулярною масою 25 кДа. Пізніше було продемонстровано здатність клітин бактерій (E. coli) транслювати інтерферонову іРНК, отриману з кісткового мозку людини.
Результати цих досліджень з’явилися передумовою для експериментів по зворотній транскрипції інтерферонової іРНК (за допомогою ферменту зворотної транскриптази) для отримання генів інтерферону людини. І в 1981 році М. Едж із співробітниками Лейчестерського університету у Великобританії синтезував ген лейкоцитарного інтерферону людини, який ідентичний гену, що міститься в клітинах організму. А роком пізніше (1982 р.) бактеріальний інтерферон методом генної інженерії було синтезовано і в нашій країні. В даний час учені синтезували ДНК-гени всіх трьох антигенних різновидів інтерферону людини і деяких видів тварин. За допомогою методів генної інженерії здійснена успішна пересадка отриманих генів у кишкову паличку і дріжджові клітини. Таким чином були отримані нові клітини-продуценти людського інтерферону. Конструюванням бактерій, які продукують інтерферон, давно займаються вітчизняні вчені Інституту біоорганічної хімії, НДІ епідеміології та мікробіології ім. Н.Ф. Гамалії та Інституту вірусології ім. Д.І. Іванівського.
Інтерферон не проникає в клітину, а активує її до формування противірусної резистентності непрямим шляхом, взаємодіючи з рецепторами на клітинній поверхні. Хромосома 21 є носієм гена, в якому закодований синтез інтерферонову рецепторів. Рецептори дозволяють клітині розпізнати інтерферон і передати сигнал про його присутність іншим структурам, які повинні на цей сигнал прореагувати. Взаємодія інтерферону з рецептором супроводжується зміною конформації останнього, а це є необхідним етапом для подальшої передачі інформації в клітині та формування антивірусного стану.
Важливо відзначити, що пріоритет використання інтерферону як противірусного препарату належить вітчизняним ученим. Так, в 1968 ─ 1969 рр.. з ініціативи В.Д. Соловйова людський лейкоцитарний інтерферон був вперше з успіхом використаний для масової профілактики гонконгського грипу, пізніше ─ для лікування грипу А у вигляді аерозолю в перші два дні хвороби. Ефективним виявилося профілактичне застосування інтерферону серед дітей дошкільних установ в період спалахів грипу А. Інтраназальне введення препарату, якщо не попереджало інфікування вірусом, то завжди пом’якшувало протікання викликаного їм захворювання. Інтерферон виявився дуже ефективним засобом для профілактики і лікування риновірусні інфекцій при частому закапуванні в ніс.
Роком пізніше (1970 р.) З.В. Ермольева із
співробітниками успішно застосувала інтерферон для лікування герпетичного
кератиту та оперізувального лишаю. У подальшому інтерферон знайшов широке
застосування при герпетичної інфекції різної локалізації у вигляді крапель,
мазі, ін’єкцій. Є окремі повідомлення про вираженому терапевтичному ефекті
інтерферону при цитомегаловірусної інфекції, вродженої краснухи, гепатиті В.
Широке застосування інтерферону для профілактики і лікування вірусних інфекцій
вимагає розширення виробництва препаратів людського походження. У цьому
відношенні великі надії покладаються на отримання генноінженерних препаратів
людського інтерферону.
2. Технологія виробництва інтерферону. Основні недоліки, які
виникають при виробництві
Відомі способи отримання лейкоцитарного інтерферону людини з лейкоцитів донорської крові людини, індукованих вірусами та іншими індукторами.
Основним недоліком цих способів отримання інтерферонів є ймовірність контамінації кінцевого продукту вірусами людини, такими як вірус гепатитів В і С, вірусу імунодефіциту та ін.
В даний час більш перспективним визнаний спосіб отримання інтерферону мікробіологічним синтезом, який забезпечує можливість отримання цільового продукту зі значно більш високим виходом з порівняно недорогого вихідної сировини. Використовувані при цьому підходи дозволяють створити оптимальні для бактеріальної експресії варіанти структурного гена, а також регуляторних елементів, контролюючих його експресію.
У якості вихідних мікроорганізмів використовують різні конструкції штамів Pichia pastoris, Pseudomonas putida і Escherichia coli. Недоліком використання P. pastoris в якості продуцента інтерферону, є вкрай складні умови ферментації цього типу дріжджів, необхідність суворо підтримувати концентрацію індуктора, зокрема метанолу, в процесі біосинтезу.
Недоліком використання штамів Ps. putida є складність процесу ферментації при низькому рівні експресії (10 мг інтерферону на 1 л культурального середовища). Більш продуктивним є використання штамів Escherichia coli.
Відомо велика кількість плазмід та створених на їх основі штамів Е. coli, експресують інтерферон: штами Е. coli ATCC 31633 і 31644 з плазмідами Z-pBR322 (Psti) HclF-11-206 або Z-pBR 322 (Pstl) / HclN SN 35 -AHL6 (SU 1764515), штам Е. coli pINF-AP2 (SU 1312961), штам Е. coli pINF-F-Pa (AU 1312962), штам E. Coli SG 20050 з плазмидой p280/21FN (Кравченко В.В. та ін Біоорганічна хімія, 1987, т.13, № 9, с.1186-1193), штам E. Coli SG 20050 з плазмидой pINF14 (SU 1703691), штам E.coli SG 20050 з плазмидой pINF16 (RU 2054041) і др. Недоліком технологій, заснованих на використанні цих штамів, є їх нестабільність, а також недостатній рівень експресії інтерферону.
Поряд з особливостями використовуваних штамів ефективність процесу багато в чому залежить від використовуваної технології виділення і очищення інтерферону.
Відомий спосіб отримання інтерферону, що включає в себе культивування клітин Ps. putida, руйнування біомаси, обробку поліетиленіміну, фракціонування сірчанокислим амонієм, гідрофобну хроматографію на фенілсілохроме С-80, рН-фракціонування лізата, його концентрування і діафільтрація, іонообмінну хроматографію на целюлозі DE-52, елюювання в градієнті рН, іонообмінну хроматографію отриманого елюента на целюлозі СМ -52, концентрування пропусканням через касету фільтрів і гель-фільтрацію на сефадекса G-100 (SU 1640996). Недоліком цього способу крім складної багатостадійної ферментації є багатостадійність при отриманні кінцевого продукту.
Відомий також спосіб отримання інтерферону, що включає в себе культивування штаму E.coli SG 20050/pIF16, в LB-бульйоні в колбах в термостатированной шейкері, центрифугування біомаси, її промивання буферним розчином і обробку ультразвуком для руйнування клітин. Отриманий лізат центрифугують, промивають 3М розчином сечовини в буфері, розчиняють в розчині гуанидін хлориду в буфері, обробляють ультразвуком, центрифугують, проводять окислювальний сульфітоліз, діаліз проти 8 М сечовини, ренатурацією і остаточну двостадійну хроматографію на СМ-52 целюлозі і сефадексі G-50 (RU 2054041).
Недоліками цього способу є його відносно невисока продуктивність основних етапів процесу виділення та очищення. Особливо це відноситься до ультразвукової обробки продукту, діалізу і окислювальному сульфітолізу, що призводить до нестабільності виходу інтерферону, а також до неможливості використання цього методу для промислового виробництва інтерферону. Як найбільш близького аналога (прототипу) може бути зазначений спосіб отримання лейкоцитарного інтерферону людини, що полягає в культивуванні рекомбінантного штаму E.coli, заморожування отриманої біомаси при температурі не вище -70°С, розморожування, руйнуванні клітин мікроорганізму лізоцимом, видаленні ДНК і РНК введенням в лізат ДНК-ази та очищенням виділеної нерозчинної форми інтерферону відмиванням буферним розчином з детергентами, розчиненні осаду інтерферону в розчині гуанидин гідрохлориду, ренатурації і одностадійної очищенню іонообмінної хроматографією. Як продуцент використовують штам E.coli SS5, отриманий за допомогою рекомбінантної плазміди pSS5, яка містить три промотора: Plac, Pt7 і Ptrp, і ген альфа-інтерферону з введеними нуклеотидними замінами.
Експресія інтерферону штамом E.coli SS5, що містить цю плазміду, контролюється трьома промоторами: Plac, Pt7 і Ptrp. Рівень експресії інтерферону складає близько 800 мг на 1 л клітинної суспензії. Недоліком способу є низька технологічність використання ферментативного руйнування клітин, ДНК і РНК мікроорганізму і одностадійна хроматографічна очищення інтерферону. Це обумовлює нестабільність процесу виділення інтерферону, призводить до зниження його якості та обмежує можливість використання наведеної схеми для промислового виробництва інтерферону.
Недоліками даної плазміди і штаму на її основі є використання в плазміді сильного нерегульованого промотора фага Т7 в штамі Є. coli BL21 (DE3), в якому ген Т7 РНК полімерази знаходиться під промотором lac оперона і який завжди "тече". Отже, в клітці безперервно відбувається синтез інтерферону, що призводить до дисоціації плазміди і зниження життєздатності клітин штаму, і в результаті - зниження виходу інтерферону. Для отримання великих кількостей ІФН використовують шестиденні одношарові культури клітин курячого ембріона або культивовані лейкоцити крові людини, заражені певним видом вірусу. Іншими словами, для отримання ІФН створюють певну систему вірус-клітина.
З клітки людини ізольований ген, відповідальний за біосинтез ІФН. Екзогенний людський ІФН отримують, використовуючи технологію рекомбінантних ДНК. Процедура виділення кДНК ІФН-ів полягає в наступному:
1) З лейкоцитів людини виділяють мРНК, фракціонують її за розмірами, проводять зворотну транскрипцію, вбудовують в сайт модифікованої плазміди.
2) Отриманим продуктом трансформують Є. соli; утворилися клони, які підрозділяють на групи, потім ідентифікують.
) Кожну групу клонів гібридизують з ІФН - мРНК.
4) З утворених гібридів, які містять кДНК і хРНК, виділяють мРНК, проводять її трансляцію в системі синтезу білка [4].
5) Визначають інтерферону противірусну активність кожної суміші,
отриманої в результаті трансляції. Групи, що проявили інтерферону активність,
містять клон з кДНК, гібридизувати з ІФН - мРНК; повторно ідентифікують клон,
що містить повнорозмірну ІФН - кДНК людини.
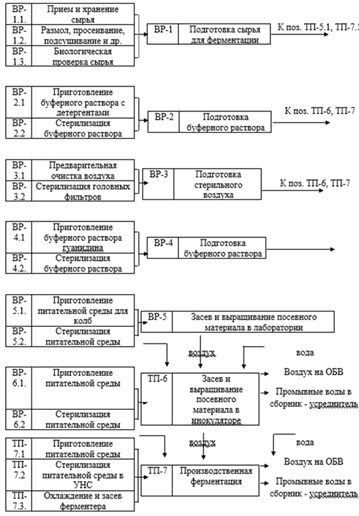
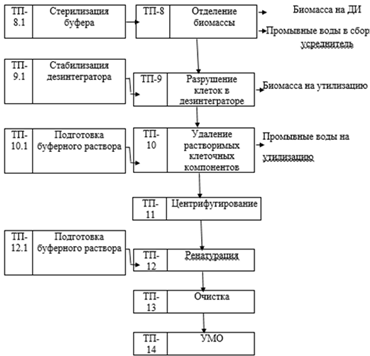
Рисунок 1. Схема виробництва інтерферону.
3. Основне
обладнання для виробництва інтерферону
.1 Реактор-змішувач
Основним технологічним обладнанням являється реактор-змішувач , в якому безпосередньо і відбувається приготування розчину . Схема реактора-змішувача представлена на рисунку 2.
Технічна характеристика реактора:
Апарат призначено для перемішування, нагрівання та охолодження суміші
1. Об’єм апарату, м3 1;
. Частота обертання вала мішалки, об/хв. 75;
4. Потужність електродвигуна, кВт 1;
. Коефіцієнт заповнення 0,8;
. Площа поверхні теплообміну рубашки, м2 4,4;
. Робочий тиск, МПа
в корпусі 0,1;
в рубашці: 0,1 - 0,3;
. Температура середовища, °С
в корпусі: 20 - 80;
в рубашці: 10 - 130;
9. Маса апарату без привода, кг 430;
. Габаритні розміри, мм
висота 1350;
діаметр 1104;
11. Виробник "Дезхімобладнання", м.
Пенза.
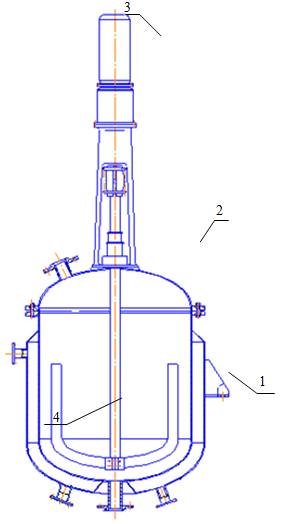
Рисунок 3.2. Схема реактора-змішувача:
1 - корпус; 2 - кришка; 3 - привід; 4 - перемішуючий пристрій.
.2 Освітлююча центрифуга
інтерферон глікопротеїд реактор центрифуга
Центрифуга являє собою освітлюючу, вертикальну, трубчасту машину з ручним вивантаженням осаду.
Центрифуга призначена для освітлення суспензій методом осадження частинок під дією відцентрових сил.
У центрифузі можуть оброблятися суспензії з тонкодисперсної твердою фазою, із вмістом частинок до 1% і ставленням питомих ваг твердої і рідкої фаз не менше 1,1.
Технічні дані
Найбільший внутрішній діаметр ротора - 105 мм.
Робоча висота ротора - 745 мм
Робочий об'єм ротора - 6 л.
максимальне завантаження - 7.7 кг
- робоча - 15000 +400
Фактор поділу - максимальний - 16800
робітник - 13200
Електродвигун приводу - потужність - 3 кВт
напруга - 220/380 В
Габаритні розміри центрифуги з електродвигуном
довжина - 970 мм
ширина - 470 мм
висота - 1830 мм
Маса центрифуги з електродвигуном - 355 кг
Робота виробу