Материал: Микрокристаллоскопия
Микрокристаллоскопия
БЕЛОРУССКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
ХИМИЧЕСКИЙ ФАКУЛЬТЕТ
КАФЕДРА
АНАЛИТИЧЕСКОЙ ХИМИИ
Курсовая работа
Микрокристаллоскопия
Студентки 2 курса, 2 группы
Химического факультета БГУ
Брановицкой Кристина Эдуардовны
Руководитель: ассистент кафедры аналитической химии
Глушко Роман Александрович
Минск
СОДЕРЖАНИЕ
Введение
Глава. Чувствительность и специфичность реакций
.1 Открываемый минимум
.2 Предельная концентрация
.3 Взаимосвязь открываемого минимума и предельной концентрации
.4 Предельное отношение
Глава. Влияние различных факторов на чувствительность реакций
.1 Объем раствора
.2 Концентрация реактивов
.3 Продолжительность опыта
.4 Влияние температуры
.5 Реакция среды
Глава. Приемы, улучшающие чувствительность
.1 Осаждение смешанных кристаллов
.2 Флотация
.3 Характер кристаллических осадков
.4 Феномен Тиндаля
.5 Контрольный опыт
.6 Другие приемы, улучшающие чувствительность
Глава. Приемы микрокристаллоскопического анализа
.1 Осаждение и перекристаллизация
.2 Фильтрование
.3 Возгонка
.4 Применение паро- и газообразных реактивов
.5 Применение металлов в качестве реактивов
Заключение
Список используемых ресурсов
ВВЕДЕНИЕ
Микрохимический анализ - наука о методах химического анализа малых, иногда микроскопических количеств вещества. Не существует четкой границы между макро- и микроанализом. Реакции, позволяющие определить искомые вещества в количестве от 0,01 мг и меньше, условно считаются микрохимическими.
Микрохимический анализ обладает рядом преимуществ, делающих его ценным и значимым:
. Необходимо малое количество определяемого вещества.
2. Быстрота выполнения.
. Низкий расход реагентов.
. Портативность аппаратуры.
. Возможность проведения реакций с дурнопахнущими и ядовитыми веществами.
Существует несколько принципиально различных методов микрохимического анализа: капельный анализ, электрокапиллярный анализ, микрокристаллоскопия, а также реакции окрашивания пламени и многие другие. Подробнее рассмотрим микрокристаллоскопический анализ.
Микрокристаллоскопический анализ - метод качественного анализа, основанный на реакциях образования характерных кристаллических осадков, которые рассматривают под микроскопом и на основании внешнего вида кристаллов делают заключение о наличии искомых ионов.
Микрокристаллоскопия была широко и глубоко исследована в конце XIX века и начале XX, принципиально новых открытий и изменений этот вид анализа не претерпевал, однако остается актуальным до сих пор.
Микрокристаллоскопия находит применение главным образом для качественного анализа очень небольших по размерам объектов (включения в металлы и минералы, мельчайшие металлические частицы, пыль, содержимое растительных и животных клеток и т.п.). Применение специфических реакций делает микрокристаллоскопию очень удобным методом анализа минералов, сплавов и других объектов, а также простым способом идентификации органических соединений.
В ходе написания курсовой работы была поставлена цель: расширить и углубить знания о микрокристаллоскопии, изучить основные факторы, влияющие на протекание микрокристаллоскопических реакций, изучить способы устранения нежелательных исходов реакций.
Из цели вытекли следующие задачи: провести аналитический обзор научной литературы: учебных пособий, электронных ресурсов, статей, соответствующих теме курсовой; выделить наиболее важную и значимую информацию; обобщить весь собранный материал.
микрохимический анализ микрокристаллоскопический реакция
ГЛАВА 1. ЧУВСТВИТЕЛЬНОСТЬ И СПЕЦИФИЧНОСТЬ
РЕАКЦИЙ
Одной из главных задач химика-аналитика является повышение чувствительности реакций. Для этого необходимо рассмотреть ряд используемых в аналитической химии понятий.
Большинство микрохимических реакций отличается
высокой чувствительностью, которая обычно выражается двумя взаимосвязанными
величинами: открываемый минимум и предельная концентрация. Существуют и другие
способы количественного выражения чувствительности, но менее распространенные.
Рассмотрим основные.
.1 Открываемый минимум
Открываемый минимум - наименьшее количество
этого вещества, дающее положительный результат при действии данного реактива.
Поскольку открываемый минимум величина на несколько тысяч порядков меньшая, чем
миллиграмм (мг), то используют другую величину - микрограмм (g).
g = 10-6 г = 10-3 мг.
Для большинства микрохимических реакций открываемый минимум выражается десятыми, сотыми либо тысячными долями микрограмма и демонстрирует минимальное количество вещества, при котором реакция еще идет. При меньшем количестве вещества реакция идти не будет.
При количестве ионов, значительно превышающем открываемый минимум, продукт реакции открывается быстро; по мере уменьшения количества ионов скорость образования продукта реакции уменьшается. При некоторых количествах вещества, близких к открываемому минимуму, мы попадаем в область ненадежной реакции, где реакция может давать как положительный, так и отрицательный результат.
Обычно за открываемый минимум принимают такое количество вещества, при котором половина из общего числа произведенных реакций дает положительный результат.
Однако на практике это использовать неудобно, поэтому вводится понятие уверенно открываемого минимума - то количество вещества, при котором данная реакция безусловно удается.
Реакции тем чувствительнее, чем меньше
открываемый минимум.
.2 Предельная концентрация
Под предельной концентрацией, или предельным разбавлением, понимают наименьшую концентрацию вещества в растворе, при которой известный объем этого раствора дает положительную реакцию. Предельную концентрацию выражают отношением открываемого иона, принимаемого за единицу, к количеству растворителя, выраженного в таких же единицах.
Реакция тем чувствительнее, чем меньше
предельная концентрация.
.3 Взаимосвязь открываемого минимума и
предельной концентрации
Уже указывалось, что открываемый минимум и предельная концентрация являются величинами взаимосвязанными. Данная зависимость выражается через формулу:
где С - предельная концентрация, m - открываемый минимум в g, v - объем раствора в мл, требующийся для выполнения одной реакции.
Пример: Микрореакция осаждения Cu2+ в виде K2PbCu(NO2)6 (рисунок 1) характеризуется открываемым минимумом в 0,03g Cu2+ в капле, равной 0,001 мл. Требуется определить предельную концентрацию:
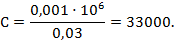
Предельная концентрация,
следовательно, равна 1:33000.

Рисунок 1. Кристаллы K2PbCu(NO2)6
.4 Предельное отношение
Основной минус микрокристаллоскопических реакций заключается в том, что при наличии посторонних ионов реакция может дать неожиданный и нехарактерный эффект, либо эффект не с искомым ионом. Поэтому всегда стараются подобрать такие условия, в которых реакция даст 100% результат на определенный ион. Но даже при нахождении подобных условий чувствительность реакции будет снижаться в присутствии посторонних ионов. Поэтому весьма важно знать, какие количества постороннего иона еще позволят найти интересующий нас ион. Это и характеризует предельное отношение.
Она демонстрирует максимальное количество данного иона, принимаемого за единицу, к постороннему иону, при котором данная реакция возможна без отделения. Предельное отношение характеризует специфичность реакций. При выборе реакции это оказывает не последнее значение.
Образование смешанных кристаллов увеличивает специфичность реакций, следовательно, увеличивается и предельное отношение.
Предельное отношение может быть еще улучшено
путем введения добавок, препятствующих посторонним ионам вступать в реакцию.
Такие добавки называются маскирующими средствами.
ГЛАВА 2. ВЛИЯНИЕ РАЗЛИЧНЫХ ФАКТОРОВ НА
ЧУВСТВИТЕЛЬНОСТЬ РЕАКЦИЙ
Чувствительность реакции играет большую роль в микроанализе и не является постоянной величиной, а зависит от ряда факторов. Несмотря на потери, которые особенно заметны при работе с малым количеством вещества, при помощи высокочувствительных реакций удается установить наличие того или иного иона в остатке.
Увеличение чувствительности качественных реакций является одной из основных целей микроскопического анализа.
В зависимости от условий реакции
чувствительность может различаться в сотни раз. Задача химика состоит в том,
чтобы подобрать условия, в которых реакция будет наиболее чувствительной и даст
наилучший результат.
.1 Объем раствора
Предельная концетрация уменьшается (улучшается), при увеличении объема. Правда, главную роль здесь играет не столько объем, сколько высота столба жидкости, связанная с ним. Чем он выше - тем проще наблюдать изменения.
Пример: Реакция Са2+ с K4[Fe(CN)6], дающая муть
CaK2[Fe(CN)6] · 3H2O, имеет в капле раствора предельное отношение 1:2000, а в
пробирке примерно 1:100.000.
.2 Концентрация реактивов
При помощи изменения концентрации реактивов
чувствительность реакции можно варьировать в очень широких пределах. Правда,
единую закономерность обнаружить нельзя, для каждой реакции эта закономерность
определяется эмпирически. Предсказать ее можно зная химические свойства
веществ.
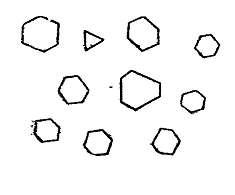
Рисунок 2. Кристаллы PbI2
Пример: При реакции на Pb2+
по образованию PbI2
(рисунок 2) имеет значение концентрация иода.
![]()
![]() , откуда
, откуда
![]()
![]() .
.
Значит, с увеличением концентрации иода происходит более полное осаждение свинца и реакция становится более чувствительной.
Но при больших концентрациях иона иода осадок PbI2 растворяется:
+ I- = [PbI3]-
Следовательно, как при малых, так и
при больших концентрациях иода чувствительность реакции будет невысокой.
Оптимальное значение находится между двумя крайними значениями.
2.3 Продолжительность опыта
Скорость реакции значительно снижается при
уменьшении концентрации искомого иона. Ионные реакции протекают относительно
быстро, но для протекания реакции слабых электролитов либо неэлектролитов может
потребоваться относительно большой промежуток времени. Влияние
продолжительности опыта на чувствительность реакции образования NaUO2(CH3COO)3
(рисунок 3) продемонстрировано в таблице 1.
Таблица 1
|
Продолжительность опыта |
Предельная концентрация |
|
Несколько секунд |
1:50000 |
|
15 минут |
1:100000 |
|
1 час |
1:200000 |
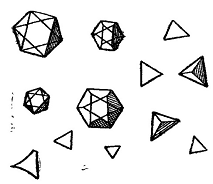
Рисунок 3. Кристаллы
NaUO2(CH3COO)3
.4 Влияние температуры
Температура оказывает значительное влияние на протекание аналитических реакций, в частности, на интенсивность окраски. Некоторые реакции при неправильном температуре режиме не дадут результата, либо он будет значительно хуже, чем мог бы быть.
Реакции с органическими веществами дают лучший результат при повышении температуры. Иногда для этих целей используют концентрированную серную кислоту, при взбалтывании которой происходит нагревание.
При реакциях с использованием окислителей либо на их обнаружение целесообразнее использовать пониженную температуру, так как окислитель может разрушить образовавшееся окрашенное вещество.
Таким образом, при выборе температурного режима
необходимо опираться на конкретные свойства реагентов: в одних случаях уместно
повышение температуры, а в других - понижение.
.5 Реакция среды
Реакция среды оказывает большое, иногда даже решающее значение на протекание опыта. Выбирать среду необходимо учитывая свойства вещества. Некоторые реакции протекают только при определенном значении рН, у других колеблется чувствительность.
Пример: Реакцию на Fe2+
с CNS- проводят только в
кислой или нейтральной среде, а чувствительность реакции будет выше при
добавлении кислоты.
ГЛАВА 3. ПРИЕМЫ, УЛУЧШАЮЩИЕ ЧУВСТВИТЕЛЬНОСТЬ
Ниже приведены лишь основные приемы, влияющие на
протекание реакций. Каждая реакция имеет свои особенности, которые необходимо
учитывать при проведении анализа. Большое количество факторов, влияющих на
протекание реакций, и объясняет тот факт, что значения открываемого минимума и
предельной концентрации у разных авторов могут колебаться в довольно широких
пределах.
.1 Осаждение смешанных кристаллов
При малых концентрациях искомого иона (микрокомпонента) осадок может не образоваться. В этом случае можно добавить подходящий ион (макрокомпонент), который будет реагировать с реактивом. В этом случае образуются смешанные кристаллы (изоморфная смесь), относящиеся к одной и той же сингонии и их кристаллографические константы окажутся очень близкими.
Изоморфно могут заменяться ионы равной валентности при условии, что их радиусы отличаются не больше, чем на 15%. Что касается гетеровалентных ионов, то ионный радиус более высоковалентного иона должен быть примерно на 10% больше, чем радиус иона с меньшей валентностью.
Если макрокомпонент образует бесцветное вещество с реактивом, а микрокомпонент - цветное, то вся изоморфная смесь приобретет характерную окраску, и заметить искомый ион будет возможно невооруженным глазом. В случае образование монохромной смеси, концентрация искомого иона будет заметно выше, чем в растворе, что сделает доступным его обнаружение при помощи подходящей качественной реакции.
Пример: Только сравнительно большие количества
солей меди и кобальта будут давать осадок с (NH4)2[Hg(CNS)4].
Первая - желто-зеленый осадок Cu[Hg(CNS)4],
второй - синий осадок Co[Hg(CNS)4].
Если в растворе присутствует соль цинка, которая легко образует осадок Zn[Hg(CNS)4],
то можно обнаружить даже малые количества меди или кобальта. Медь даст
смешанный осадок фиолетового цвета, а кобальт - голубого.
.2 Флотация
При взбалтывании мутного раствора и
несмешивающегося с ним органического вещества осадок будет образовываться на
границе раздела двух фаз - осадок флотируется. Небольшие количества осадка наш
глаз не всегда способен заметить, гораздо проще и вернее это сделать будет при
концентрации всего вещества в одном месте. Чувствительность реакции при
флотации значительно улучшается.