Материал: микра от 104 группы
34.Брожение. Получение энергии анаэробными микроорганизмами. Химизм процесса.
Брожение (субстратное фосфорилирование) - разновидность анаэробного дыхания, при котором и донором и акцептором водорода является органическое вещество. При анаэробном дыхании микроорганизмы получают энергию не путем окисления, а путем распада сложных органических веществ до более простых. Микроорганизмы, у которых имеет место анаэробное дыхание, называют анаэробами.
При брожении происходит расщепление сложных органических веществ до более просто устроенных с выделением небольшого количества энергии. При поступлении глюкозы в клетку, происходит гликолиз и образуется ПВК. Дальнейшие ее превращения зависят от набора ферментов анаэробных бактерий. В зависимости от того какие конечные продукты образуются, выделяют разные типы брожения:
· Молочнокислое брожение вызывается лактобактериями, бифидобактериями, стрептококками, образуя из ПВК молочную кислоту (гомоферментативное брожение) или молочную, янтарную, уксусную кислоты, ацетон (гетероферментативное брожение). Эти бактерии применяются в производстве молочно-кислых продуктов: ряженки, простокваши, кефира, йогуртов и творога.
· Маслянокислое брожение. Возбудителями этого вида брожения являются анаэробные бактерии рода клостридии, а также бактероиды, фузобактерии и другие микроорганизмы, вызывающие у человека опасные анаэробные инфекции. Основным продуктом брожения является масляная,изомасляная, уксусная, валериановая кислоты.
· Пропионовокислое брожение также вызывается анаэробами - пропионибактериями (обитатели кожи и слизистой оболочкичеловека и животных могут вызывать анаэробные инфекции), которые используются в производстве сыров. Конечный продукт брожения - пропионовая кислота.
· Спиртовое брожение. Вызывают дрожжи. В результате спиртового брожения образуется этиловый спирт, что издавна используется в пивоварении и виноделии.
· Бутиленгликолевое брожение. В результате брожения образуются бутиловый спирт, этиленгликоль, срероводород и другие токсические продукты. Этот вид брожения вызывают кишечная палочка и другие энтеробактерии, в том числе - возбудители кишечных инфекций - сальмонеллёза, дизентерии.
При субстратном фосфорилировании из глюкозы или других источников углерода выделяется незначительное количество энергии, так как образующиеся при этом продукты брожения (молочная кислота, спирты и др.) сохраняют в себе значительные количества энергии. Поэтому в анаэробных условиях бактериальная культура для получения необходимой энергии во много раз больше разлагает пищевого материала, чем в присутствии кислорода. Теплообразование при развитии бактериальной флоры в органическом материале (навоз, торф, мусор) может привести к его самовозгоранию.
Изучение ферментов бактерий имеет большое практическое значение для разработки методов диагностики (идентификации) возбудителей инфекционных заболеваний по набору ферментов, а также для создания современных биотехнологий получения продуктов питания в том числе молочнокислых продуктов, сыра, хлеба, вина, пива и т.д.
Химизм процесса брожения был расшифрован в 1933 г. в результате независимых исследований немецкого ученого Г. Г. Эмбдена, немецко-американского — О.Ф. Мейергофа и польско-советского — Я.О. Парнаса.
Было установлено, что брожение представляет собой последовательную цепочку реакций, протекающих в цитоплазме клетки бродящего организма под воздействием вырабатываемых здесь ферментов. В процессе анаэробной диссимиляции глюкозы различают три стадии: подготовительную, энергетическую и завершающую.
«Пусковой» реакцией катаболического распада глюкозы является ее фосфорилирование за счет АТФ с образованием глюкозо-6-фос- фата и АДФ, в результате чего молекула глюкозы активируется для участия в последующих превращениях. Катализирует реакцию фермент гексокиназа (КФ 2.7.1.1).
Затем образовавшийся глюкозо-6-фосфат (альдоза) превращается во фруктозо-6-фосфат (кетозу). Эта реакция происходит под воздействием фермента глюкозо-6-фосфат—изомеразы (КФ 5.3.1.9).
Третья реакция — фосфорилирование фруктозо-6-фосфата за счет АТФ с образованием фруктозо-1,6-бисфосфата и АДФ. Она катализируется ферментом фосфофрукгокиназой (КФ 2.7.1.11) и представляет собой еще одну «пусковую» реакцию брожения.
35. Аммонификация мочевины. Возбудители и ход процесса. Условия, определяющие накопление аммиака в почве и навозе.
Аммонификация- процесс, сопровождающийся выделением аммиака при разложении белков и азотосодержащих соединений
К азотосодержащим органическим соединения, часто встречающимися в природе, относятся мочевина, мочевая и гиппуровая кислота.
Разложение мочевины
Мочевина – конечный продукт превращения соединений азота в организме человека и животных.
Мочевину могут синтезировать почвенные грибы.
Это же соединение образуется при гидролитическом распаде аргинина под действием фермента аргиназы
Многие бактерии и грибы синтезируют уреазу, могут использовать мочевину как источник азота и для синтеза белков
Бактерии, разлагающие мочевину – уробактерии
Бактерии развиваются при щелочной среде рН 9-10, что позволяет вызвать распад значительного количества мочевины до аммиака.
Представители:
Micrococcus urea,
Bacillus pasteurii,
Sporosarcina urea
Источник углерода – углеводы и соли органических кислот
Ход процесса
Под действием микроорганизмов, содержащих фермент уреазу, мочевина в несколько этапов превращается в аммиак и диоксид углерода:
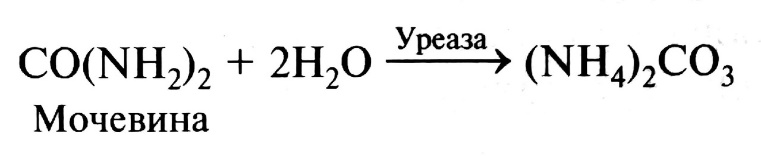
Образующиеся на первом этапе углеаммиачная соль мало устойчиво и быстро разлагается:
![]()
Значение
Мочевина содержит 46% азота используется как удобрение
Физиологический смысл распада мочевины по-видимому сводится к переводу аминный формы азота в более легко своему аммиачную
Гиппуровая кислота
Мочевая и гиппуровая кислота также играют важную роль в белковом обмене млекопитающих, пресмыкающихся, насекомых и птиц
в экскрементах змей до 90 % мочевой кислоты, в помете птиц -25%
В моче млекопитающих содержание мочевой кислоты незначительное
Разложение мочевой кислоты в местах скопления помета птиц гуано в условиях засушливого климата приводит к накоплению нитратов. Поэтому в Южной Африке, Чили, Перу есть богатые залежи нитратов
Ход процесса
Мочевая и гиппуровая кислоты быстро распадаются под влиянием гидролитических ферментов ряда микроорганизмов:
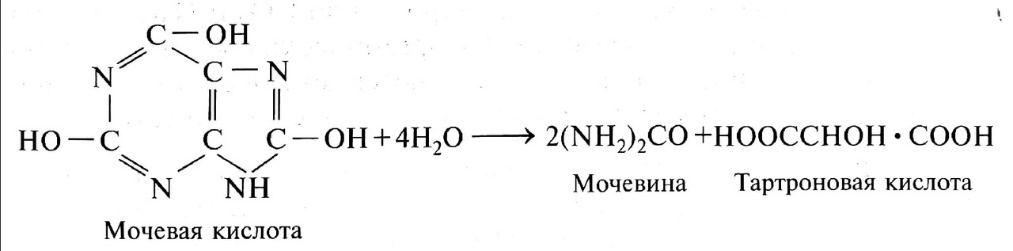
Условия, определяющие накопление аммиака в почве и навозе.
Количество азота зависит от типа почвы. В пахотном слое разных почв количество азота колеблется в широких пределах; в дерново-подзолистых, песчаных и супесчаных почвах – 0,04 – 0,08%, суглинистых и глинистых – 0,1– 0,15%. Серые лесные и черноземные почвы наиболее богаты общим азотом (0,3 – 0,5% и более). В каштановых почвах его количество колеблется от 0,1 (в светло-каштановых и бурых) до 0,2—0,25% (в темно-каштановых).
неисчерпаемым источником азота является атмосфера (среди прочих газов атмосферы на молекулярный азот приходится 78%. Однако молекулярный азот, будучи инертным газом, не может непосредственно усваиваться растениями.
Четвертая реакция процесса брожения — расщепление фруктозо- 1,6-бисфосфата и образование двух молекул фосфотриоз: фосфоди- гидроксиацетона (ФДА) и 3-фосфоглицеринового альдегида (3-ФГА). Фермент альдолаза (КФ 4.1.2.13) катализирует разрыв углеродной цепочки фруктозо-1,6-бисфосфата посередине, чему способствует
«Пусковой» реакцией катаболического распада глюкозы является ее фосфорилирование за счет АТФ с образованием глюкозо-6-фос- фата и АДФ, в результате чего молекула глюкозы активируется для участия в последующих превращениях. Катализирует реакцию фермент гексокиназа (КФ 2.7.1.1).
Затем образовавшийся глюкозо-6-фосфат (альдоза) превращается во фруктозо-6-фосфат (кетозу). Эта реакция происходит под воздействием фермента глюкозо-6-фосфат—изомеразы (КФ 5.3.1.9).
Третья реакция — фосфорилирование фруктозо-6-фосфата за счет АТФ с образованием фруктозо-1,6-бисфосфата и АДФ. Она катализируется ферментом фосфофрукгокиназой (КФ 2.7.1.11) и представляет собой еще одну «пусковую» реакцию брожения.
Четвертая реакция процесса брожения — расщепление фруктозо- 1,6-бисфосфата и образование двух молекул фосфотриоз: фосфоди- гидроксиацетона (ФДА) и 3-фосфоглицеринового альдегида (3-ФГА). Фермент альдолаза (КФ 4.1.2.13) катализирует разрыв углеродной цепочки фруктозо-1,6-бисфосфата посередине, чему способствует
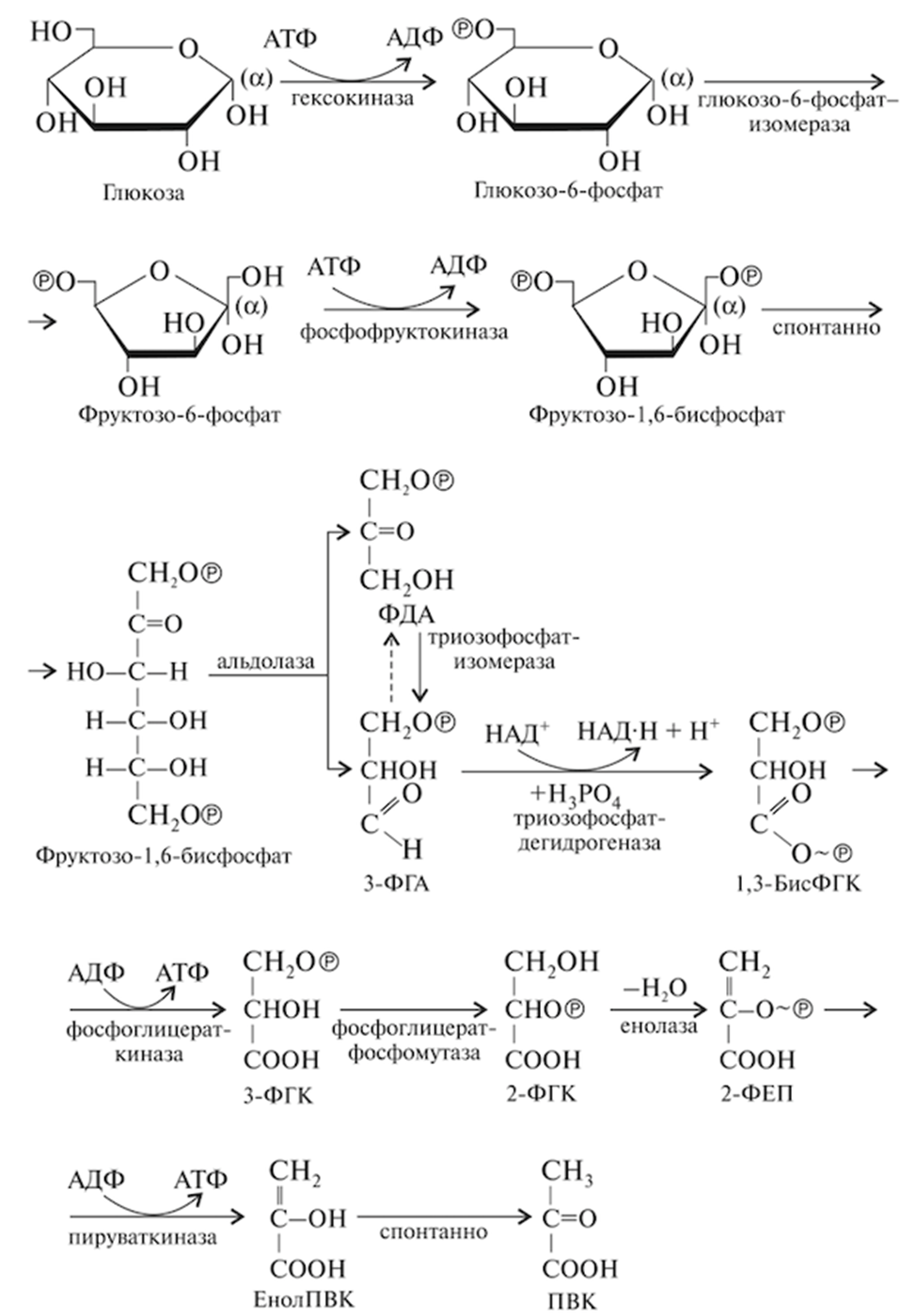
Энергетическая стадия брожения также включает пять реакций, в ходе которых энергия, содержащаяся в глюкозе, постепенно высвобождается и запасается в форме АТФ (рис. 61).
Она начинается с того, что 3-фосфоглицериновый альдегид под воздействием фермента триозофосфатдегидрогеназы (КФ 1.1.1.12) при участии фосфорной кислоты превращается в 1,3-бисфосфогли- цериновую кислоту (1,3-бисФГК). Энергия, высвобождающаяся в результате окисления альдегидной группы 3-фосфоглицеринового альдегида, аккумулируется в образуемой высокоэнергетической связи, с помощью которой присоединяется фосфатная группа.
Затем фермент фосфоглицераткиназа (КФ 2.7.2.3) катализирует перенос остатка фосфорной кислоты, содержащего высокоэнергетическую связь, от карбоксильной группы 1,3-бисфосфоглицерино- вой кислоты на АДФ с образованием АТФ и 3-фосфоглицериновой кислоты (3-ФГК).
В результате этой реакции энергия, ранее высвободившаяся при окислении альдегидной группы 3-фосфоглицеринового альдегида до карбоксильной, оказывается запасенной в виде АТФ.
После этого 3-фосфоглицериновая кислота под воздействием фермента фосфоглицерат-фосфомутазы (КФ 5.4.2.1) превращается в 2-фосфоглицериновую кислоту (2-ФГК).
Образовавшаяся 2-фосфоглицериновая кислота под воздействием фермента енолазы (КФ 4.2.1.11) превращается в 2-фосфоенолпиро- виноградную кислоту (2-ФЕП). При этом молекула 2-фосфоглице- риновой кислоты отдает молекулу воды. Это вызывает перераспределение энергии внутри молекулы субстрата, и связь, с помощью которой к нему присоединен остаток фосфорной кислоты, становится высокоэнергетической.
На последнем этапе энергетической стадии брожения 2-фосфо- енолпировиноградная кислота с помощью фермента пируваткиназы (КФ 2.7.1.40) передает содержащий высокоэнергетическую связь остаток фосфорной кислоты молекуле АДФ, в результате чего образуются АТФ и енолпировиноградная кислота (енолПВК). Последняя весьма нестойка и быстро неферментативным путем превращается в устойчивую кетоформу — пировиноградную кислоту (ПВК).
Таким образом, в ходе брожения молекула глюкозы расщепляется ферментативным путем в десяти последовательных реакциях до двух молекул пировиноградной кислоты и двух пар атомов водорода.
Образовавшаяся в результате реакций гликолиза пировиноград- ная кислота может подвергаться дальнейшим превращениям, направление которых зависит от условий среды (аэробных или анаэробных) и от специфических особенностей данного организма. В аэробных условиях она может окисляться до диоксида углерода и воды в процессе дыхания, а при анаэробной диссимиляции последующие превращения пировиноградной кислоты составляют завершающий этап брожения.
фиксация молекулярного азота и пополнение запасов его в почве осуществляется двумя путями: под влиянием грозовых разрядов и с помощью определенных микроорганизмов. Под действие электрических и фотохимических реакций при грозах образуются аммиак и окислы азота, которые поступают в почву с атмосферными осадками. По данным А.В.Петербургского, в осадках всегда больше аммонийного, чем нитратного азота, и общий приход его достигает в среднем около 4кг/га*год.
Гораздо большее значение в обогащении почв азотом имеет биологическая фиксация атмосферного азота свободноживущими микроорганизмами, сине-зелеными водорослями и клубеньковыми бактериями. Потенциальные возможности симбиотических и несимбиотических свободноживущих азотфиксаторов неравноценны. Свободноживущие азотфиксирующие микроорганизмы способны при благоприятных условиях ассимилировать 10-15 кг/га*год связанного азота. Клубеньковые бактерии поглощают значительно больше азота из атмосферы. По данным Д.Н.Прянишникова , ежегодно на 1 га люцерна накапливает 300(до 500-600), клевер 150-160 (до 250-300), люпин до 150, соя до 100, вика, горох- 50-60 кг азота. Количество фиксированного азота зависит от вида бобового растения Ph почвенного раствора, величины урожая. Наиболее активно азотфиксация осуществляется в фазу цветения бобовых культур.
Некоторое количество аммонийных удобрений, а также аммония, накапливающегося при минерализации органических соединений, закрепляется почвенными минералами
Потери азота из удобрений существенно уменьшаются при использовании гранулированных и медленно растворяющихся удобрений. К ним относятся уреаформ (конденсат мочевины с формальдегидом), гранулированная мочевина с оболочкой из элементарной серы, уреа-зет (конденсат мочевины с ацетальдегидом), изобутилен-диуреа и т. д.
Минеральные азотные удобрения позволяют быстро повышать урожаи, действуя практически в год внесения в почву. Под зерновые культуры в среднем вносят около 30 кг/га минеральных азотных удобрений в год
большое внимание уделять культурам бобовых растений, которые не только обогащают почву азотом, но и дают корм, богатый белком.
Содержание органического вещества в навозе составляет 20—25%; количество питательных для растений веществ ограничивается долями процента (0,5% азота, 0,2% Р2О5 , 0,6% К2О) и около 75% воды. Органическая часть навоза в расчете на беззольную сухую массу содержит до 40% перегнойных соединений, около 30% целлюлозы и лигниноподобных веществ.
Навоз, хранившийся плотным способом, содержит значительное количество аммиачного asoia, эффективность его гораздо выше, чем при других способах хранения
Потери азота при разложении навоза во время хранения значительно сокращаются при добавлении к нему (при укладке в штабеля) фосфоритной муки в количестве 3% массы навоза.
До 40% азота находится в навозе в виде гиппуровой и мочевой кислот, но большая часть — в виде мочевины. Последняя легко гидролизуется уробактериями и многими сапротрофными бактериями. При этом образуется углекислый аммоний, который легко диссоциирует на NH3 и СО2 .
При повышенной температуре распад мочевины и карбоната аммония усиливается, поэтому при горячем способе приготовления навоза потеря азота возрастает до 30%. Правильное приготовление навоза холодным способом резко снижает потери азота. Если вместо соломенной подстилки применяют торфяную, хорошо поглощающую аммиак, то потери снижаются до нескольких процентов
В бесподстилочном навозе значительная часть азота (40—60%) содержится в форме аммиака. Поэтому при его использовании целесообразно применять ингибиторы нитрификации.
В навозе много бактерий рода Pseudomonas, представителей группы кишечной палочки и других аммонификаторов, гнилостные спорообразующие бактерии — Bacillus subtilis, В. mesentericus, В. megateriит, В. mycoides и т. д., но при холодном способе приготовления эти виды размножаются слабо.