Материал: Металлокомплексный катализ
Металлокомплексный катализ
Ивановский
государственный химико-технологический университет
Доклад на тему:
«Металлокомплексный
катализ»
Подготовили:
студенты гр.4-11
Гончаренко А., Роднина Д.
Преподаватель:
Лефёдова О.В.
Иваново 2014
Металлокомплексный катализ
Большое значение координационные соединения приобрели в качестве катализаторов промышленно важных процессов. Запатентовано огромное число различных координационных соединений, катализирующих разнообразные реакции.
Координационные соединения способны активировать молекулы водорода, кислорода, оксида углерода (II), олефинов, ацетиленов и других соединений.
Перейдем к рассмотрению особенностей металлокомплексного катализа:
) Мягкие условия протекания процессов;
) Высокая избирательность и стереоселективность;
) Гомогенность процесса
) Центральные атомы - переходные металлы и металлы платиновой группы;
Лиганды - молекулы, имеющие вакантные орбитали (СО, олефины, фосфины и т.д.), которые могут взаимодействовать с заполненными орбиталями металла, образуя π-дативные связи.
История открытия и внедрения в промышленность
металлокомплексного катализа начинается в 1938 г., когда немецкий химик
О.Роелен открыл реакцию, позволяющую превращать олефины в кислородсодержащие
соединения. В качестве катализаторов использовались карбонильные соединения
переходных металлов. В первую очередь была изучена реакция с этиленом и
установлено, что она протекает по двум направлениям:
СН2= СН2 + СО + Н2 => СН3СН2СНО
В промышленности она получила название
«оксо-реакции». Однако впоследствии было установлено, что кетоны образуются не
из всех олефинов, и поэтому процесс чаще стали называть «гидроформилированием».
В общем виде его можно записать следующим образом:
RCH=CH2
+ CO + H2
→ RCH2CH2CHO
Наиболее распространенным катализатором данного процесса является HCo(CO)4 , но с успехом применяется и [Rh(PPh3)2(CO)Cl].
В начале 50-х годов в промышленном масштабе начал осуществляться процесс полимеризации этилена (а затем и пропилена) в мягких условиях на катализаторах, впервые предложенных Циглером. Они основаны на галогенидах и алкилгалогенидах металлов, например на TiCl3 и Al(C2H5)2Cl. Ранее в отсутствии этих катализаторов процесс осуществлялся при давлениях порядка 2000 атм (2 * 105 Па). Катализаторы циглеровского типа позволили снизить давление более чем в 100 раз. Не менее важно, что получающиеся при этих условиях полимеры имеют стереорегулярное строение, т.е. для них характерна значительно меньшая разветвленность макромолекул и высокая степень кристалличности. Стереорегулярность этих полимеров была установлена Натта. За основополагающие работы по каталитической полимеризации олефинов при низком давлении Циглер и Натта в 1963г. были удостоены Нобелевской премии.
Миллионы тонн уксусной кислоты в мире получают
путем каталитического карбонилирования метанола по реакции:
СН3ОН + СО → СН3СООН
Катализатором процесса служит комплекс [Rh(PPh3)2(CO)Cl], а промотором CH3I. Последний можно получать взаимодействием метанола с йодистоводородной кислотой.
Практически одновременно Шмидт и Хафнер в ФРГ ,
а Сыркин и Моисеев в СССР разработали каталитический способ промышленного
производства ацетальдегида из этилена. При пропускании этилена через водный
раствор, содержащий хлорид палладия (II),
идет реакция
C2H4 + PdCl2 + H2O → CH3COH +
Pd(0) + 2HCl
При наличии в растворе хлорида меди (II)
палладий регенерируется в соответствии с уравнением
Pd + 2CuCl2
=> PdCl2 + 2CuCl
Окисление меди проводят кислородом воздуха.
Синтез ацетальдегида осуществляют в одну операцию, пропуская смесь этилена и кислорода в реактор, содержащий хлориды палладия (II) и меди (II).
Помимо промышленных процессов металлокомплексный
катализ встречается во многих природных процессах. Примеры таких процессов
представлены в таблице.
Природные процессы:
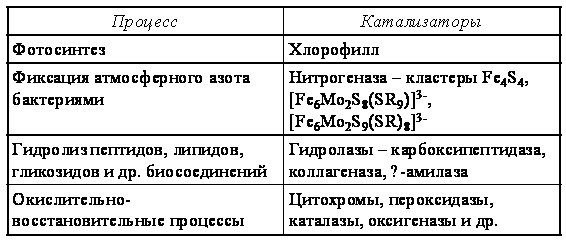
Технологические процессы:
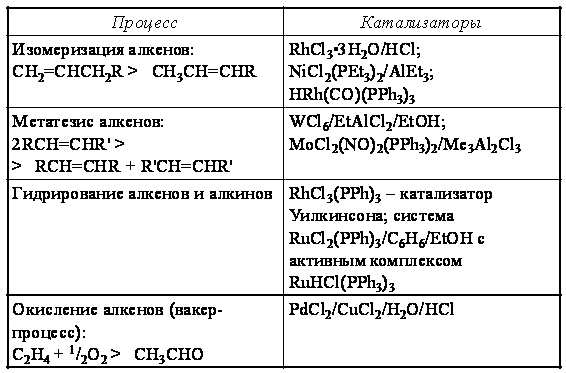
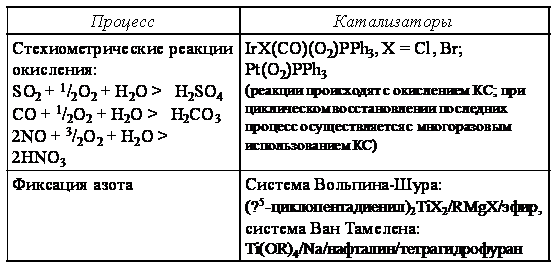

) Гетерогенизированный катализ;
) Гетерогенный катализ;
) Гомогенный катализ;
) Ферментативный катализ;
) Мицеллярный катализ;
) Фотокатализ;
) Электрокатализ;
) Биоэлектрокатализ;
) Фотоэлектрокатализ;
) Межфазный катализ.
Рассмотрим свойства комплексов металлов, определяющих каталитическую активность:
а) Координационная ненасыщенность центрального атома;
б) Способность координировать различные молекулы;
в) Активация лигандов.
Перейдем к изучению основных стадий,
встречающихся в металлокомплексном катализе:

Применение металлокомплексного катализа
металлокомплексный катализ ферментативный
1. Изучение строения природных металлоферментов и механизмов их каталитического действия, разработка искусственных синтетических моделей ферментов;
. Дизайн металлокомплексных катализаторов для решения проблем экологии и синтеза (в т.ч. крупнотоннажного) необходимых материалов;
Моделирование ферментативного катализа
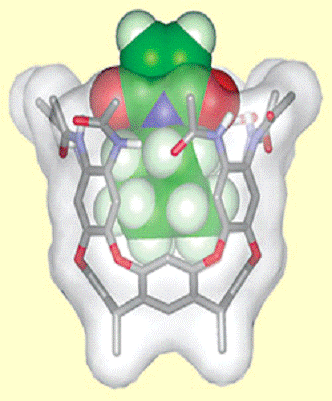
«Молекулярная ваза»: подражает работе фермента в том, что кавитанд обладает полостью, способной вместить лишь субстрат подходящего размера и формы. Функциональные группы, обеспечивающие водородное связывание по верхнему ободу кавитанда, активируют субстрат (ненасыщенный имид), оттягивая электронную плотность с кратных связей. Это обстоятельство увеличивает реакционную способность субстрата и увеличивает скорость участия его в реакции Дильса-Альдера с ароматическим спиртом. Размеры продукта не позволяют ему разместиться в полости, полость освобождается и может активировать очередную молекулу субстрата.
Как и любой метод, помимо неоценимых достоинств, металлокомплексный катализ имеет ряд недостатков:
|
Достоинства |
Недостатки |
|
Высокая активность |
Необходимость отделения катализатора от продуктов реакции |
|
Селективность |
Регенерация металлокомплексных катализаторов сложно осуществима |
|
Способность осуществлять каталитический процесс в мягких условиях |
Высокая стоимость составляющих катализатора |
|
|
Необходимость отделения катализатора от продуктов реакции |
Список использованной литературы
1. Химическая кинетика : учебное пособие / В. В. Буданов, О. В. Лефедова ; Иван. гос. хим.-технол. ун-т. - Иваново : ИГХТУ, 2011. - 176 с.
2. Химическая кинетика : учебное пособие / В. В. Буданов, Т. Н. Ломова, В. В. Рыбкин. - Санкт-Петербург [и др.] : Лань, 2014. - 283 с. : ил. ; 21 см.
. Координационная химия / В. В. Скопенко, А. Ю. Цивадзе, Л. И. Савранский, А. Д. Гарновский. - М. : Академкнига, 2007. - 487 с.