Материал: Контроль качества лекарственных средств с применением фотометрических методов анализа
Контроль качества лекарственных средств с применением фотометрических методов анализа
Контроль качества лекарственных
средств с применением фотометрических методов анализа
Содержание
Введение
1. Фотометрические методы в нормативной документации
2. Фотометрия в УФ области спектра
2.1 Качественный анализ
2.2 Количественный анализ
2.3 Оценка доброкачественности
3. Фотометрия в видимои области спектра
3.1 Типы реакций, применяемых в фотометрии
3.2 Экстракционная фотометрия
3.3 Испытание на подлинность
3.4 Количественное определение
3.5 Определение примесей
3.6 Определение светозащитных свойств упаковки
Выводы
Список литературы
Введение
Все химические соединения взаимодействуют с электромагнитным излучением, уменьшая интенсивность его потока. На измерении уменьшения интенсивности излучения, прошедшего через раствор анализируемого вещества основан фотометрический метод анализа. Эффективность его использования обусловлена рядом обстоятельств, важнейшими из которых являются [1]:
наличие разнообразных фотометрических методик анализа практически на все элементы периодической системы и многочисленные органические вещества;
возможность использования относительно недорогой и доступной аппаратуры;
возможность фотометрических определений соединений в интервале от 100 до 10-6 %, включая анализ веществ высокой степени очистки.
Специфичность, чувствительность, относительная простота и точность определений, достигаемая с помощью современной аппаратуры, обеспечивает широкое использование метода в различных областях науки и практики.
Фотометрический метод, в частности, успешно применяется для контроля качества лекарственных средств при их производстве и хранении [2].
Контроль качества лекарственного вещества включает три основных этапа: испытание на подлинность (идентификация), испытание на чистоту (определение примесей) и количественное определение фармакологически активного компонента.
Цель данной работы - исследование возможности применения фотометрического анализа в контроле качества лекарственных средств.
Задачи данной курсовой работы:
дать общую характеристику фотометрического метода;
проанализировать доступную периодическую литературу и интернет ресурсы (www.е-librаry.ru, www.sрringеr.соm, <#"879231.files/image001.gif">
Рисунок 1 - УФ-спектры поглощения преднизолона, кортизона и
гидрокортизона
2.2 Количественный анализ
Прямая фотометрия наиболее простой и широко применяемый метод,
пригодный для решения разных задач фармацевтического анализа, в частности для
оценки доброкачественности, количественное определение активных компонентов. За
последние годы разработано немало методик анализа лекарственных форм и
препаратов по их УФ спектрам поглощения [7, 8, 9]. Применение метода основано
на существовании прямо-пропорциональной зависимости величины поглощения от концентрации
вещества в анализируемом растворе: ![]() .
.
Различают несколько способов количественного анализа:
· графический по калибровочному графику;
· сравнительный относительно стандартного образца;
· расчетный по удельному показателю поглощения (Е1%1см).
Наиболее простой способ, применимый при неперекрывающихся спектрах, определение компонентов по собственному светопоглощению на предварительно выбранных аналитических длинах волн. Так анализируют препараты, содержащие одно активное вещество, например, анальгин [10], димедрол, пиридоксина гидрохлорид, новокаин [11, 12], папаверина гидрохлорид [13], пентоксифиллин [13], триметазидина дигидрохлорид, аспирин и многие другие соединения. Расчет концентраций обычно проводят с применением стандартных образцов [9-13].
Расчет количественного содержания индивидуального вещества в
процентах (Х) в субстанции проводят по формуле:
![]()
где А и Аст − оптическая плотность растворов исследуемого и государственного стандартного образца соответственно;
С − концентрация раствора стандартного образца, г/мл;
а − точная масса лекарственного вещества, г;
Главным достоинством спектрофотометрического анализа является его применимость для определения двух и более активных компонентов препаратов сложного состава без их предварительного разделения. В случае перекрывающихся спектров поглощения индивидуальных соединений используют метод Фирордта (МФ), включенный в Государственную фармакопею многих стран, в частности Американскую [14] и РФ [4, 15], реже метод вычитания оптической плотности. Метод Фирордта применен для нахождения концентраций кофеина и парацетамола при исследовании кинетики растворения твердых смесей указанных веществ [16]. Разработана методика количественного определения левомицетина и анестезина в присутствии суммы каротиноидов облепихового масла в препарате "Олазоль" [17], методика основана на применении модифицированного метода Фирордта. Разработаны методики определения по методу Фирордта двух активных компонентов в таблетках "Папазол›› [17], "Панадол-ЭКСТРА››, "Солпадеин›› и других лекарственных препаратах [17-18].
Точность методик, основанных на применении метода Фирордта, во многом зависит от правильного выбора аналитической длины волны.
При анализе многокомпонентных смесей ЛВ используется производная спектрофотометрия. Переход к регистрации "производных" спектров ведет к значительному повышению селективности за счет улучшения разрешения отдельных полос и снижения влияния фона.
Для нахождения концентраций лекарственных веществ в последние годы стали использовать данные совокупных измерений оптической плотности анализируемой смеси в широком диапазоне длин волн. Обработку полученных результатов в таких случаях проводят с применением различных вариантов регрессионного анализа. Нахождение концентраций в рамках классического линейного множественного регрессионного анализа требует решения переопределенной системы уравнений, как правило, методом наименьших квадратов Известно, что МНК позволяет получать линейные относительно оптической плотности оценки концентраций с минимальной дисперсией, если погрешности определения коэффициентов поглощения пренебрежимо малы, а погрешности измерений аналитического сигнала случайны. Используют разные варианты МНК: модифицированный метод наименьших квадратов (ММНК), метод частичных наименьших квадратов (ЧМНК) и др. Так, предложена простая и экспрессная методика одновременного определения пирамидона и кофеина с использованием многоволновой линейной регрессии.
Часто в методе УФ фотометрии совмещают качественный и количественный анализ, так, например, при анализе примидона С14Н14N2О2, снимают спектр тестируемого ЛВ в области от 240 до 270 нм относительно "слепой" пробы - спирта [20].
Снимают спектр стандартного раствора примидона, взятого в концентрации 400 мкг/мл, в области от 240 до 270 нм относительно "слепой" пробы - спирта.
Расчет количества С14Н14N2О2
в мг в тестируемом препарате проводят по формуле:
Сх = 0,1 Сst (2D257 - D254 -
D261) x / (2D257 - D254 - D261)
st,
Где Сst - концентрация примидона в стандартном растворе, выраженная в мкг/мл, Сх - концентрация примидона в тестируемом растворе в мг/мл, D - значения абсобции двух образцов при различных длинах волн 254, 257, 261 нм.
Значение абсорбции примидона при разных длинах волн берут из
прилагаемых спектров. Полученную концентрацию тестируемого примидона,
выраженную в мг, сравнивают со стандартом (40 мг). Учитывая данные о содержании
С14Н14N2О2 в примидоне, делают
вывод о качестве препарата.
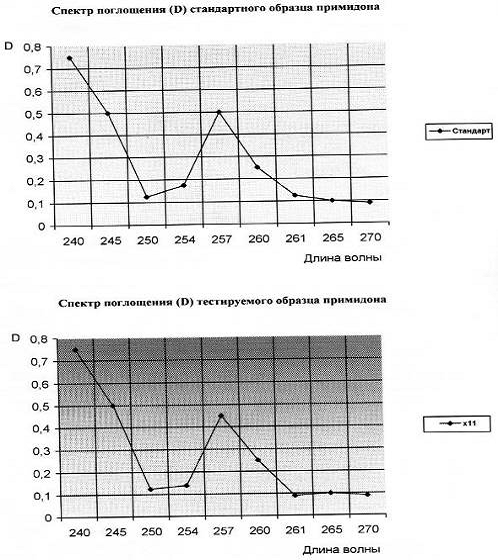
Риснок 2 - Спектры поглощения примидона
2.3 Оценка доброкачественности
УФ-спектрофотометрия применяется и для определения
специфических примесей в лекарственных веществах [21]. Например, л mаx
растворов адреналина находится при 278 нм, а его специфическая токсичная
примесь адреналон имеет максимум поглощения при длине волны 310 нм.
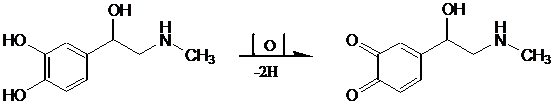
Адреналин Адренолон
Согласно ФС, оптическая плотность 0,05 % раствора адреналина при
310 нм не должна превышать 0,1 (т.е. в адреналине допускается незначительное
строго нормируемое содержание адреналона).
3. Фотометрия в видимои области спектра
Большинство лекарственных веществ не поглощает в видимой области спектра, поэтому для перевода их в окрашенные соединения необходимо проводить соответствующие фотометрические реакции. Методики такого типа известны довольно давно и широко применяются в фармакопейном анализе [22, 23, 1, 2]. Они являются более трудоемкими, чем методики, основанные на измерении собственного поглощения лекарственных веществ в УФ области спектра. Методики определения лекарственных веществ по светопоглощению в видимой области обычно основаны на образовании окрашенных комплексов со специально добавленным реагентом. Реже используется окисление лекарственного вещества или его превращение в новую форму под воздействием облучения [24-25].
3.1 Типы реакций, применяемых в фотометрии
1. Получение ацисолей с NаОН
фурацилин, фуразолидон, левомицитин, нитроксолин.
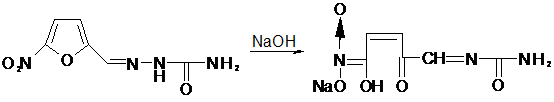 оfurаl (Фурацилин, 5 - нитрофурфурола семикарбазон) желтая -
желто-зеленая окраска [25]
оfurаl (Фурацилин, 5 - нитрофурфурола семикарбазон) желтая -
желто-зеленая окраска [25]
2. Диазотирование с последующим азосочетанием для
препаратов, содержащих первичную ароматическую группу (анестезин, новокаин,
сульфамиламид)
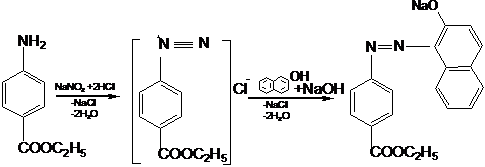 еnzосаinе, Этиловый эфир п-аминобензойной кислоты
еnzосаinе, Этиловый эфир п-аминобензойной кислоты
3. Получение гидроксаматов меди и железа для препаратов,
содержащих сложноэфирную (новокаин), лактонную (пилокарпин), лактамную
(бензилпенициллина К - и Nа - соли) группы.
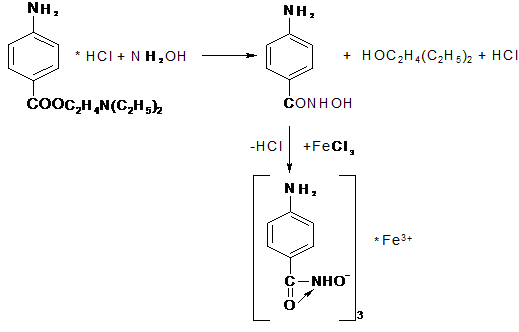
Рrосаinе Hydrосhlоridе, Новокаин, β-диэтиламиноэтилового эфира
n-аминобензойной кислоты гидрохлорид
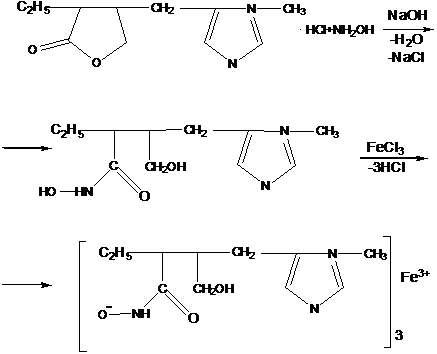
Рilосаrрinе Hydrосhlоridе
4. Окисление калия перманганатом и определение продуктов
реакции после реакции диазотирования с последующим азосочетанием с
N-1-нафтилэтилендиамином дихлоридом.



6. Конденсация с n-диметиламинобензальдегидом
(новокаин), 2,4 - динитрофенилгидразином (цитраль):
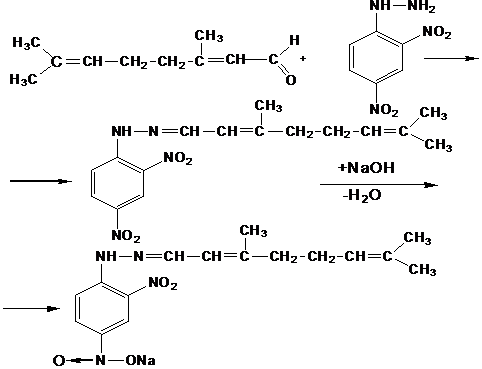
Если полученное окрашенное соединение нерастворимо в воде, его извлекают органическим растворителем, несмешивающимся с водой (хлороформ, эфир и др.) и определяют оптическую плотность извлечения. Это вариант экстракционной фотометрии [26].
Требования, предъявляемые к реакциям:
· продукт реакции образует устойчивую окраску и имеет постоянный состав;
· реакция должна быть стехиометричной;
· реакция протекает быстро;
· высокая избирательность и чувствительность реакции;
· реагенты должны быть доступны, безвредны и экономичны.
3.2 Экстракционная фотометрия
Методом экстракционной фотометрии проводится определение следующих веществ:
производных барбитуровой кислоты
эфедрина
солей органических азотсодержащих оснований
алкалоидов по реакции с кислотными индикаторами
(бромтимоловый синий, пикриновая кислота, тропеолин 00 и др.) с образованием
ионных ассоциатов [27].
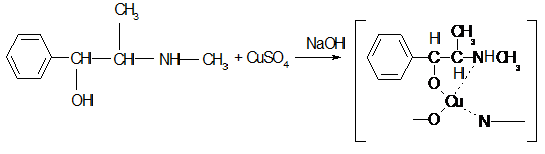
Ерhеdrinе Hydrосhlоridе, 1-эритро-2-метиламино-1-фенилпропанола-1
гидрохлорид. Эфир - краснофиолетовый цвет, H2О - синий.
В дифференциальном варианте фотометрии измерение светопоглощения проводится относительно раствора сравнения, содержащего определенное количество анализируемого вещества. В связи с этим дифференциальная фотометрия позволяет повысить точность фотометрических измерений при определении высоких концентраций (10 - 100%) и уменьшить относительную ошибку анализа до 0,5 - 1,0%.
3.3 Испытание на подлинность
Приведем примеры. В видимой области проводят идетификацию тетрациклинов, поглощающих при изомеризации в кислой среде [3-5]:
. Аλ (Dотн.) (0,01% тетрациклина в 0,01М HСl), А380нм=0,36-0,38 (прямая фотометрия.
2. По показателю удельного коэффициента поглощения![]() при определенной длине волны λ
- (цианокобаламин при 550 нм
при определенной длине волны λ
- (цианокобаламин при 550 нм ![]() =61,5-66,5)
=61,5-66,5)
. По отношению оптических плотностей при разных длинах волн,
например, для растворов цианокоболамина: ![]()
3.4 Количественное определение
Количественное определение в фармакопейном анализе с использованием фотометрии проводится несколькими способами [1-5]:
. По калибровочному графику: у = аx + b
Концентрация вещества в лекарственной форме
![]() ,
,
где
СX - масса вещества по калибровочному графику (г);
Р - средняя масса лекарственной формы (г);- объем раствора лекарственной формы (мл);
а - навеска лекарственной формы, взятая для анализа (г).
2. Расчет по стандарту (ГСО, РСО, СОВС):
концентрация в индивидуальном веществе
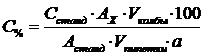
где
Р - средняя масса лекарственной формы (г);- объем лекарственной формы (мл).
. Расчет по молярному коэффициенту поглощения - ε
или ![]()
![]() или
или ![]()
концентрация в индивидуальном веществе:
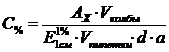
3.5 Определение примесей
Отметим, что спектрофотометрический метод используют не только для определения активных лекарственных веществ, но и для определения нежелательных примесей. При наличии примесей могут изменяться максимумы их интенсивность, появляться дополнительные максимумы поглощения,.
С целью обнаружения примесей используют те же характеристики, что и при испытаниях на подлинность, т.е. величины отношений оптических плотностей при различных максимумах и значение удельных показателей поглощения.
При хранении некоторые препараты могут частично окисляться с появлением окраски, интенсивность которой контролируется величиной оптической плотности приготовленного раствора при определенной длине волны.
Например, при определении цветности 16 % водного раствора
метамизола (анальгина) измеряют его оптическую плотность при 400 нм, которая не
должна быть более 0,10 (НД 42-4593-95). При определении цветности 10 % водного
раствора ампициллина натриевой соли измеряют его оптическую плотность при длине
волны 430 нм; она не должна превышать 0,15 (ФС 42-3535-98) [1-5].
3.6 Определение светозащитных свойств упаковки
Одним из важнейших защитных свойств упаковки является свойство задерживать световой поток [28]. Известно, что ультрафиолетовый и видимый свет являются причиной фотодеструкции и других изменений лекарственных средств. Государственная фармакопея XI и другая нормативно-техническая документация предусматривает хранение большой группы ЛС в упаковке из оранжевого стекла и защищенном от света месте.