Материал: Клеточные технологии
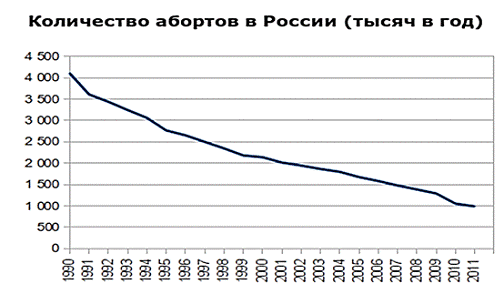
Рисунок 3
Источником стволовых клеток может быть слизистая оболочка носоглотки. В ней преобладают частично специализировавшиеся стволовые клетки, способные превращаться в клетки нервной ткани - нейроны и клетки глии. Эти клетки пригодны для лечения заболеваний головного и спинного мозга. Однако, применяемость этих клеток для замены иных, чем нервные, требует дальнейших исследований. Помимо этого, выделение и хранение данного материала достаточно трудоемки.
Мезенхимальные стволовые клетки содержатся в жировой, хрящевой, мышечной тканях. В настоящее время весьма перспективным является выделение этих клеток из жировой ткани, полученной при липосакции.
И, наконец, еще одним источником стволовых клеток является бластоциста, которая формируется к 5-6 дню оплодотворения. Это эмбриональные стволовые клетки. Они наиболее универсальны, по сравнению со стволовыми клетками взрослых людей, и способны дифференцироваться абсолютно во все типы клеток организма. Положительной стороной использования этих универсальных стволовых клеток следует считать тот факт, что в них отсутствует штампик «моё»: клетки как бы никому не принадлежат и не выполняют никаких специальных функций, а потому при введении не возникает реакция отторжения. Даже, если эмбриональные стволовые клетки взяты от другого организма, они не отторгаются, поскольку на их поверхности еще нет антигенов гистосовместимости.
. Применение клеточных технологий в XXI веке
Наиболее продвинутым в настоящее время является применение клеточных технологий в кардиологии для лечения инфаркта миокарда и восстановления кровотока в ишимизированных органах и тканях, повышения насосной функции сердца, а также лечения дислипидемий и атеросклероза.
В неврологии трансплантационные клеточные технологии начали применять для лечения болезни Паркинсона и болезни Хантингтона. Результаты первых испытаний по применению стволовых клеток при болезни Паркинсона были опубликованы в 2009 году. Согласно полученным данным, через 36 месяцев после введения стволовых клеток положительный эффект отмечен у 80% больных. Лечение заключается в трансплантации нейронов, полученных в результате дифференцировки стволовых клеток, в головной мозг. Теоретически они должны заменить погибшие дофаминсекретирующие клетки. В 2003 году впервые человеку с болезнью Паркинсона в субталамическое ядро были введены генетические векторы, содержащие ген, ответственный за синтез глутаматдекарбоксилазы. Данный фермент снижает активность субталамического ядра. Вследствие этого он оказывает положительное терапевтическое воздействие. Несмотря на полученные хорошие результаты лечения, на первую половину 2011 года методика практически не применяется и находится в стадии клинических исследований.
В связи с выявленной противоопухолевой активностью низкодифференцированных кроветворных клеток и их способностью прямо супрессировать опухолевый рост начаты исследования и клинические применения клеток предшественников в онкологии. Клеточные технологии в борьбе против онкологии вышли на тот уровень, на котором возможно использование собственных антител организма для борьбы с опухолевым заболеванием. Алгоритм выглядит достаточно просто: из вены больного берётся кровь; из препарата крови изымаются иммунные клетки, которые клонируются; клонированные клетки активизируют в инкубаторе-биореакторе. Затем активированные клетки снова внедряются в организм. Они начинают разрушать раковую опухоль изнутри. Это пока единственный работающий метод.
Значительное применение нашли данные технологии в области травматологии и ортопедии. Имеются сообщения о положительном применении стволовых клеток костного мозга для заживления ожоговых и глубоких кожных ран, лечения системных и местных костных дефектов. Например, традиционные методы лечения переломов заключаются в наложении фиксации гипсом. Доктора сопоставляют костные отломки и далее фиксируют эти участки, предоставляя возможность организму восстанавливаться. Существуют определенные периоды восстановительных процессов. Однако данные процессы могут длиться чрезмерно длительно. В этом плане клеточные технологии намного эффективнее, так как помимо совмещения костных отростков медики выполняют транспортировку клеточного материала к локализации сращения. В итоге процессы продолжают протекать в норме, но организм получает положительное содействие к оздоровлению и регенерация выполняется быстрее. Костная мозоль образуется прочной, а период регенерации уменьшается вдвое или более. Внутрисуставный перелом обладает существенной трудностью лечения. Более того, он влечет возникновение остеоартроза, который до недавнего периода времени считался неизлечимым. Восстановительные процессы в подобных хрящах значительно замедлены. Без дополнительных воздействий хрящи могут полностью не восстановиться, а болевой синдром продолжится и после сращения костей. Тем не менее, использование клеточных технологий предоставляет благоприятные перспективы. Специалисты используют малое количество подкожно-жировой ткани пациента, из которой биотехнологии выделяют специализированные стволовые клетки и выращивают прехондроциты клеток хряща. Хрящевые клетки транспортируются в поврежденный сустав. Таким образом, выполняется восстановление недостающей хрящевой массы. Клеточные технологии применяются и в области спортивной медицины для пациентов, которые активно занимаются разнообразными спортивными дисциплинами. Использование стволовых клеток позволяет восстанавливать и укреплять сухожилия и суставы. Причем тут следует отметить не только лечение после спортивной карьеры и накопившихся микротравм, которые дают осложнения с возрастом, но и возможность эффективной профилактики по укреплению разнообразных тканей и частей тела.
При этом необходимо учитывать моральные, нравственные и правовые аспекты данной проблемы. Различают срочную (аварийную) и плановую (системную) терапию СК. В первом случае решают вопросы, связанные с купированием остро развившегося критического состояния в тканях на фоне дефицита или полного отсутствия СК, например, при инсультах и инфарктах. Обычно при этих заболеваниях, несмотря на наличие всех необходимых компонентов (ростовых факторов, цитокинов и др.) и вспомогательных клеток (лимфоцитов, макрофагов, эндотелия и т.п.), невозможно восстановить исходную ткань из-за отсутствия специализированных СК. В результате развиваются необратимые изменения, заканчивающиеся образованием рубцовой ткани и нарушением функции органа. Трансплантация СК таким пациентам, как показали первые наблюдения, способствует реконструкции исходной ткани на 40-70 %. Второй подход направлен на использование СК при восстановлении функции ткани, которая находится в стадии истощения или декомпенсации. При этом (в зависимости от тяжести состояния) сначала стимулируют регенерацию поврежденной ткани. Следует помнить, что если нарушено специфическое микроокружение органа, то начинают поэтапно осуществлять его восстановление, а затем трансплантируют СК. Если имеются глубокие системные повреждения, то необходимо избрать другую тактику и последовательно реконструировать иммунную, кроветворную, нейроэндокринную и другие системы макроорганизма. Обычно количество вводимых клеток не превышает 0,1-0,01% от общей массы ткани, которую необходимо восстановить. Теоретически введение 1×106 СК с учетом 50% их гибели способно реконструировать от 1 до 10 г специализированных клеток поврежденной ткани. Анализ литературных данных позволяет предположить, что ССК обладают способностью к хомингу в соответствующую их дифференцировочным потенциям ткань. Ряд специалистов считают, что предпочтительнее использовать ССК.
При этом существенно снижается риск возникновения злокачественных и доброкачественных новообразований. Многие вопросы, связанные с использованием СК, ССК и их аналогов, полученных генно-инженерными методами, в клинической практике уже решены. Так, разработаны технологии выделения, наработки, хранения и клинического использования данных клеток при лечении разнообразных заболеваний. Однако ряд проблем остается на уровне теоретических разработок или экспериментов. Необходимо проведение серьезных фундаментальных исследований в данной области медицины в рамках программ по развитию высоких технологий в России. Выявленные закономерности станут основой для разработки оптимальных подходов для проведения клеточной хирургии. После всесторонних доклинических и клинических испытаний необходимо выработать адекватные протоколы (СТО) для конкретной ткани с последующим контролем качества материала, всех технологий, включая клиническое применение. Деятельность лаборатории и клиники должна быть соответствующим образом лицензирована, а продукты и технологии - сертифицированы в установленном порядке.
Однако следует помнить, что клеточная терапия с использованием СК и ССК не является панацеей от всех болезней и имеет строгие противопоказания. Применение донорского материала всегда несет потенциальный риск переноса скрытых инфекций, патогенных генов и возникновения РТПХ. Образующиеся химеры могут быть структурно и функционально неполноценными и приобретать новые, пока еще мало изученные свойства. В частности, при реконструкции нервной ткани существует риск нарушения работы мозга и его высшей психической деятельности. В связи с этим данный метод занимает особое положение среди других манипуляций. Его использование должно осуществляться по строгим показаниям, когда другие технологии бессильны спасти жизнь пациента, с учетом правовых, этических и иных аспектов.
.
Клеточные технологии для лечения инфаркта миокрада
В мире много
болезней, но лишь немногие из них приводят к летальному исходу. Конечно, все
болезни требуют внимания и интенсивного лечения, но я думаю, что именно
смертельные болезни требуют особого внимания и внедрения в их лечение
инновационных технологий. Как видно из диаграммы, большая часть населения в
России погибает от сердечно-сосудистых заболеваний, поэтому я решила
поподробнее рассмотреть, как клеточные технологии могут помочь в лечении этих
заболеваний, а именно в лечении самого распространенного сердечно-сосудистого
заболевания, инфаркта миокарда. [16]
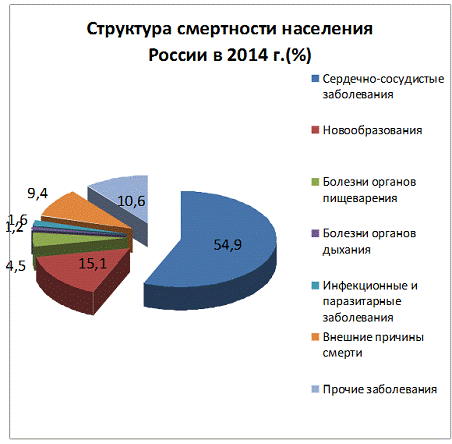
Рисунок 4
Инфаркт миокарда давно стал бичом современно высокотехнологичного общества. Вредные привычки в виде курения и алкоголя, гиподинамия, неправильное питание с высоким содержанием жиров и холестерина, гиподинамия и стрессы - все эти факторы ведут к постоянному росту числа инфарктов во многих странах мира. При том более 11% госпитализаций по поводу инфаркта приходятся на повторные случаи заболевания. При этом в лечении этого заболевания продолжают использоваться устаревшие методы лечения.
Суть инфаркта - нарушение кровоснабжения определенного участка сердечной мышцы и ее гибель. Причиной такого нарушения является обычно атеросклеротическая бляшка или тромб. При инфаркте миокарда ткань сердца просто не успевает так быстро приспособиться к резкому снижению кровотока, так как сердце должно постоянно работать, ведь его остановка ведет к гибели. В итоге, при отсутствии тока крови на определенном участке ткани сердца возникает некроз - это и есть инфаркт. Основными симптомами инфаркта миокарда являются сильная загрудинная боль, которая длится более получаса и не купируется приемом нитроглицерина. Кроме того, в атипичных случаях инфаркта миокарда боль может отмечаться в животе, может также отмечаться головная боль.
В диагностике инфаркта миокарда на сегодняшний день ведущую роль играет ЭКГ, а также некоторые лабораторные методы - анализ крови и тропониновый тест. Лечение инфаркта миокарда направлено, прежде всего, на восстановление кровотока в закупоренной коронарной артерии. Для этого обычно с первых же часов вводятся различные антикоагулянты, тромболитические препараты, цель которых - растворить тромб. В случае возможности, проводится экстренная операция - ангиопластика и стентирование суженной коронарной артерии. То есть, под местной анестезией через бедренную артерию пациенту вводится тонкий катетер, на конце которого раздувающийся баллончик и сам стент. К слову сказать, такой метод лечения инфаркта миокарда является идеальным, но применим далеко не в каждом городе России.
Обычно после инфаркта миокарда в ткани сердца остается рубец, так как некротическая ткань постепенно замещается фиброзной. Этот участок сердца уже никогда не будет нормально сокращаться, в результате чего сердце работает хуже, возникает сердечная недостаточность. Появляется одышка ввиду застоя крови в малом кругу кровообращения. На ногах к концу дня появляются отеки. Все это, как уже говорилось, связано со слабостью работы сердца. Обычно при сердечной недостаточности пациент бывает вынужден принимать целый спектр препаратов - сердечные гликозиды, диуретики дня снятия отеков, антилипидные препараты, антиагреганты для профилактики инфаркта, различные метаболическте препараты и т.д. В некоторых случаях в участке стенки сердца, где имеется рубец после инфаркта, может возникнуть аневризма - мешотчатое выпячивание.
Стволовые клетки сегодня являются весьма новым методом лечения многих заболеваний, в том числе и заболеваний сердца. Стволовые клетки обладают способностью образовывать разные ткани, то в случае инфаркта нужно заставить их как бы восстановить те элементы, из которых состоит сердце. Технология такова. В ближайшие неделю-полторы после инфаркта берутся собственные костномозговые клетки и вводятся в коронарную артерию. А дальше они проникают в ткань сердца и начинают делать то, что нужно для нормальной работы сердечной мышцы. При этом, данный метод все еще находится на стадии исследований, но он уже успешно применяется во многих зарубежных клиниках. За последние несколько лет в Европе таким образом было вылечено более 200 человек.
Для лечения инфаркта миокарда применяются гематопоэтические стволовые клетки, то есть, они берутся из костного мозга. Совсем недавно ученые из США и Канады выяснили, что для лечения инфаркта миокарда следует брать стволовые клетки не от самого больного человека, а от здорового донора. Этот факт был подтвержден на многочисленных экспериментах на животных. Восстановительный процесс в сердечной ткани после введения стволовых клеток в нее определяется уже через два месяца после начала лечения инфаркта миокарда.
Лечение инфаркта миокарда стволовыми клетками имеет ряд уникальных особенностей. Прежде всего - лечение инфаркта миокарда стволовыми клетками способствует восстановлению здоровой ткани сердца, и замену ею рубца. Это обеспечивает правильную работу сердца, устраняет, прежде всего, явления сердечной недостаточности, нормализует работу всех органов, систем, и устраняет последствия инфаркта миокарда - отеки на ногах, одышку и т.д.
Процедура лечения инфаркта миокарда стволовыми клетками состоит из трёх этапов.
На первом этапе лечения проводится забор стволовых клеток. В настоящее время для лечения инфаркта миокарда стволовые клетки берут из костного мозга. Хватает малого количества стволовых клеток пациента. После этого полученные стволовые клетки тщательно изучаются лабораторных условиях. Врачи проводят строгий отбор стволовых клеток, в ходе которого выбираются самые жизнеспособные клетки. Затем в течение 45-60 дней стволовые клетки культивируют для получения клеточной массы. В ходе этого процесса популяция стволовых клеток вырастает до 200000000. При этом часть стволовых клеток в процессе дифференцировки превращаются в клетки сердечной мышца. Введенные кардиомиобласты полностью восполняют собой все поврежденные клетки сердечной ткани.
На первом этапе часть стволовых клеток пациента помещается на хранение в банк клеток. Обычно эти стволовые клетки помещают в персонализированный контейнер, в таком количестве, чтобы их можно было использовать для проведения процедуры клеточной терапии. Это позволит пациенту или его ближайшим родственникам воспользоваться ими, минуя первый этап.
На втором этапе терапии стволовыми клетками проводится их трансплантация пациенту. Обычно, клетки вводятся внутривенно. При этом обязательно их повторное введение через полгода. Само введение стволовых клеток не требует госпитализации пациента и проходит амбулаторно. Через несколько часов после введения стволовых клеток пациент может вернуться к своей привычной жизни. С этого момента начинается обновление сердечной ткани. Трансплантируемые стволовые клетки, током крови попадают к сердцу, где прикрепляются к неповрежденным участкам миокарда и начинают замену поврежденных клеток на здоровые.
Результатами лечения инфаркта с помощью клеточной терапии, становится полностью восстановленная мышца сердца, свободная от рубца и способная сокращаться самостоятельно, поддерживая правильный сердечный ритм. Кроме того, стволовые клетки, являясь первоисточником для других клеток сердца, способствуют росту новой сети коллатеральных кровеносных сосудов, в обход пораженных бляшками коронарных артерий.