Материал: Физико-химические методы исследования природных вод
Жесткость воды обусловливается присутствием в воде ионов кальция (Са2+) и магния (Мд2+). В бутылку с образцом воды добавляют немного мыльного раствора и взбалтывают ее. Если вода жесткая, то пена почти не образуется, а в мягкой воде ее будет много. Можно опросным методом выяснить много ли накипи образуется в чайниках, что свидетельствует о повышенной жесткости воды. Принято различать воду по жесткости на очень мягкую, мягкую, умеренно жесткую, жесткую и очень жесткую.
Присутствие железа можно определить в камеральных условиях по потемнению настоя чая или листьев брусники, по окрашиванию в синий цвет раствора желтой кровяной соли, по почернению раствора танина.
Присутствие нефтепродуктов в воде обнаруживается в
полевых условиях визуально по радужным пятнам и серым пленкам на поверхности
воды, по вымазанным нефтью берегам водоемов, по пленкам нефти на прибрежных
растениях. Для определения присутствия продуктов нефти в камеральных условиях
пробу воды наносят на фильтровальную бумагу или подкисляют ее слабым раствором
перманганата калия. Если в образце присутствуют нефтепродукты, то после
высыхания нанесенной пробы на фильтровальной бумаге остаются масляные пятна, а
розовый раствор «марганцовки» обесцвечивается.
1.2.3 Химические показатели воды
Водородный показатель ( рН).
Питьевая вода должна иметь нейтральную реакцию (рН около 7). Величина рН воды водоемов хозяйственного, питьевого, культурно-бытового назначения регламентируется в пределах 6,5 - 8,5. В большинстве природных вод водородный показатель соответствует этому значению и зависит от соотношения концентраций свободного диоксида углерода и гидрокарбонат-иона. Более низкие значения рН могут наблюдаться в кислых болотных водах за счет повышенного содержания гуминовых и фульвокислот. Летом при интенсивном фотосинтезе рН может повышаться до 9. На величину рН влияет содержание карбонатов, гидроксидов, солей, подверженных гидролизу, гуминовых веществ и др. В результате происходящих в воде химических и биологических процессов и потерь углекислоты рН воды может быстро изменяться, поэтому его следует определять сразу же после отбора пробы, желательно на водоеме.
Оценивать величину рН можно разными способами.
.Приближенное значение рН. В пробирку наливают 5 мл исследуемой воды, 0,1 мл универсального индикатора, перемешивают и по окраске раствора оценивают величину рН:
розово-оранжевая - рН около 5,
светло-желтая - 6,
светло-зеленая - 7,
зеленовато-голубая - 8.
.рН можно определить с помощью универсальной индикаторной бумаги, сравнивая ее окраску со шкалой.
. Наиболее точно значение рН можно определить на рН-метре или по шкале набора Алямовского.
Сухой остаток.
Сухим остатком называют остаток, полученный после выпаривания отфильтрованной пробы воды и высушенный до постоянной массы при ПО- 120 "С. Сухой остаток характеризует содержание минеральных и частично органических примесей, образующих с водой истинные и коллоидные растворы.
Жесткость воды. Различают общую, временную и постоянную жесткость воды. Общая жесткость обусловлена, главным образом, присутствием растворенных соединений кальция и магния в воде. Временная жесткость иначе называется устранимой или карбонатной. Она обусловлена наличием гидрокарбонатов кальция и магния. Постоянная (некарбонатная) жесткость вызвана присутствием других растворимых солей кальция и магния. Общая жесткость варьирует в широких пределах в зависимости от типа пород и почв, слагающих бассейн водосбора, а также от сезона года. Величина общей жесткости в источниках централизованного водоснабжения допускается до 7 ммоль экв/л, в отдельных случаях по согласованию с органами санитарно-эпидемиологической службы - до 10 ммоль экв/л.
При жесткости до 4 ммоль экв/л вода считается мягкой;
- 8 ммоль экв/л- средней жесткости;
-12 ммоль экв/л - жесткой;
более 12 ммоль экв/л - очень жесткой.
Методами химического анализа обычно определяют общую
жесткость (![]() ) и карбонатную (
) и карбонатную (![]() ), а некарбонатная (Жн)
рассчитывается как разность
), а некарбонатная (Жн)
рассчитывается как разность ![]() -
- ![]() .
.
Окисляемость - общее количество содержащихся в воде восстановителей (неорганических и органических) , реагирующих с сильными окислителями (например, дихроматом, перманганатом и др.). Результаты определения окисляемости одной и той же воды с помощью различных окислителей обычно неоднозначны из-за неодинаковой степени окисления веществ, присутствующих в воде. Это зависит от свойств окислителя, его концентрации, температуры, рН воды и т. п. Вместо термина «окисляемость» часто используется термин «потребление кислорода». Все методы определения окисляемости условны, а получаемые результаты сравнимы только в том случае, когда точно соблюдаются все условия проведения анализа. Результаты определения окисляемости приводят в миллиграммах кислорода на 1 л воды (мг кислорода/л). Наиболее полное окисление достигается дихроматом калия, поэтому дихроматную окисляемость нередко называют «химическим потреблением кислорода» (ХПК). Это основной способ определения окисляемости. Большинство соединений окисляется при этом на 95 - 100%. Нормативы ХПК воды водоемов хозяйственно-питьевого водопользования- 15 мг кислорода/л, культурно-бытового - 30 мг кислорода /л. Дихроматный метод недоступен для школ из-за отсутствия соответствующих реактивов. Более доступным является перманганатный метод (метод Кубеля). Перманганат как окислитель может окислять как в кислой, так и в щелочной средах. При малом содержании хлоридов окисление ведут в кислой среде, при повышенном (более 300 мг/л хлорид-ионов) - в щелочной.
Биохимическое потребление кислорода (БПК) - это количество кислорода (мг), требуемое для окисления находящихся в 1 л воды органических веществ в аэробных условиях при 20 "С в результате протекающих в воде биохимических процессов за определенный период времени (ВПК за 3, 5, 10, 20 суток и т. д.). В аналитической практике чаще всего определяют 5-суточное БПК5 (установлено, что БПК5 составляет 70% БПК полного). Величина полного ВПК регламентируется в зависимости от категории водоема: не более 3 мг кислорода/л для водоемов хозяйственно-питьевого водопользования и не более 6 мг кислорода/л для водоемов хозяйственно-бытового и культурного водопользования. Среди различных методов установления БПК наиболее распространено определение по разности содержания растворенного кислорода до и после инкубации при стандартных условиях (20 °С, аэробные условия без дополнительного доступа воздуха и света). В величину ВПК не входит расход кислорода на нитрификацию. Для подавления этого процесса в пробу воды можно ввести вещества, ингибирующие нитрифицирующие микроорганизмы и не влияющие на микроорганизмы, осуществляющие основные биохимические процессы (например, этилентиокарбомид), из расчета 1 мл 0,05 % раствора на 1 л исследуемой воды.[ 1 ]
физический химический природный вода
. Объект исследования
.1 Озеро «Яльчик»
Озеро «Яльчик» расположено на территории национального природного парка «Марий Чодра», на территории Волжского района.
Климат территории парка умеренно континентальный. Он характеризуется сравнительно жарким летом и морозной зимой с устойчивым снежным покровом. Средняя температура самого теплого месяца июля составляет 18,6°C. Абсолютный минимум температуры воздуха зимой достигает -52 C. Средняя продолжительность теплого периода года с температурой выше 0°C составляет около 200 дней.
Территория парка относится к зоне неустойчивого увлажнения: отмечаются годы с достаточным, иногда избыточным увлажнением, но бывают и засушливые годы. В течение года осадки выпадают неравномерно: наибольшее их количество отмечается летом, наименьшее - зимой. За год выпадает в среднем около 500 мм осадков. Самое большое месячное количество осадков отмечается в июле - 60-70 мм. Вторжение холодных воздушных масс из полярного бассейна с северными, северо-западными и северо-восточными ветрами вызывает резкое падение температуры зимой, а весной и осенью - заморозки. Нередко на территорию парка вторгаются континентальные воздушные массы с юго-востока. Весной или летом они обусловливают засушливые условия, зимой - ясную, морозную погоду.
Рельеф из-за развития современного карста представляет собой
слабоволнистую равнину с возвышенностями и впадинами. Само озеро,
соответственно, является озером провального типа с максимальной глубиной 35
метров. Озеро состоит из двух озёр: «Большой Яльчик» и «Малый Яльчик». Площадь
«Большого Яльчика» составляет - 1,285 ![]() , «Малый Яльчик» по площади занимает
- 0,536
, «Малый Яльчик» по площади занимает
- 0,536 ![]() . Процесс карста до сих пор
продолжает увеличивать озеро.
. Процесс карста до сих пор
продолжает увеличивать озеро.
Озеро расположено внутри массивного участка леса. Преобладающей породой является сосна. На северо-восточном берегу располагаются базы отдыха, детские лагеря, пансионаты: «Чайка», «Олимпиец», Пансионат «Яльчик» , «Политехник», «Рубин» и др. На северо-западном берегу располагается «дикий» пляж, оборудованный лишь контейнером для мусора.
Флора озера разнообразна. Береговая растительность представлена в виде,
кубышка жёлтая, стрелолист обыкновенный, сальвиния плавающая, можно встретить
кувшинку белую.[ 12 ]
Таблица - 3 Химический состав воды озера Яльчик за 1995 и 1998 годы [ 2 ]
|
Химические элементы |
1995 год |
1998 год |
3,4 мг/л |
4,0 мг/л |
|
|
1,9 мг/л |
14,5 мг/л |
||
|
|
нет |
следовое количество |
||
|
|
0,3 мг/л |
0,3 мг/л |
||
|
|
0,2 - 0,4 мг/л |
2,2 мг/л |
||
|
|
50 мг/л |
28 мг/л |
||
|
|
9 мг/л |
следовое количество |
||
|
|
170,8 мг/л |
250,1 мг/л |
||
|
|
- |
0,7 мг/л |
||
|
|
2,3 мг/л |
15,62 мг/л |
||
|
|
0,3 мг/л |
0,3 мг/л |
По данным таблицы можно наблюдать, что за трехлетний
период большая часть химических элементов увеличила свою концентрацию в воде.
Некоторые элементы такие как: Mg; Cl; HCl; ионы аммония - увеличили концентрацию в достаточно
большом количестве. Можно предположить, что в этот период начала возрастать
антропогенная нагрузка на озеро. Или снизилось качество обслуживания озера.
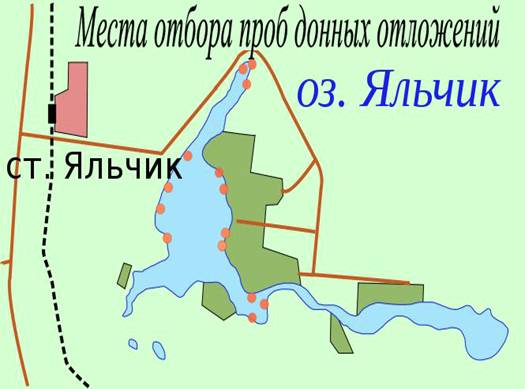
3. Методики исследования
Отбор проб воды для гидрохимических исследований в озерах производится с помощью батометра Молчанова ГР-18, с поверхностного и придонного (при глубине 5 м) горизонтов в стеклянные банки, заполняя их до краев и закрыв без пузырьков. При невозможности проведения анализа в указанный срок пробы воды охлаждают до +2 - +4 °С. Пробы хранят не более 24 часов после отбора [ 2 ].
В отобранных пробах определялись рН, общее Fe, жесткость, хлориды, нитраты, нитриты, нефтепродукты, взвешенные вещества, фосфаты и Ca, концентрация ТМ (Fe, Cu, Zn, Cd, Pb, Mg).
Отбор проб донных отложений (ДО) для гидрохимических исследований и растительного материала для биоиндикационных исследований. Отбор проб донных отложений в озерах осуществлялся в придонном (при глубине 5 м) слое специальным дночерпателем и помещали в широкогорлые стеклянные или пластиковые емкости с крышками, этикетировали, и доставляли в лабораторию, где их хранили в холодильнике. Отобранные пробы хранят до анализа в охлажденном (от 0 до -3°С) или в замороженном состоянии (до -20°С). Сосуды для хранения проб должны быть из химически стойкого стекла или полиэтилена, полученного при высоком давлении, с герметично закрывающимися крышками [ 3, 4, 5 ]. Отбор проб растений осуществлялся вручную с лодки или вдоль кромки водоема.
Все аналитические методики определения основных гидрохимических параметров допущены для целей государственного экологического контроля и утверждены метеорологической службой Росстандарт [ 6 ].
При определении физико-химических показателей использовались стандартные методы и методики, для определения рН - потенциометрический метод.
Определение концентраций тяжелых металлов в воде и донных отложениях
Химические исследования (атомно-абсорбционный метод) проводились согласно стандарту ИСО 11047 и методики ФГУ «ФЦАО», на атомно - абсорбционном спектрометре «AAnalit-400» [7, 8 ].
Математическая обработка данных проводилась с помощью методов
математической статистики: рассчитывались основные статистические показатели
выборок. Расчеты проведены с применением пакета «Statistica».
4. Исследовательская часть
Одним из наиболее объективных и надежных показателей загрязнения водоема и общей антропогенной нагрузки на него - содержание тяжелых металлов (ТМ) донных отложениях (ДО) и биоте. В отличии от органических веществ ТМ практически не подвержены деградации и могут лишь мигрировать и накапливаться в различных компонентах природной экосистемы. Накопление ТМ в ДО до значений, превышающих допустимые нормативы и фоновые представляют опасность для качества вод из - за возможного вторичного загрязнения. Высокие содержания ТМ в ДО неблагоприятно отражаются на биологических компонентах. Поскольку гидробионты активно аккумулируют из воды химические соединения, в частности ТМ, информация о содержании последних в природных водах важна для понимания влияния соединения металлов на водные организмы. Реальная картина качества воды и экологического состояния природного водоема и водотока должна включать в себя комплексную оценку содержания различных химических веществ в компонентах экосистемы водоема. [ 9 ]
Предельно допустимая концентрация вещества в воде водоема хозяйственно-питьевого и культурно-бытового использования (ПДКв, мг/л) - это концентрация вредного вещества в воде, которая не должна оказывать прямого или косвенного влияния на организм человека в течение всей его жизни и на здоровье последующих поколений, и не должна ухудшать гигиенические условия водопользования.
Нормативы ПДК для культурно-бытового водопользования использовали в соответствии с СанПиН 2.1.4.1074-01.
.1 Содержание тяжелых металлов в воде и донных отложениях озера «Яльчик»
Для оценки экологического состояния водоема исследовали следующие физико-химические параметры воды и донных отложений: содержание ТМ в воде и донных отложениях. Кислотность водной среды, ее жесткость и общая минерализация.
Результаты анализа на наличие тяжелых металлов проведенного по воде
показали, что содержание в воде свинца превышает ПДК в 1,01 раза. Кадмий -
отсутствует, также отсутствуют хром, кобальт, никель и марганец. Концентрация
меди не превышает допустимую концентрацию, также цинк и железо превышения по
концентрации не дают. Концентрация кальция в воде сравнительно близка к
предельно допустимой ( табл. 4).
Таблица - 4 Содержание тяжелых металлов в воде озера Яльчик
|
Содержание тяжелых металлов в воде озера Яльчик |
||
|
Тяжелые металлы |
Концентрация, мг/л |
ПДК, мг/л |
|
Pb |
0,070±0,006 |
0,069 |
|
Cd |
0 |
0,014 |
|
Sr |
0,06±0,001 |
- |
|
Cr |
0 |
0,05 |
|
Co |
0 |
- |
|
Ni |
0 |
|
|
Cu |
0,0009±0.00009 |
1,0 |
|
Zn |
0,009±0.0005 |
0,22 |
|
Mn |
0 |
0,1 |
|
Fe |
0,02±0,002 |
0,63 |
|
K |
1,74±0.04 |
- |
|
Ca |
120±11 |
30-140 |
Таким образом, качество воды на объекте исследований по содержанию тяжелых металлов можно считать удовлетворительным: превышение ПДК наблюдается только в отношении свинца.
Анализ донных отложений на содержание ТМ показал, что стронций имеет превышение предельно допустимой концентрации в 1,8 раз. Концентрация хрома, марганца, железа, меди, кадмия и цинка в донных отложениях не имеет превышения по предельно допустимым концентрациям. Концентрация никеля в донных отложениях имеет превышение предельно допустимой концентрации в 1,144 раз. ПДК(табл.5).