Материал: Физхимия шпоры
1.Термодинамическая система. Параметры и функции состояния термодинамической системы. Формы обмена энергией термодинамической системы с окружающей средой. Выражение количества работы через параметры состояния термодинамической системы.
Химическая термодинамика изучает превращения химической энергии в теплоту, работу и другие энергии.
ТД изучает термодинамические системы(ТС).
ТС-часть пространства, выделяемая для изучения, которая отделена от окружающей среды(ОС) реальной или воображаемой границей.
Типы ТС:
Изолированные – отсутствуют, какие-либо формы обмена с окружающей средой.
Открытыми – система обменивается с окружающей средой энергией и веществом.
Закрытые - система обменивается с окружающей средой только энергией, обмен веществом невозможен.
Адиабатические- нет обмена веществом и нет теплообмена.
Для описания ТС:
ТД параметры
Интенсивные (не зависит от кол-ва в-ва) – t, P, δ.
Экстенсивные (зависит от кол-в в-ва) – V, m, ν.
Уравнение, которое связывет ТД параметры, называется уравнением состояния.
PV= νRT – уравнение Менделеева-Клапейрона.
Всякое изменение ТД параметров есть ТД процесс.
ТД функции
Состояния – U, H, S, G, F. Зависят от основных.
В химии наиболее часто используются:
внутренняя энергия U и её изменение U при V = const;
энтальпия (теплосодержание) H и её изменение H при p = const;
энтропия S и её изменение S;
энергия Гиббса G и её изменение G при p = const и T = const.
Для ф-ций состояния хар-но, что их изм-ние в хим. р-ции определяется только начальным и конечным состоянием системы и не зависит от пути или способа протекания процесса.
Процесса – Q, А. Зависит от пути перехода.
Q (теплота образования)- форма передачи энергии путем сталкивания молекул сталкивающихся тел; это микроскопическая неупорядоченная форма передачи энергии хаотичным движением частиц.
А(работа) – это макроскопическая форма передачи энергии упорядоченных частиц.
Теплота и работа зависят от пути процесса, следовательно, они являются функциями процесса, а не состояния. Теплоту и работу выражают в джоулях (Дж). Теплота является положительной величиной, если система ее поглощает, а отрицательной - если система её выделяет. Работа является положительной величиной, если она осуществляется системой, и отрицательной- если она осуществляется над системой.
А= P V
2.Первый закон термодинамики. Обмен энергией в форме работы и теплоты. Понятия: внутренняя энергия, энтальпия. Обмен энергией в форме теплоты. Изобарная и изохорная теплоёмкости.
Первый закон ТД(закон сохранения и превращения энергии):
В любом процессе в закрытой системе изменение внутренней энергии равно количеству сообщающейся системе теплоте за вычетом работы, которую совершает система.
∆U=Q-A
dU=δQ-δA
Внутренняя энергия системы (U, Дж) – это полная энергия системы, включающая кинетическую энергию всех видов движения молекул, атомов, ядер, электронов и других структурных единиц, а также потенциальную энергию взаимодействия и др., кроме кинетической и потенциальной энергии всей системы как целого по отношению к другим системам.
Абсолютное значение внутренней энергии определить невозможно, т.к. нельзя привести систему в состояние, полностью лишенное энергии.
Можно судить лишь об изменении внутренней энергии системы U при её переходе из начального состояния U1 в конечное U2:
U = U2 U1,
При переходе неизолированной системы из одного состояния в другое изменение её внутренней энергии осуществляется путём обмена с окружающей средой.
Основными формами обмена с окружающей средой являются совершение работы и выделение или поглощение теплоты.
Энтальпия (Н, Дж) — это термодинамическое свойство вещества, которое указывает уровень энергии, сохраненной в его молекулярной структуре. Это значит, что, хотя вещество может обладать энергией на основании температуры и давления, не всю ее можно преобразовать в теплоту.
Н=U+pU
∆H=∆U+∆νPT,
где ∆ν – изменение числа моль газообразных веществ.
Теплоемкость (С) - это отношение количества сообщаемой системе теплоты и наблюдаемое при этом повышение Т.
Типы теплоемкости:
Средняя
С=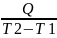 (Дж/К)
(Дж/К)
Истинная
С=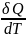
Удельная
Молярная
Изохорная Cv
V-const,
ν
Cv=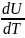
Изобарная Cp P-const, νCv=
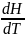
dU= νCvdT => ∆U= νCv(T2-T1)
dH= νCpdT
Cp=Cv+R – связь изобар и изохор теплоемкости.
Для одноатомных идеальных газов Cv=3/2R, Cp=5/2R
Для идеального газа Cv=5/2R, Cp=7/2R
3.Термодинамический процесс. Обратимые и необратимые процессы. Равновесные и неравновесные процессы. Самопроизвольный процесс. Классификация термодинамических процессов в зависимости от условий их проведения.
Любое изменение термодинамически состояния системы, то есть изменение хотя бы одного параметра состояния называется термодинамическим процессом.
Состояние равновесия - состояние, при котором система не изменяется во времени, и в ней отсутствуют потоки вещества или энергии.
О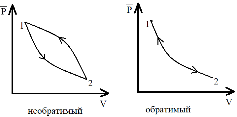 братимым
процессом
является процесс, который дает возможность
возвращения системы в исходное состояние
без того, чтобы в окружающей среде
произошли какие-либо изменения. В
противном случае процесс является
необратимым.
братимым
процессом
является процесс, который дает возможность
возвращения системы в исходное состояние
без того, чтобы в окружающей среде
произошли какие-либо изменения. В
противном случае процесс является
необратимым.
Равновесный процесс - процесс, в ходе которого система проходит через непрерывный ряд равновесных состояний.
НЕРАВНОВЕСНЫЙ ПРОЦЕСС - физ. процесс, включающий неравновесные состояния.
К самопроизвольным относятся процессы, проходящие без затраты энергии извне. Может происходить обратимо или необратимо. Для осуществления несамопроизвольного процесса необходимо затратить внешнюю энергию в количестве, пропорциональном величине изменения состояния системы.
Применение 1 закона ТД к некоторым процессам, в которых совершается только А расширенная:
Т=const – изотермический
∆U=0, Q=A= νRTln(V2/V1)
V=const – изохорный
A=0, ∆U=Q
P=const – изобарный
Q=∆U+p∆U, ∆H=Q, H=U+pV
Q=const - адиабатический
dU=-δA, A= νCv(T2-T1), ϒ=Сp/Cv
TVϒ-1=const => уравнение адиабаты
PVϒ=const
4.Термохимия. Закон Гесса и следствия из закона г есса. Теплоты образования и теплоты сгорания. Расчёт тепловых эффектов физико-химических процессов.
Раздел химии и хим. ТД, занятый расчётами тепловых эффектов, наз-ся термохимией.
Термохимические уравнения:
аА + bB = cC + dD; Hp
ех: Н2 + 1/2О2 = Н2О(ж); ΔΗ˚298 = -285,8 кДж,
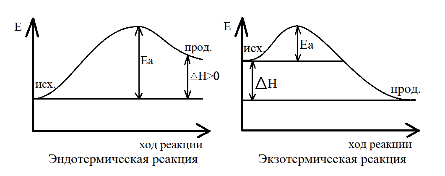
Закон Гесса :
Тепловой эффект реакции (Нр) не зависит от пути её протекания, а определяется только природой и физическим состоянием исходных веществ и конечных продуктов.
Qv=∆U; Qp =∆H
Следствия закона:
Тепловой эффект прямой реакции равен тепловому эффекту обратной, но с обратным знаком.
Изменение энтальпии химической реакции равно сумме энтальпий образующихся продуктов реакции за вычетом сумм энтальпии исходных веществ с учетом их стехиометрических коэффициентов.
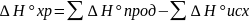
Энтальпия образования (∆H◦f , кДж/моль)– тепловой эффект образования 1 моль в-ва из простых в-в в стандартных условиях.
Энтальпия реакции равна разности сумм энтальпий сгорания начальных и конечных реагентов с учетом их стехиометрических коэффициентов.
ΔH = ΣΔHсгор.нач – ΣΔHсгор.конечн |
5.3Ависимость тепловых эффектов химических реакций от температуры. Закон Кирхгофа.
Зависимость теплового эффекта химической реакции от температуры определяется законом Кирхгофа.
т.е.
влияние температуры на тепловой эффект
реакции обусловлено разностью
теплоемкостей продуктов реакции и
исходных веществ c учетом стехиометрических
коэффициентов:![]() .
.
При
P = const:![]() .
.
Закон Кирхгофа:
Температурный коэффициент теплового эффекта химической реакции равен изменению теплоёмкости системы в ходе реакции.
б.Самопроизвольные и несамопроизвольные процессы. Второе начало термодинамики. Теорема Карно-Клаузиуса. Принцип существования энтропии. Принцип возрастания энтропии.
К самопроизвольным относятся процессы, проходящие без затраты энергии извне. Может происходить обратимо или необратимо. Для осуществления несамопроизвольного процесса необходимо затратить внешнюю энергию в количестве, пропорциональном величине изменения состояния системы.
Второй закон ТД:
В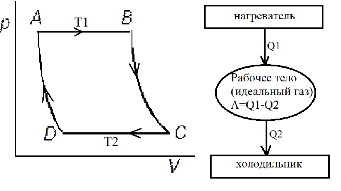 любой системе два произвольно выбранных
состояния отличаются тем, что переход
из 1 во 2 самопроизвольный, а переход из
2 в 1 – с затратой энергии, поэтому должен
существовать объективный критерий
системы, позволяющий судить о направлении
реакции.
любой системе два произвольно выбранных
состояния отличаются тем, что переход
из 1 во 2 самопроизвольный, а переход из
2 в 1 – с затратой энергии, поэтому должен
существовать объективный критерий
системы, позволяющий судить о направлении
реакции.
Машина работает обратимо под цепью из 2 изотерм AB и CD, Т1=const, и 2 адиабат BC и DA. На участке AB рабочее тело изотермически при Т=Т1, претерпевая циклические изменения, рабочее тело возвращается в исходное состояние, при этом совершает работу А=Q1-Q2.
1.|AB|, T=T1=const (ΔU=Q-A)
A1=Q1=RT1lnV1/V2
2.|CD|, A3=Q3=RT2lnV4/V3, где V1-n=A-D.
Из уравнения адиабаты: VTᵞ-1=const
Для точек A и D →V4/V3=V1/V2. => A3=Q2=-RT2lnV2/V1
3.|BC|
A2=Cv(T1-T2)
4.|DA|
A4=Cv(T2-T1)=-Cv(T1-T2)
Суммируем А на всех участках:
А=∑A=R(T1-T2)lnV2/V1
Принимая, что Q1=RT1lnV2/V1, найдём КПД машины:
Ƞ=A/Q1=(Q1-Q2)/Q1=(T1-T2)/T1
ВЫВОДЫ:
1.КПД тепловой машины, работающей обратимо по циклу Карно, не зависит от природы рабочего тела, а лишь от температуры нагревателя и холодильника. Это теорема Карно-Клаузиуса.
2.Т.к.работа обратимого процесса является максимальной, то КПД машины, которая работает по необратимому циклу, меньше КПД по обратному циклу:
Ƞнеобрат. < Ƞобрат.
Принцип существования энтропии:
Для каждой ТД системы существует физическая величина энтропии, значение которой зависит от состояния системы и изменения которой происходит только под действием энергии, передаваемой в виде теплоты.
Q1/T1-Q2/T2=0, где Q/T-приведенная теплота.
Принцип возрастания энтропии:
Принцип возрастания энтропии сводится к утверждению, что энтропия изолированных систем неизменно возрастает при всяком изменении их состояния и остается постоянной лишь при обратимом течении процессов.
Q1/T1<Q2/T2 => ∆S>0 – условие самопроизвольного протекания процесса.