Материал: Фармакотерапия глазных болезней
Препарат быстро и практически полностью всасывается при приеме внутрь: биодоступность Максаквина составляет почти 100%, и достаточно медленно выводится из организма (период полувыведения в среднем составляет 7 ч).
Выделяется Максаквин из организма с мочой в основном в неизменном виде, выведение пропорционально принятой дозе и составляет 46 - 69% за 24 ч.
Противопоказанием для применения Максаквина является плохая переносимость препаратов группы хинолонов. Как и другие хинолоны, Максаквин не рекомендуется назначать беременным женщинам, детям и подросткам.
В процессе лечения Максаквином необходимо избегать пребывания на солнце и УФ-облучения во избежание развития фотодерматоза.
Производитель препарата фирма "Серл" ("Searle', США), которая выпускает ломефлоксацин под названием Максаквин (Maxaquin).
Окацин (Okacin) - ломефлоксацин 0,3% (Lomefloxacin) - высокоэффективное синтетическое химиотерапевтическое средство широкого спектра действия, выпускаемое в виде глазных капель по 5 мл во флаконе. Производитель препарата - лаборатория CIBA VISION, Франция.
Окацин относится к группе антимикробных препаратов дифторхинолонов из класса хинолонов. Высокочувствительными к Окацину являются грамположительные бактерии (Staphylococcus aureus, Staphylococcus epidermidis, Staphylococcus saprophyticus); грамотрицательные (Citrobacter diversus, Enterobacter cloace, Escherichia coli, Haemophilus influenzae, Klebsiella pneumoniae, Moraxella catarrhalis, Proteus mirabilis, Pseudomonas aeruginosa, Neisseria sp.) и другие микроорганизмы (Clamydia trachomatis).
Противопоказанием для применения Окацина является гиперчувствительность к препаратам хинолонового ряда.
Тобрекс (тобрамицин 0,3%) - антибиотик, предназначенный для местного применения при лечении инфекционных заболеваний переднего отрезка глаза. Выпускается в виде глазных капель и мази. В 1 мл раствора содержится тобрамицина 0,3% (3 мг/мл) и бензалконий хлорид (0,01%) в качестве консерванта. В 1 грамм мази входит: тобрамицин 0,3% (3 мг/г), минеральное масло, вазелиновая основа и хлорбутанол (0,5%) в качестве консерванта. Производитель препарата - фирма ALCON, Бельгия.
Тобрекс (Тобрамицин) - антибиотик широкого спектра действия, хорошо растворимый в воде, относящийся к группе аминогликозидов и обладающий бактерицидным действием. Препарат высоко активен в отношении грамотрицательных микроорганизмов (Pseudomonas aeruginosa, Escherichia coli, Klebsiella pneumonia, Enterobacter aerogenes, Proteus, Haemophilus influenzae, Moraxella lacunata, Acinetobacter calcaceticus, Neisseria gonorrhoeae), a также грамположительных микроорганизмов (стафилококков, в том числе Staphylococcus aureus, Staphylococcus epidermidis и штаммов, устойчивых к пенициллину, метициллину, некоторым штаммам стрептококков, в том числе Streptococcus pneumoniae).
Противопоказанием для назначения Тобрекса является гиперчувствительность к препаратам аминогликозидов.
Витабакт (Vitabact) - пиклоксидин 0,05% (Picloxydine) - антисептик с широким антибактериальным спектром действия. В состав глазных капель Витабакт входит антисептический препарат пиклоксидин дигидрохлорид 0,05%.
Производитель препарата - лаборатория CIBA VISION, Франция.
Витабакт эффективен против многих видов бактерий, вызывающих такие широко распространенные инфекционные заболевания глаз, как конъюнктивиты острые и хронические, блефароконъюнктивиты, блефариты. Как антисептическое средство Витабакт применяется и при тяжелых заболеваниях роговицы таких, как кератиты, язва роговицы. В отделе инфекционных и аллергических заболеваний глаз МНИИ ГБ им. Гельмгольца проходили курс амбулаторного и стационарного лечения больные, у которых была обнаружена микрофлора: стафилококк патогенный, пневмококк, стафилококк + пневмококк, стрептококк, кишечная палочка, палочка Ксероза. При использовании в лечении глазных капель Витабакт положительный терапевтический эффект отмечен у всех больных.
Витабакт обладает хорошей переносимостью, противопоказанием к применению может служить аллергия на один из компонентов препарата.
Колбиоцин (Colbiocin) - антибактериальный препарат, выпускающийся в виде глазных капель и мази. Производитель - фирма SIFI, Италия. В 100 мл глазных капель Колбиоцин содержатся вещества: хлорамфеникол 4 мг; колистин 18.000.000 М.Е.; ролитетрациклин 5 мг, соответствующий 4,21 мг тетрациклина. В 1 г глазной мази Колбиоцин содержится: хлорамфеникол 10 мг, колистин 18.000.000 М.Е., тетрациклин 5 мг. Глазные капли выпускаются во флаконе по 5 мл, глазная мазь в тубе по 5 г.
Колбиоцин - антибактериальный противовоспалительный препарат, обладающий широким спектром действия. Высоко активен в отношении грамположительных и грамотрицательных бактерий (в том числе Pseudomonas aeruginosa), спирохет, хламидий, микоплазм, риккетсий, амеб. Противопоказанием к применению является индивидуальная повышенная чувствительность к компонентам препарата.
Эубетал антибиотик (Eubetal antibiotico) выпускается в виде глазных капель во флаконе емкостью 3 мл, и глазной мази в тубе 3 гр. Изготовитель фирма SIFI, Италия. В 1 мл глазных капель Эубетал содержатся: бетаметазон динатрий фосфат 1 мг; хлорамфеникол 4 мг; колистин 18.000.000. М.Е.; ролитетрациклин 5 мг, который соответствует 4,21 мг тетрациклина.
В 1 г мази содержатся: бетаметазон динатрий фосфат 1 мг; хлорамфеникол 10 мг; колистин 18.000.000 М.Е.; тетрациклин 5 мг.
Эубетал - комбинированный препарат для местного
применения в офтальмологии, оказывает выраженное антибактериальное,
противовоспалительное и противоаллергическое действие. Активен в отношении
грамположительных и грамотрицательных бактерий (в том числе Pseudomonas и
Haemophilus), воздействует на микоплазмы, риккетсии, хламидии и амебы.
Противопоказанием к применению являются: повышенная чувствительность к
компонентам препарата, повышенное внутриглазное давление, заболевания роговицы
в стадии изъязвления (положительный тест с флюоресцеином), эрозия роговицы,
угроза перфорации роговицы[11].
.1 Терапия при язвах роговицы, вызванных
синегнойной палочкой
При язве роговицы, вызванной синегнойной палочкой, молниеносное течение воспалительного процесса может привести к перфорации через 2-3 дня от начала заболевания. В этом случае главным в лечении являются новые группы антибиотиков: хинолоны, аминогликозиды и некоторые цефалоспорины. Ломефлоксацин (окацин), норфлоксацин (чиброксин), ципрофлоксацин (цилоксан), тобрамицин (Тобрекс), гентамицин + полимиксин, амикацин, колбиоцин (тетрациклин) применяются в виде инстилляций, 5 - 8 раз в день. Антибактериальную терапию дополняют инстилляции противовоспалительных препаратов, мидриатиков, препаратов регенерирующего и эпителизирующего действия.
Максаквин (ломефлоксацин) оказался наиболее перспективным в комплексном лечении бактериальных кератитов и язв роговицы. В наших наблюдениях группу больных с заболеваниями роговицы бактериальной этиологии составили 45 человек, из них 20 больных с кератоувеитом, 4 больных с кератоувеитом с изъязвлением, 11 больных с язвой роговицы, 5 больных со стромальным кератитом (один из которых акантамебный), 5 - со стромальным кератитом с изъязвлением, (2 из которых акантамебные). Системный курс Максаквина включал: по 1 таблетке (400 мг) 2 раза в день в течение 5 дней при кератитах и язвах роговицы средней тяжести. При тяжелых язвах продолжительность лечения составляла 10 дней. При анализе результатов лечения препаратом Максаквин учитывали сроки исчезновения микрофлоры из мазков и посевов, а также исчезновение клинических симптомов заболевания. Выздоровление наступило у всех больных в сроки 20-35 дней, т.е. быстрее, чем при применении других препаратов.
В лечении инфекции глаз, вызванной синегнойной
палочкой, особая роль отводится хинолоновым антибиотикам, применяемым местно и
внутрь (Таблица 1).
Таблица 1.

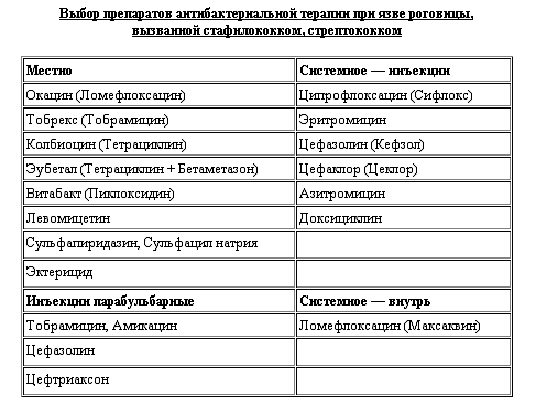
.2 Терапия при язвах роговицы, вызванных
стафилококком и стрептококком
При язве роговицы, вызванной стафилококками,
стрептококками, пневмококком, главным в лечении является местное и системное
применение антибиотиков и сульфаниламидов (Таблица 2). Наиболее перспективными
в этих случаях являются антибактериальные препараты нового поколения -
хинолоны: ломефлоксацин (Максаквин для системного, Окацин для местного
применения), цефалоспорины: цефазолин, цефтриаксон - парабульбарно и
внутримышечно, глазные капли: Сульфапиридазин, Тобрекс, Витабакт; глазные мази:
Колбиоцин, Эубетал.(см.таб 2).
Таблица 2.
.3 Терапия больных хламидийным конъюнктивитом
Больным с хламидийным конъюнктивитом проводится комплексное системное и местное лечение, при необходимости проводят лечение у гинеколога или уролога.
Проведенные нами клинические наблюдения,
охватывающие около ста стационарных и амбулаторных больных с хламидийным
конъюнктивитом, позволяют рекомендовать методику, включающую общее и местное
лечение: 10-дневный курс Максаквина (ломефлоксацина) по 1 таблетке (400 мг) 1
раз в день в сочетании с одним из препаратов для местной терапии: Эубетал,
мазь, 4-5 раз в день; Колбиоцин, мазь, 4-5раз в день; Окацин 0,3%, глазные
капли, 5-6 раз в день.По наблюдениям, такая схема лечения была наиболее
эффективна, что проявлялось в более активной резорбции инфильтрации и
фолликулов конъюнктивы, уменьшении явлений кератита и лимбита. В конечном итоге
это привело к значительному сокращению длительности лечения по сравнению с
пациентами, получавшими такое же местное лечение, а системно - ципрофлоксацин
или тетрациклин (таблица 3).
Таблица 3.
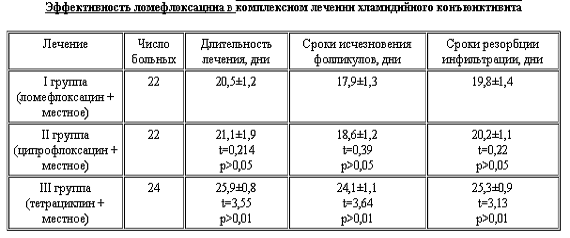
При использовании ломефлоксацина удалось сократить длительность лечения в стационаре на 5,4 дня по сравнению с традиционным курсом тетрациклина. Немаловажно, что ломефлоксацин применяли в меньшей суточной дозе, чем ципрофлоксацин, однако по своей эффективности препарат не только не уступал, но и превзошел результат при лечении ципрофлоксацином, что также сказалось на длительности лечения.Все пациенты хорошо переносили ломефлоксацин, не было отмечено побочных проявлений или аллергических реакций на препарат. Учитывая высокую эффективность и безопасность лечения ломефлоксацином, а также доступность для пациентов, его можно считать препаратом выбора при лечении хламидийного конъюнктивита в стационаре и рекомендовать для широкого амбулаторного применения[11].При положительной динамике на фоне проводимого лечения число инстилляций капель или аппликаций мази уменьшается в каждую последующую неделю.
По нашим наблюдениям, наиболее эффективной оказалась мазь Эубетал: в течение 4 недель излечено 71,8% больных, а в течение 6 недель - 86,4%. Больные, получившие эту мазь, уже в первые дни лечения отмечали субъективное улучшение состояния: уменьшились светобоязнь, слезотечение, гиперемия и отек слизистой, что мы связываем с наличием в составе мази кортикостероида бетаметазона.
По терапевтическому эффекту мазь Колбиоцин несколько уступала мази Эубетал, но оба препарата по терапевтической эффективности превосходят тетрациклиновую мазь и субъективно лучше переносятся больными благодаря более нежной мазевой основе. У больных, получавших глазные капли Окацин, был отмечен хороший терапевтический эффект препарата, не было зарегистрировано случаев непереносимости или аллергических реакций. Применение глазных капель Окацин или глазной мази Колбиоцин целесообразно сочетать с противовоспалительной терапией: начиная со второй недели добавлять инстилляции глазных капель дексаметазона (Максидекс) - одну неделю - 1 раз в день, в последующие - 2 раза в день. При острых хламидийных конъюнктивитах в течение первой недели антибиотикотерапию целесообразно сочетать с местным применением противоаллергических капель: например, инстилляция глазных капель Гистимет или Кромогексал 2 раза в день.
Таким образом, антибиотики-фторхинолоны, в том
числе Максаквин, являются несомненными препаратами выбора как для системного,
так и для местного лечения хламидийного конъюнктивита, обладая высокой
эффективностью и хорошей переносимостью.
Глава 3. Наноносители лекарственных веществ в
офтальмологии
Применение нанотехнологий (т. е. технологий частиц, размеры которых измеряются нанометрами) в фармации оказалось весьма плодотворным и в течение последних 10-15 лет привело к созданию препаратов, обладающих новыми свойствами на основе давно и хорошо известных лекарственных веществ (ЛВ).
Наноносители представляют собой один из видов терапевтических систем. С их помощью удается реализовать целенаправленный транспорт ЛВ в орган-мишень или ткань-мишень, что является одним из базовых элементов технологии контролируемого высвобождения. При длительной циркуляции наноносителей в кровяном русле содержащееся в них ЛВ защищается от инактивации, а его действие пролонгируется.
Размер частиц корпускулярных носителей определяется:
)проходимостью артерио-венозных капилляров (частицы <1000 нм), хотя это не относится к “шунтирующим” частицам, которые, застревая в капиллярах, постепенно выделяют ЛВ и рассасываются;
)стабильностью суспензии наноносителей в плазме крови, т. к. агрегация (слипание частиц друг с другом) вызывает сильные токсические эффекты, вплоть до тромбозов средних и мелких сосудов;
)способностью наноносителей проникать внутрь клеток, что наиболее эффективно для частиц размером от 300 до 50 нм;
)вязкостью суспензии наноносителей в плазме крови.
В отличие от макрокапсул (например, желатиновых) и микрокапсул (размером 500-10 мкм) наноносители предназначены не столько для перорального введения (хотя и оно применяется), сколько для инъекционного введения как внутривенного (транспорт к органам-мишеням либо длительная циркуляция в кровяном русле), так и внутримышечного (депо ЛВ или постепенное поступление наноносителей либо выделяемых ими ЛВ в кровоток). Также используется пероральное, ингаляционное и интраокулярное введение наноносителей. Возможна также интра- и трансдермальная подача ЛВ с помощью наноносителей. Широко применяются наноносители в косметике.
Наноносители могут быть двух видов:
)наночастицы, представляющие монолитные, обычно сферические образования, содержащие ЛВ по всей массе наночастицы или только на ее поверхности. Выделение ЛВ из наночастицы происходит постепенно с контролируемой скоростью: а) только с поверхности; б) со всей массы наночастицы в результате ее распада или набухания. К наночастицам относятся также нанокристаллы, состоящие только из ЛВ, подвергнутого измельчению до соответствующих размеров, что позволяет им растворяться со скоростью, превышающей скорость растворения частиц более крупных размеров;
)нанокапсулы представляют собой полые сферические контейнеры (с толщиной стенки ~10-30 нм), содержащие жидкую среду, в которой растворено ЛВ. Высвобождение ЛВ из нанокапсулы происходит за счет диффузии ЛВ через стенку или разрыва капсулы. Скорость высвобождения регулируется дизайном нанокапсул и способом их получения.
Взаимодействие наноносителей с клетками зависит и от материала, из которого они изготовлены. Наиболее часто используют:
нанокристаллы ЛВ без дополнительного материала;
липиды (жиры) для получения липидных нанокапсул, т. е. липосом, и липидных наночастиц;
полимеризованные липиды (полимерные липосомы);
термически или химически модифицированный сывороточный альбумин;
химически модифицированные полисахариды (например, диальдегидкрахмал);
биодеструктирующиеся, т. е. распадающиеся постепенно в организме, полимеры и сополимеры (полиалкилцианоакрилаты, полиллактидгликолиды).
Нанокристаллы по сравнению с другими наносистемами имеют следующие преимущества:
высокая (~100%) степень содержания ЛВ;
простая и предсказуемая подача ЛВ (скорость высвобождения растворимого ЛВ зависит от скорости растворения нанокристаллов);
распределение ЛВ в организме происходит как обычно;
простой и эффективный способ производства.
Обладая большой удельной поверхностью, нанокапсулы особенно пригодны для труднорастворимых ЛВ. При пероральном введении увеличивается абсолютная биодоступность, уменьшаются индивидуальная вариабельность и эффект потребленной пищи. Максимальная концентрация ЛВ в плазме достигается быстрее. Добавляемые иногда биостабилизаторы не только стабилизируют нанокристаллы (например, от агрегации), но и дают возможность контролировать их распределение в организме, время транспорта через желудочно-кишечный тракт, а также биоадгезию, т. е. прилипание к стенкам кишечника в определенном месте (мишени). Уменьшается терапевтическая доза ЛВ. Актуально применение нанокристаллов для анальгетиков, когда быстрое подавление боли и уменьшение вариабельности концентрации ЛВ в плазме играют решающую роль. Например, дисперсия нанокристаллов напроксена через ~20 мин дает в 3-5 раз большую концентрацию ЛВ в плазме по сравнению с обычной суспензией или таблетками ЛВ и меньшую зависимость от содержимого желудка.
Нанокристаллы ЛВ часто включают в макрокапсулы, матричные таблетки и т. д. Добавление биоспецифических мукоадгезивов (веществ, склеивающихся со слизистой оболочкой) позволяет локализовать действие нанокристаллов ЛВ в определенной области желудочно-кишечного тракта.