Материал: Электрообработка в технологиях очистки воды
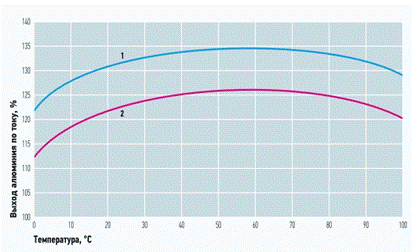
Рисунок 1 показывает зависимость выхода алюминия по
электрическому току от температуры обрабатываемой воды.
На рисунке 2 представлена схема движения воды по
межэлектродным каналам.
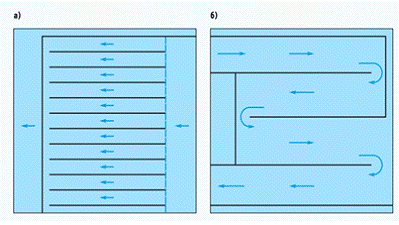
Рисунок 2 - Схема движения воды по межэлектродным
каналам (а - параллельное, б - лабиринтное)
Сама по себе электрокоагуляция всех вопросов не решает, но играет ключевую роль при комплексном подходе к очистке воды.
Перед электрокоагуляцией через насос-дозатор в общий поток подается окислитель, расходы которого незначительны, при этом происходит первичное окисление различных загрязнений.
Вторичное окисление проистекает непосредственно в электрокоагуляторе. В процессе электрокоагуляции, проводимой при переменном давлении, появляются очень мелкие, буквально микроскопические пузырьки, заполняющие собой всё межэлектродное пространство. Поскольку процесс окисления происходит диффузионно - через стенку пузырька, то их малый размер и обилие многократно интенсифицируют названный процесс, так как, в этом случае, основным является величина суммарной поверхности раздела фаз.
Третичное окисление происходит в отстойниках, где продолжается процесс дегазации, но уже как остаточное явление. Образовавшиеся продукты окисления достаточно плохо осаждаются при традиционных технологиях, но при коагулировании проистекает интенсивное хлопьеобразование и выделение продуктов окисления в осадок совместно с полученными хлопьями. Затем вода подаётся на осветление (фильтрация через зернистую загрузку). После чего с помощью последовательного использования сорбента и катионита происходит удаление из воды остаточных загрязнений. На выходе очищенная вода подвергается ультрафиолетовому облучению.
В случаях значительного биозагрязнения исходной воды, на входе очистной
системы предусмотрено наличие второго насоса-дозатора, предназначенного для
введения дополнительного окислительного агента. Данный насос подключается по
мере необходимости, если в исходной воде наблюдается значительное увеличение
концентраций загрязняющих веществ.
4. Электрокоагуляция как технологический процесс
Электрокоагуляция - коагуляция (оседание) высокодисперсных коллоидных частиц и взвесей в виде гидроокисей металлов (алюминий, железо), генерируемых электрическим током за счет растворения металла анода (алюминиевого или железного) и воздействия постоянного электрического тока, который вызывает электролитическую диссоциацию растворенных в воде солей, а также селективное взаимодействие образующихся ионов с образованием и выпадением в осадок в виде нерастворимых гелей. Вследствие растворения анодов вода обогащается соответствующими катионами металлов, образующими затем в нейтральной и слабощелочной среде гидроокисью алюминия или гидрозакисью железа, которая под воздействием растворенного в воде кислорода переходит в гидроокись железа. Гидроокиси металлов обладают повышенной коагуляционной активностью и сорбционной способностью, что обеспечивает эффективную коагуляцию дисперсных примесей с участием продуктов электролиза.
Наряду с электрокоагуляцией при наложении электрического поля происходит также: электролиз воды; поляризация коллоидных частиц; движение заряженных частиц в электрическом поле (электрофорез); окислительно-восстановительные процессы; химические реакции между ионами Аl3+ или Fe2+, образующимися при электролитическом растворении металлических анодов и некоторыми содержащимися в воде ионами (S2-, РO43-); взаимодействие продуктов электролиза друг с другом; флотация твердых частиц пузырьками газообразного водорода, выделяющегося на катоде; сорбция ионов и молекул растворенных примесей на поверхности гидроксидов железа и алюминия, обладающих значительной сорбционной способностью.
Различают электростатическую, электрохимическую и гальваническую коагуляцию. Электростатическая коагуляция протекает за счет поляризации коллоидных частиц под влиянием внешнего электрического поля и слипания образовавшихся диполей. При этом возможно применение, как постоянного поля, так и пульсирующего и знакопеременного. Для электростатической коагуляции требуются очень большие напряженности электрического поля, около 10-30 кВ/м, поэтому этот метод в водообработке сточных вод используется мало. Разновидностью электростатической можно считать электроконтактную коагуляцию, которая возникает при фильтровании воды в электрическом поле. В этом случае возможна частичная поляризация гидратированных ионов и коллоидных частиц под действием электрического поля с последующей коагуляцией диполей. Однако необходимые для коагуляции коллоидных частиц напряженности электрического поля очень велики, и этот способ применяется, в основном, для очистки обессоленных вод.
Электрохимическая коагуляция протекает за счет электролиза воды и изменения значения рН и окислительно-восстановительного потенциала в объеме воды вблизи электродов. Электролиз производится с нерастворимыми электродами при электрическом напряжении на электродах, превышающем потенциал разложения воды (1,22 В).
Гальваническая электрокоагуляция протекает за счет электрохимического растворения в воде металлических электродов. В качестве материала электродов используют алюминий или сталь.
Механизм электрокоагуляции последовательно включает в себя следующие стадии: электрофоретическое концентрирование (направленное движение заряженных частиц примесей и концентрирование их у поверхности электродов); растворение электрода и образование гидроокисей металлов; поляризационная коагуляция дисперсных частиц; упаковка первичных агрегатов по мере накопления частиц гидроокисей; флокуляционная коагуляция; флотация образовавшихся агрегатов пузырьками газов.
На процесс электрокоагуляции оказывает влияние материал электродов, расстояние между ними, скорость движения сточной воды между электродами, ее температура и солевой состав, напряжение, сила и плотность электрического тока. С повышением концентрации взвешенных веществ более 100 мг/л эффективность электрокоагуляции снижается. С уменьшением расстояния между электродами расход энергии на анодное растворение металла уменьшается. Теоретический расход электроэнергии для растворения 1 г железа составляет 2,9 Вт*ч, а 1 г алюминия - 2 Вт*ч.
Степень использования металла электродов составляет 50-90% и зависит от конструкции коагуляторов, материала анода и состава обрабатываемой воды.
Электрокоагуляцию рекомендуется проводить в нейтральной или слабощелочной среде содержащей не менее 20% хлористых солей (от общего солесодержания) и не более 75% гидрокарбонатов и сульфатов, вызывающих пассивацию электродов, при плотности электрического тока не более 10 А/м2, расстояния между электродами не должны превышать 20 мм, а скорости движения воды - не менее 0,5 м/с.
При наличии в воде больших количеств катионов Са2+ и Mg2+ и невозможности добавления к ней хлоридов в качестве катодного материала следует использовать нержавеющую сталь и не производить смену полярности электродов. Продолжительность электрообработки воды определяется свойствами загрязнений и в среднем может изменяться в пределах одной-пяти минут. Учитывая малое расстояние между электродами и возможность засорения электродного пространства, сточные воды перед электрокоагуляцией целесообразно подвергать механической сорбции от крупно диспергированных загрязнений.
На рисунке 3 представлены схемы электрокоагуляционных
установок, а на рисунке 4 показана схема электрокоагулятора-флотатора.
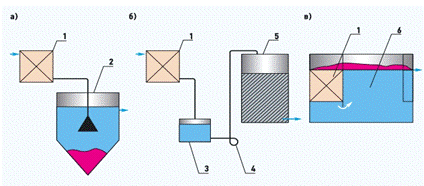
Рисунок 3 - Схемы электрокоагуляционных установок (а - с последующим
отстаиванием, б - с последующим фильтрованием, в - с последующей флотацией; 1 -
электродная камера, 2 - отстойник, 3 - промежуточный бак, 4 - насос, 5 -
фильтр, 6 - флотационная камера)
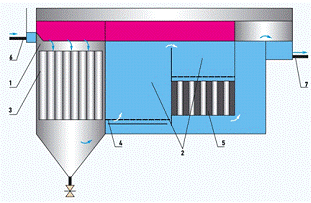
Рисунок 4 - Схема электокоагулятора-флотатора (1 - камера
электрокоагуляции, 2 - камера электрофлотации, 3 - электокоагулятор, 4 -
электроды для электрофлотации (графитовый анод и сетчатый катод), 5 -
электрофлотатор, 6 - сточная вода, 7 - очищенная вода)
5. Процессы при электрокоагуляции
Главной лимитирующей стадией электрокоагуляции является образование катионов металлов - результат электрохимического растворения металлических анодов в соответствии с уравнением:
→ Mn+ + ne-,
где М - символ металла; n - его валентность.
На алюминиевых анодах протекает следующая реакция:
а на анодах из стали идет реакция:
→ Fe2+ + 2e-,
при этом часть катионов железа окисляется под действием растворенного в воде кислорода у анода до трехвалентного железа (III):
+ → Fe3+ + e-.
Второй этап коагуляции сводится к химической
гидратации образующихся катионов металлов, образовании нерастворимых
гидроксидов металлов, их выпадении в осадок (кристаллизации) с последующим
формированием хлопьев, способных флокулировать грубодисперсные примеси воды.
Соответствующие химические реакции происходят в межэлектродном пространстве и
включают несколько этапов:
Al3+ + 3 OH → Al(OH)3+,+ + 3 OH
→ Fe(OH)3+,+ + 2 OH → Fe(OH)2+,(OH)2 + O2 + H2O → Fe(OH)3.
В результате поступления в воду необходимого
количества катионов железа или алюминия за счет приведенных выше реакций
возникает та же ситуация, что и при обработке воды коагулянтами: солями железа
или алюминия. Однако в отличие от применения солевых коагулянтов при
электрокоагуляции вода не обогащается сульфатами или хлоридами, содержание
которых в очищенной воде лимитируется как при сбросе ее в водоемы, так и при
повторном использовании в системах промышленного водоснабжения. Образование в
воде многовалентных катионов понижает устойчивость отрицательно заряженных
коллоидов, так как уменьшается толщина диффузионного слоя коллоидной частицы и
понижается ее потенциал. Устойчивость (стабильность) коллоидов обусловлена
взаимодействием межмолекулярных сил взаимного притяжения и отталкивания, возникающих
на границе соприкосновения двойных электрических слоев (ДЭС) сблизившихся
частиц:
ΔU = U1 - U2,
где U1 и U2 - соответственно силы отталкивания и притяжения.
Если ΔU ≥ 0, укрупнение частиц невозможно, если ΔU ≤ 0 - произойдет слипание частиц, то есть коагуляция.
В электрическом поле создаются особенно благоприятные
условия для коагуляции, чему способствует дополнительно возникающая сила
диполь-дипольного воздействия U3, уменьшающего ДЭС и поляризующего коллоидные
частицы:
ΔU = U1 - U2 - U3.
Процесс коагуляции в электрокоагуляторах протекает значительно интенсивнее, чем при реагентной коагуляции, что объясняется положительным влиянием электрофореза на взаимное укрупнение зародышей частиц гидроксидов металлов и перемешиванием воды выделяющимися на катодах пузырьками водорода. Благоприятные условия электрокоагуляции позволяют уменьшить дозы металла, необходимые для очистки, по сравнению с дозами при реагентной коагуляции на 10-20% и более.
Помимо использования электрокоагуляции для дестабилизации коллоидов и флокуляции грубодисперсных примесей, этот метод применим в схемах очистки воды от катионов тяжелых металлов. Это становится возможным в результате повышения значения рН воды (от 2,3 до 10,4) при электролизе, когда металлы переходят в состояние нерастворимых гидроксидов и осаждаются совместно с гидроксидами железа. Значения рН зависят от концентрации осажденного иона. Большие значения рН относятся к меньшим концентрациям. Если при электролизе повышение рН оказывается недостаточным, необходимо увеличить водородный показатель воды перед электролизером путем подщелачивания за счет добавления в обрабатываемую воду щелочи.
Электрохимическое растворение металлов включает анодное растворение за счет внешнего электрического тока и химическое растворение анодов и катодов. Поэтому на практике выход металлов G по электрическому току может оказаться больше теоретически рассчитанного по формуле, определяемой законами Фарадея, и может составлять 120-130% от теоретического выхода:
= AIcurτ,
где А - электрохимический эквивалент элемента:
= M/(26,8z) г/(А*ч);
- валентность; Icur - сила тока, А; τ - время обработки, ч.
Основными факторами, влияющими на электрохимическое растворение анода, являются: температура, сила и плотность электрического тока, значение рН, солевой состав воды, расстояние между электродами, скорость движения воды между электродами, концентрация взвешенных веществ. Повышение температуры воды при электрокоагуляции увеличивает выход металла по току, так как при этом интенсифицируются химические реакции, в том числе растворения металлов. Однако, положительное влияние роста температур наблюдается только до достижения некоторого температурного максимума (60-80°C), а дальнейшее повышение температуры снижает выход металла. Это объясняется возрастающей интенсивностью пассивации алюминиевого анода за счет уплотнения и набухания коллоидальной гидроокиси алюминия в его микропорах.
Существенное влияние на соотношении количества металла, растворяемого электрохимическим и химическим путем, оказывает и значение рН. При рН = 6-8 в результате электрохимического процесса растворяется до 90% алюминиевых анодов. Химическим способом растворяется около 70% металла при рН=6-8, в том числе 50% при растворении катода. Суммарный выход алюминия по электрическому току возрастает в слабокислой и особенно щелочной среде, достигая 150-200%. Влияние водородного показателя на процесс растворения электродов связано с растворением пассивирующих отложений.
Влияние анионного состава водной среды на растворение анодов главным образом обусловлено условиями пассивации. Эффективным депассивантом является анион хлора (анодная поляризация). Вершины треугольной диаграммы соответствуют 100% содержанию трех основных анионов: хлор (Cl-) -, сульфат (SO42+) - и гидрокарбонат (HCO3- ) - аниона. С уменьшением процентного содержания хлориона в водной среде выход алюминия по току уменьшается.
На процесс химического растворения катода также влияет
катионный состав водной среды. Диаграмма, иллюстрирующая влияние основных
катионов - натрия, кальция и магния на химическое растворение алюминиевого
катода приведена на рис. 3. Катионы натрия оказывают депассивирующее
воздействие на катод. Напротив, катионы магния и особенно кальций, усиливают
пассивацию катода (рис. 3). Другим фактором, оказывающим положительное влияние
на выход катионов металлов, является плотность электрического тока, А/м2:
τ = I/Fэл.
где I - величина электрического тока при электролизе, А; Fэл - площадь анода или катода, м2.
Оптимальными принимаются плотности электрического тока: для алюминиевых электродов, катодная плотность - tк = 10-35 А/м2, анодная - tа = 20-150 A/м2, а для железных электродов tа = tк = 10-100 A/м2.
При плотности тока более 200 А/м2 растворение
электродов сопровождается заметной электрофлотацией и усилением пассивации электродов.
Периодическое переключение полюсов способствует депассивации электродов, что
интенсифицирует их химическое растворение. Экспериментально установлено, что
максимальный выход алюминия по току достигается при переключении полюсов через
каждые 15 минут, то есть четыре раза в час. На выход металла по току влияет и
схема соединения электродов, при этом наибольший выход - при монополярном
соединении.
. Конструкции электрокоагуляторов
Электрокоагуляция осуществляется в специальных генерирующих катионы металла (чаще всего алюминия и железа) электрических приборах - электрокоагуляторах (рисунок 3-4). Основной элемент электрокоагулятора - электродная камера со сменным набором стальных или алюминиевых (дюралюминиевых) электродов чередующейся полярности, в зазорах между которыми (шириной 5-20 мм) протекает обрабатываемая вода со скоростью не менее 0,5 м/с. Как и в электролизерах, в электрокоагуляторах электроды могут располагаться горизонтально или вертикально с зазором 10-16 мм, что зависит от условий размещения и монтажа, а также от расходов обрабатываемой воды. В электрокоагуляторах с меньшими плотностями электрического тока в связи с незначительным пенообразованием можно принимать ширину межэлектродных каналов менее 15 мм, и при обосновании не предусматривать устройств для удаления пены. При больших плотностях электрического тока ширина межэлектродных каналов должна принимается не менее 15-20 мм. Для удаления скоплений пены в каналах предусматриваются различные устройства, в частности, продувка сжатым воздухом.
Аноды и катоды выполняются в виде пластин из алюминия, его сплавов, не содержащих медь, или стали. Подключение пластин к источнику тока может быть параллельным или последовательным. В первом случае все электроды действуют как монополярные, во втором - промежуточные пластины работают биполярно. Последовательное же подключение позволяет работать при меньших значениях электрического тока. Наряду с пластинчатыми иногда используют засыпные электроды из стальной стружки. Несмотря на некоторые преимущества (большая поверхность, низкая стоимость), засыпные электроды применяются редко, поскольку они засоряются гидроксидами металлов и плохо регенерируются. Выбор материала для электродов зависит от технологических особенностей процессов очистки.