Материал: Экологическое состояние родников города Ижевска (на примере Карлутской группы)
![]() +
+![]() R®
R®![]() MgR+2
MgR+2![]()
где R - радикал этилендиаминтетрауксусной кислоты -
![]() NС
NС![]() N(С
N(С![]()
Анализ проводили в аммиачном буферном растворе при рН 10,0-10,5 титриметрическим методом в присутствии индикатора хром темно-синего кислотного [7].
Общую жесткость (![]() ) в ммоль/л экв. вычисляют по формуле:
) в ммоль/л экв. вычисляют по формуле:
![]() =
= ![]()
где: ![]() - объем раствора трилона Б, израсходованного на титрование,
мл;
- объем раствора трилона Б, израсходованного на титрование,
мл;
Н - концентрация титрованного раствора трилона Б, моль/л экв.;
![]() - объем воды, взятой на анализ, мл;
- объем воды, взятой на анализ, мл;
- коэффициент пересчета единиц измерения из моль/л в ммоль/л.
Допустимая величина общей жесткости для питьевой воды источников
нецентрализованного водоснабжения составляет не более 7 ммоль/л экв. (в
отдельных случаях - до 10 ммоль/л экв.), лимитирующий показатель вредности -
органолептический (Муравьев, 2004).
3.3.3 Определение нитратов
Нитраты являются солями азотной кислоты и обычно присутствуют в воде. Нитратобразующие бактерии превращают нитриты в нитраты в аэробных условиях. Под влиянием солнечного излучения атмосферный азот превращается также преимущественно в нитраты посредством образования оксидов азота. Многие минеральные удобрения содержат нитраты, которые при избыточном или нерациональном внесении в почву приводят к загрязнению водоемов. Источниками загрязнения нитратами являются также сточные воды предприятий, поверхностные стоки и т.п (Пименова, 2011).
Повышенное содержание нитратов в воде может служить индикатором загрязнения в результате распространения фекальных либо химических загрязнений. Питьевая вода и продукты питания, содержащие повышенное количество нитратов, могут вызывать заболевания, и в первую очередь у младенцев (так называемая метгемоглобинемия). Вследствие этого расстройства ухудшается транспортировка кислорода с клетками крови и возникает синдром «голубого младенца» (гипоксия) (Пименова, 2011).
Смертельная доза нитратов для человека составляет 8-15 г. Допустимое суточное потребление по рекомендациям ФАО/ВОЗ - 5 мг/кг массы тела. ПДК по нитратам составляет 45 мг/л (Сапожникова, 2009).
Метод основан на реакции нитратов с салициловокислым натрием в присутствии серной кислоты с образованием соли нитросалициловой кислоты, окрашенной в желтый цвет (ГОСТ, 1973).
Содержание нитратов (X), мг/![]() , вычисляют по
формуле в пересчете на нитратный азот (ГОСТ, 1973)
, вычисляют по
формуле в пересчете на нитратный азот (ГОСТ, 1973)
= С,
где С - содержание нитратов, найденное по графику,
мг/![]()
3.3.4 Определение железа общего
Железо - один из самых распространенных элементов в природе. Его содержание в земной коре составляет около 4,7% по массе, поэтому железо с точки зрения его распространенности в природе принято называть макроэлементом. Известно свыше 300 минералов, содержащих соединения железа.
В малых концентрациях железо всегда встречается практически во всех природных водах и особенно - в сточных водах.
Поскольку соединения железа в воде могут существовать в различных формах как в растворе, так и во взвешенных частицах, точные результаты могут быть получены только при определении суммарного железа во всех его формах, так называемого общего железа (Пименова, 2011).
В данной работе для определения общего железа в воде использовали метод
соответствующий ГОСТ 4011. Он является визуально-колориметрическим и основан на
способности катиона железа(II) в
интервале рH 3-9 образовывать с ортофенантролином
комплексное оранжево-красное соединение. Реакцию можно представить схемой
(Муравьев, 2004).
При наличии в воде железа(III), оно восстанавливается до железа(II)
солянокислым гидроксиламином в нейтральной или слабокислой среде:
![]() +2N
+2N![]() ОH´HСl =
ОH´HСl = ![]() +
+![]() +2
+2![]() О+2HСl+2
О+2HСl+2![]()
Таким образом, определяется суммарное содержание железа(II) и железа(III). Анализ проводился в ацетатном буферном растворе где рН 4,5-4,7. Концентрацию железа в анализируемой воде определяли по окраске пробы, визуально сравнивая ее с окраской образцов на контрольной шкале (Муравьев, 2004).
ПДК общего железа в воде водоемов составляет 0,3 мг/л, лимитирующий
показатель вредности - органолептический (Государственный доклад...,2014).
3.3.5 Определение хлоридов
Хлориды присутствуют практически во всех пресных поверхностных и грунтовых водах, а также в питьевой воде в виде солей металлов. Если в воде присутствует хлорид натрия, она имеет соленый вкус уже при концентрациях свыше 250 мг/л; в случае хлоридов кальция и магния соленость воды возникает при концентрациях свыше 1000 мг/л. Именно по органолептическому показателю - вкусу установлена ПДК для питьевой воды по хлоридам (350 мг/л), лимитирующий показатель вредности - органолептический.
Большие количества хлоридов могут образовываться в промышленных процессах концентрирования растворов, ионного обмена, высоливания и т.д., образуя сточные воды с высоким содержанием хлорид-аниона. Высокие концентрации хлоридов в питьевой воде не оказывают токсического воздействия на человека, хотя соленые воды очень коррозионно активны по отношению к металлам, пагубно влияют на рост растений, вызывают засоление почв (Пименова, 2011).
Использованный метод для определения массовой концентрации хлорид-аниона
описан в ГОСТ 1030 и ИСО 9297. Он основан на титровании хлорид-анионов
раствором нитрата серебра, в результате чего образуется суспензия практически
нерастворимого хлорида серебра:
![]() +
+![]()
В качестве индикатора использовался хромат калия, который реагирует с
избытком нитрата серебра с образованием хорошо заметного оранжево-бурого осадка
хромата серебра:
![]() +
+![]() =
=![]()
Данный метод получил название метода аргентометрического титрования.
Титрование можно выполнять в пределах рН 5,0-8,0. Массовую концентрацию
хлорид-аниона (![]() ) в мг/л вычисляют по уравнению:
) в мг/л вычисляют по уравнению:
![]() =
= ![]() ,
,
где: ![]() - объем раствора нитрата серебра, израсходованный на
титрование, мл;
- объем раствора нитрата серебра, израсходованный на
титрование, мл;
Н - концентрация титрованного раствора нитрата серебра с учетом поправочного коэффициента, моль/л экв.;
![]() - объем воды, взятой на анализ, мл;
- объем воды, взятой на анализ, мл;
,5 - эквивалентная масса хлора;
- коэффициент пересчета единиц измерений из г/л в мг/л (Муравьев, 2004).
3.3.6 Определение сульфатов
Сульфаты - распространенные компоненты природных вод. Их присутствие в
воде обусловлено растворением некоторых минералов - природных сульфатов (гипс),
а также переносом с дождями содержащихся в воздухе сульфатов. Последние
образуются при реакциях окисления в атмосфере оксида серы (IV) до оксида серы (VI), образования серной кислоты и ее
нейтрализации (полной или частичной):
2S![]() +
+![]() =2S
=2S![]()
![]() +
+![]() О =
О = ![]() S
S![]()
Сульфаты в питьевой воде не оказывают токсического воздействия на человека, однако ухудшают вкус воды: ощущение вкуса сульфатов возникает при их концентрации 250-400 мг/л (Муравьев, 2004).
Метод определения массовой концентрации сульфат-аниона основан на реакции
сульфат-анионов с катионами бария с образованием нерастворимой суспензии
сульфата бария по реакции:
![]() +
+![]() = BаS
= BаS![]() ¯
¯
О концентрации сульфат-анионов судят по количеству суспензии сульфата
бария, которое определяют турбидиметрическим методом. Предлагаемый, наиболее
простой, вариант турбидиметрического метода основан на измерении высоты столба
суспензии по его прозрачности и применим при концентрациях сульфат-анионов не
менее 30 мг/л. Анализ выполняли в прозрачной воде. Для работы необходим
мутномер - несложное приспособление, которое может быть изготовлено и
самостоятельно. ПДК сульфатов в воде водоемов хозяйственно-питьевого назначения
составляет 500 мг/л, лимитирующий показатель вредности - органолептический
(Муравьев, 2004).
3.4 Социологический опрос населения
Социологический опрос населения проводили для выяснения отношения местного населения к нецентрализованным источникам водоснабжения. Также опрос позволяет определить интенсивность нагрузки отдельных источников, степень информированности местных жителей о качестве воды в них, заинтересованность в получении подобных сведений. Особое внимание следует обратить на родники, пользующиеся наибольшей популярностью. Опрос проводился в период времени с 13:00 до 17:00 часов в выходные дни.
Респондентам задавали следующие вопросы:
1. Какими источниками питьевой воды вы пользуетесь?
а) водопровод <#"905335.files/image033.gif">
Рис.
2. Изменение дебита родников р.Карлутки в течение года
Кислотность
вод исследованных родников изменяется незначительно, в течение года этот
показатель колеблется от 7,1 до 8,4, в среднем составляя 7,6 единиц рH.
Вода щелочная. За пределы норматива СанПиНа (6-9) данные показатели не выходят.
(СанПиН, 2003). Наименьшее значение рH получилось в воде родника № 39
в ноябре и составило 7,0; наибольшее - в воде родников № 29 в июле и № 40 в
сентябре и составило 8,4. Значительные сезонные колебания данного показателя не
наблюдаются. Наглядно можно увидеть на рис. 3
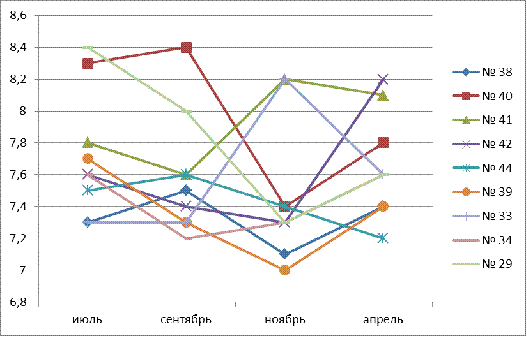
Рис.
3. Сезонные изменения рH родниковой воды источников р.Карлутки
Общая
жесткость воды обусловлена суммарным содержанием ионов кальция и магния.
Показатели жесткости колеблются от 6,6 до 11,6, что превышает норматив СанПиНа
- 7-10 мг-экв/л. (СанПиН, 2003) Превышения нормы зафиксированы в 4 родниках, в
разное время года. Наибольшее значение было обнаружено в воде родника № 42 и
составило - 11,6 мг-экв/л, наименьшее значение в воде родника № 29 составило
6,6 мг-экв/л. Сезонные колебания данного показателя можно наблюдать на рис.4.
Минимальное среднее значение характерно для весеннего периода, что может быть
связано с поступлением талых вод.
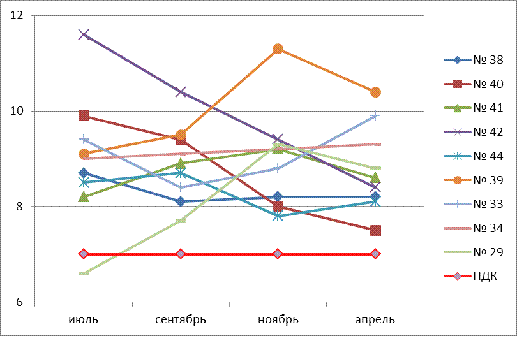
Рис. 4. Сезонные изменения общей жесткости в родниковой воде источников р.Карлутки
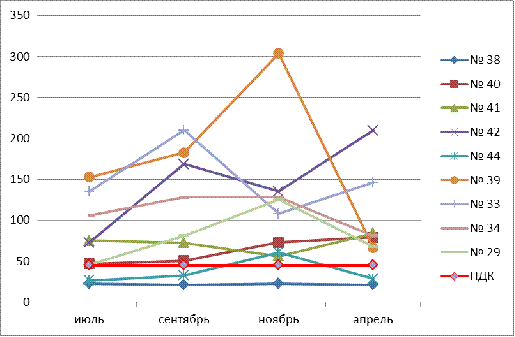
Рис.
5. Сезонные изменения нитратов в родниковой воде источников р.Карлутки
По
содержанию хлоридов и сульфатов в родниковой воде не выявлено превышений. По
нормам СанПиНа содержание хлоридов не должно превышать 350 мг/л, а сульфатов -
500 мг/л. Содержание хлоридов варьируется от 29,4 мг/л в роднике № 38 до 89
мг/л в роднике № 39. Среднее содержание хлоридов составило 54,6 мг/л. Сезонные
изменения выражены слабо. Наиболее высокие средние значения - 58,4 характерны для
июля, вероятно в результате эффекта разбавления дождевыми водами. Наиболее
богат хлоридами родник № 39. Динамику изменений можно увидеть на рис. 6.
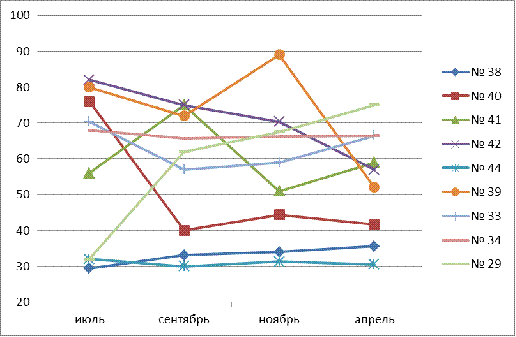
Рис.
6. Сезонные изменения хлоридов в родниковой воде источников р.Карлутки
Количество
сульфатов колеблется от 39,2 мг/л в роднике № 33до 126 мг/л в роднике 39.
Среднее значение по родникам составило 70 мг/л. Наиболее богат сульфатами
родник № 44. Сезонные колебания незначительны, наиболее высокие средние
значения характерны также для июля, что можно наблюдать на рис.7.
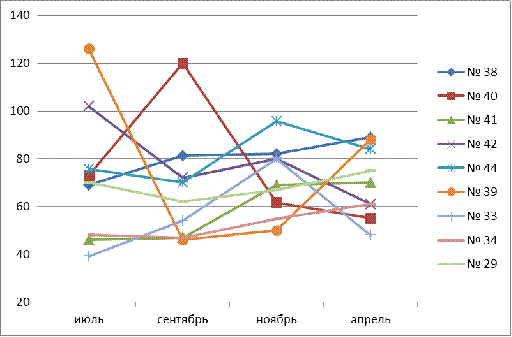
Рис.
7. Сезонные изменения сульфатов в родниковой воде источников р.Карлутки
Содержание
ионов железа не превышает нормативов СанПиН (0,3 мг/л). Сезонных изменений не
выявлено (рис. 8). Среднее значение для всех проб составило 0,07 мг/л.
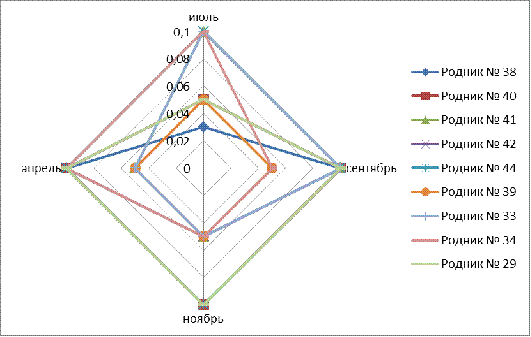
Рис.
8. Сезонные изменения железа общего в родниковой воде источников р.Карлутки
4.2 Результаты социологического опроса
Социологический опрос проводился с целью подтвердить версию об использовании подземных вод города для бытовых нужд. Опрашивались все люди, которые подходили к источнику в период наблюдения. Итого в опросе приняли участие 136 человек.
На вопрос: какими источниками питьевой воды вы пользуетесь?
46 % ответили, что используют и водопроводную и родниковую воду.
% ответили, что используют водопроводную воду. 22% ответили, что используют родниковую воду.
На вопрос: с какой периодичностью вы пользуетесь родниковой водой?
% ответили, что используют воду 1-2 раза в неделю.
% ответили, что используют воду 1-2 раза в месяц.
На вопрос: обладаете ли вы достоверными данными о качестве воды, которой пользуетесь?
% ответили, что нет
% ответили, что имеют некоторые сведения
- На вопрос: какие способы очистки питьевой воды вы используете?
% ответили, что используют фильтрующие устройства
% ответили, что очищают воду кипячением
% ответили, что не используют очистку
Наибольшая рекреационная нагрузка наблюдается на
родники под № 41 в парке Березовая Роща и № 29 в районе остановки «Нефтемаш».
4.3 Рекомендации по
возможному улучшению качества воды в родниках и методов их защиты
Для всех родников остается актуальным вопрос о решении вопроса о развитии нормативно-правовой документации на региональном и муниципальном уровне и паспортизация родников
Минимальные методы защиты населения от потребления некачественной воды, не соответствующей нормам СанПиН возможны через информирование с помощью табличек, районных газет с подробным описанием химического состава каждого родника, а также через предупреждения об обязательном фильтровании и кипячении воды из природных источников.
В целом, санитарное состояние изученных родников не соответствует санитарно-гигиеническим нормам. Водосборный бассейн, каптажные камеры оставляют желать лучшего. В близости от родников находятся завалы веток, бытовой мусор, также они значительно близко расположены от жилых застроек и промышленных объектов, что тоже негативно влияет на их состояние, вследствие этих причин родники становятся источниками загрязнения малых рек, в данном случае Карлутки, в которую впадают все ручьи, а она в свою очередь является загрязнителем реки Иж. По химическим показателям больше других отличается родник №38, уровень нитратов соответствует норме. Вода всех других источников, несмотря на то, что нитраты (так же как сульфаты и хлориды) относятся к III категории токсичности, является потенциально опасной. Высокое содержание нитратов в потребляемой воде может привести к образованию метгемоглобина, вследствие чего наблюдаются признаки удушья, сердечная недостаточность.