Материал: Биологическое значение белка
Биологическое значение белка
Биологическое
значение белка
ОГЛАВЛЕНИЕ
I. СТРОЕНИЕ И СВОЙСТВА АМИНОКИСЛОТ
1.1 Классификация
1.2 Номенклатура
1.4 Получение
1.5 Физические свойства
1.6 Химические свойства
II. УРОВНИ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКОВЫХ МОЛЕКУЛ
III. КЛАССИФИКАЦИЯ БЕЛКОВ
3.1 Характеристика простых белков
3.2 Характеристика сложных белков
IV. БИОЛОГИЧЕСКИЕ ФУНКЦИИ БЕЛКОВ
V. МЕТОДЫ ВЫДЕЛЕНИЯ И АНАЛИЗА БЕЛКА
СПИСОК
ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
I. СТРОЕНИЕ И СВОЙСТВА АМИНОКИСЛОТ
Среди азотсодержащих органических веществ имеются соединения с двойственной функцией. Особенно важными из них являются аминокислоты.
В клетках и тканях живых организмов встречается около 300 различных аминокислот, но только 20 (α-аминокислоты) из них служат звеньями (мономерами), из которых построены пептиды и белки всех организмов (поэтому их называют белковыми аминокислотами). Последовательность расположения этих аминокислот в белках закодирована в последовательности нуклеотидов соответствующих генов. Остальные аминокислоты встречаются как в виде свободных молекул, так и в связанном виде. Многие из аминокислот встречаются лишь в определенных организмах, а есть и такие, которые обнаруживаются только в одном из великого множества описанных организмов. Большинство микроорганизмов и растения синтезируют необходимые им аминокислоты; животные и человек не способны к образованию так называемых незаменимых аминокислот, получаемых с пищей. Аминокислоты участвуют в обмене белков и углеводов, в образовании важных для организмов соединений (например, пуриновых и пиримидиновых оснований, являющихся неотъемлемой частью нуклеиновых кислот), входят в состав гормонов, витаминов, алкалоидов, пигментов, токсинов, антибиотиков и т. д.; некоторые аминокислоты служат посредниками при передаче нервных импульсов.
Аминокислоты - органические амфотерные соединения, в состав которых входят карбоксильные группы - СООН и аминогруппы -NH2.
Аминокислоты можно рассматривать как карбоновые
кислоты, в молекулах которых атом водорода в радикале замещен аминогруппой.
.1 Классификация
Аминокислоты классифицируют по структурным признакам.
. В зависимости от взаимного расположения амино-
и карбоксильной гру гршргрупп аминокислоты подразделяют на α-,
β-, γ-, δ-, ε- и т. д.
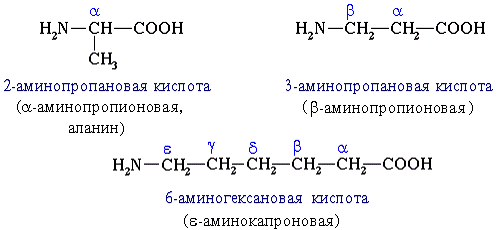
. В зависимости от количества функциональных групп различают кислые, нейтральные и основные.
. По характеру углеводородного радикала различают алифатические (жирные), ароматические, серосодержащие и гетероциклические аминокислоты. Приведенные выше аминокислоты относятся к жирному ряду.
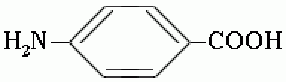
Примером ароматической аминокислоты может
служить пара-аминобензойная кислота:
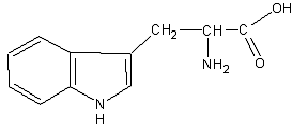
Примером гетероциклической аминокислоты может служить триптофан - незаменимая α- аминокислота:
.2 Номенклатура
По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино- и указанием места расположения аминогруппы по отношению к карбоксильной группе. Нумерация углеродной цепи с атома углерода карбоксильной группы.
Например:
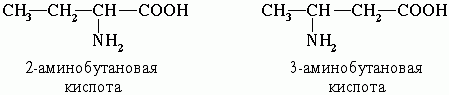
Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставка амино- с указанием положения аминогруппы буквой греческого алфавита.
Пример:
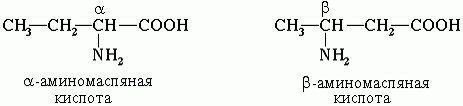
Для α-аминокислот R-CH(NH2)COOH, которые играют исключительно важную роль в процессах жизнедеятельности животных и растений, применяются тривиальные названия.
Если в молекуле аминокислоты содержится две аминогруппы, то в ее названии используется приставка диамино-, три группы NH2 - триамино- и т.д.
Пример:
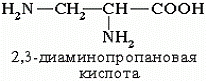
Наличие двух или трех карбоксильных групп отражается в названии суффиксом -диовая или -триовая кислота:
Пример:
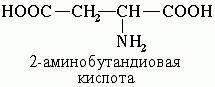
.3 Изомерия
. Изомерия углеродного скелета
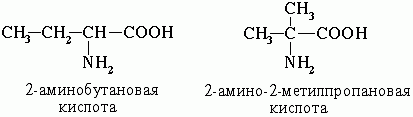
. Изомерия положения функциональных групп
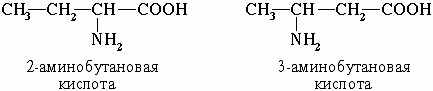
. Оптическая изомерия
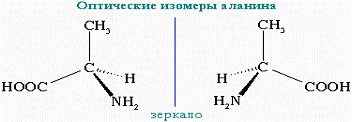
α-аминокислоты, кроме
глицина NН2-CH2-COOH.
.4 Получение
. Из карбоновых кислот по схеме:
2 1
R-CH2-COOH + Cl2 t, hν → R-CH-COOH + HCl (р. замещения)
│
Cl
2-хлоркарбоновая кислота
стадия:
αCH-COOH + 2NH3 → R-CH-COOH + NH4Cl
│ │
Cl NH2
α -аминокарбоновая кислота
2. Гидролиз полипептидов (белков):
CH2-CO-NH-CH-COOH + H2O ↔ CH2-COOH + CH3-CH-COOH
│ │ │ │ CH3 NH2 NH2
глицил-аланин (дипептид) глицин аланин
3. Микробиологический синтез. Известны
микроорганизмы, которые в процессе жизнедеятельности продуцируют α
- аминокислоты
белков.
.5 Физические свойства
.6 Химические свойства
Аминокислоты амфотерные органические соединения, для них характерны кислотно-основные свойства.. Общие свойства
. Внутримолекулярная нейтрализация → образуется биполярный цвиттер-ион:
Водные растворы электропроводны. Эти свойства
объясняются тем, что молекулы аминокислот существуют в виде внутренних солей,
которые образуются за счет переноса протона от карбоксила к аминогруппе:
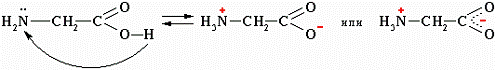
+ --CH2-COOH ↔ NH3-CH2-COO
цвиттер-ион
Водные растворы аминокислот имеют нейтральную, кислую или щелочную среду в зависимости от количества функциональных групп.
. Поликонденсация → образуются полипептиды
(белки):
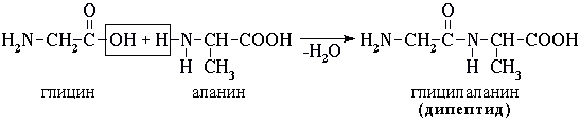
При взаимодействии двух α-аминокислот образуется дипептид.
. Разложение → Амин + Углекислый газ:
-CH2-COOH → NH2-CH3 + CO2↑
. Свойства карбоксильной группы (кислотность)
1. С
основаниями → образуются соли:
NH2-CH2-COOH + NaOH → NH2-CH2-COONa + H2O
натриевая соль аминоуксусной кислоты
2. Со
спиртами → образуются сложные эфиры - летучие вещества (р. этерификации):
NH2-CH2-COOH + CH3OH HCl(газ)→ NH2-CH2-COOCH3 + H2O
метиловый
эфир аминоуксусной кислоты
. С аммиаком → образуются амиды:
NH2-CH(R)-COOH
+ H-NH2
→ NH2-CH(R)-CONH2
+ H2O
. Практическое значение имеет внутримолекулярное
взаимодействие функциональных групп ε-аминокапроновой
кислоты, в результате которого образуется ε-капролактам
(полупродукт для получения капрона):
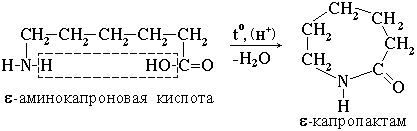
. Свойства аминогруппы (основность)
. С сильными кислотами → соли:
HOOC-CH2-NH2 + HCl → [HOOC-CH2-NH3]Cl
или
HOOC-CH2-NH2*HCl
. С азотистой кислотой (подобно первичным
аминам):
NH2-CH(R)-COOH + HNO2 → HO-CH(R)-COOH + N2↑+ H2O
гидроксокислота
Измерение объёма выделившегося азота позволяет определить количество аминокислоты (метод Ван-Слайка) . Качественная реакция
. Все аминокислоты окисляются нингидрином с образованием продуктов сине-фиолетового цвета!
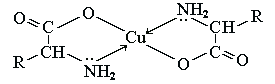
. С ионами тяжелых металлов α-аминокислоты
образуют внутрикомплексные соли. Комплексы меди (II), имеющие глубокую синюю
окраску, используются для обнаружения α-аминокислот.
II. УРОВНИ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКОВЫХ
МОЛЕКУЛ
Последовательность чередования аминокислотных
остатков в полипептидной цепи называется первичной структурой белка (или первым
уровнем структурной организации белковой молекулы).

Закручивание полипептидной цепи белка в спиралеобразную структуру (α-спираль) происходит вследствие взаимодействия посредством образования водородных связей между кислородом карбонильной группы i-го аминокислотного остатка и водородом амидогруппы i+4 аминокислотного остатка.
Наряду со спирализованными участками в
образовании вторичной структуры белка принимают также участие β-структуры
параллельная и антипараллельная, и β-изгиб.

При упаковке вторичной структуры белка в пространстве образуется третичная структура белка, состоящая из всех компонентов вторичной структуры. При образовании третичной структуры белка происходят гидрофобные, ионные (электростатические), водородные ковалентные взаимодействия между группировками в боковых радикалах аминокислотных остатков полипептидной цепи.
С появлением третичной структуры у белка
появляются и новые свойства - биологические. В частности, проявление
каталитических свойств связано именно с наличием у белка третичной структуры. И
наоборот, нагревание белков, приводящее к разрушению третичной структуры (иначе
известно как денатурация) одновременно приводит к утрате биологических свойств.

Четвертичная структура белка подразумевает такое
объединение белков третичной структуры, при котором появляются новые
биологические свойства, не характерные для белка в третичной структуре. Каждый
из белков - участников третичной структуры - при образовании четвертичной
структуры называют субъединицей или протомером. В образовании четвертичной
структуры белка принимают участие те же связи, что и при образовании третичной
структуры, за исключением ковалентных.

Объединение белковых молекул третичной структуры без появления новых биологических свойств называют агрегированным состоянием.
Биологический смысл появления четвертичной структуры у белков - экономия «генетического материала», поскольку каждая из субъединиц кодируется только одним геномом ДНК. К тому же, в случае появления ошибки при трансляции у одной из субъединиц, отпадает необходимость ресинтеза остальных субъединиц. Четвертичная структура в таком случае распадается на субъединицы, дефектная субъединица удаляется и вновь образуется четвертичная структура с участием нормальной субъединицы. В конце концов, появление ошибки менее вероятно при синтезе (трансляции) сравнительно небольшой полипептидной цепи.
Практически все белки-ферменты имеют
четвертичную структуру и состоят, как правило, из четного числа протомеров
(двух, четырех, шести, восьми).
III. КЛАССИФИКАЦИЯ БЕЛКОВ
В организме человека содержится свыше 50 000 индивидуальных белков, отличающихся первичной структурой, конформацией, строением активного центра и функциями. Однако до настоящего времени нет единой и стройной классификации, учитывающей различные особенности белков. В основе имеющихся классификаций лежат разные признаки. Так белки можно классифицировать:
• по форме белковых молекул (глобулярные - округлые или фибриллярные - нитевидные)
• по молекулярной массе (низкомолекулярные, высокомолекулярные)
• по выполняемым функциям (транспортные, структурные, защитные, регуляторные и др.)
• по локализации в клетке (ядерные, цитоплазматические, лизосомальные и др.)
• по структурным признакам и химическому составу
белки делятся на две группы: простые и сложные. Простые белки представлены
только полипептидной цепью, состоящей из аминокислот. Сложные белки имеют в
своем составе белковую часть и небелковый компонент (простетическую группу).
Однако и эта классификация не является идеальной, поскольку в чистом виде
простые белки встречаются в организме редко.
.1 Характеристика простых белков
белок аминокислота карбоксильный
К простым белкам относят гистоны, протамины, альбумины и глобулины, проламины и глютелины, протеиноиды.
Гистоны - тканевые белки многочисленных организмов, связаны с ДНК хроматина. Это белки небольшой молекулярной массы (11-24 тыс.Да). По электрохимическим свойствам относятся к белкам с резко выраженными основными свойствами (поликатионные белки), ИЭТ у гистонов колеблется от 9 до 12. Гистоны имеют только третичную структуру, сосредоточены в основном в ядрах клеток.
Основная функция гистонов - структурная и регуляторная. Структурная функция состоит в том, что гистоны участвуют в стабилизации пространственной структуры ДНК, а следовательно, хроматина и хромосом. Регуляторная функция заключается в способности блокировать передачу генетической информации от ДНК к РНК.
Протамины - своеобразные биологические заменители гистонов, но отличаются от них составом и структурой. Это самые низкомолекулярные белки (М - 4-12 тыс. Да), обладают резко выраженными основными свойствам из-за большого содержания в них аргинина (80%).
Как и гистоны, протамины - поликатионные белки. Они связываются с ДНК в хроматине спермиев и находятся в молоках рыб.
Сальмин - протамин из молоки лосося.
Скумбрин - из молоки скумбрии.
Протамины делают компактной ДНК сперматозоидов, т.е. выполняют как и гистоны, структурную функцию, однако не выполняют регуляторную.
Альбумины и глобулины.
Альбумины (А) и глобулины (Г).
А и Г белки, которые есть во всех тканях. Сыворотка крови наиболее богата этими белками. Содержание альбуминов в ней составляет 40-45 г/л, глобулинов 20-30 г/л, т.е на долю альбуминов приходится более половины белков плазмы крови.
Характерным свойством альбуминов является их высокая адсорбционная способность. Они адсорбируют полярные и неполярные молекулы, выполняя транспортную роль. Это неспецифические переносчики они транспортируют гормоны, холестерол, билирубин, лекарственные вещества, ионы кальция. Связывание и перенос длинноцепочных жирных кислот - основная физиологическая функция сывороточных альбуминов. Альбумины синтезируются преимущественно в печени и быстро обновляются, период их полураспада 7 дней.
Глобулины - белки с большей, чем альбумины молекулярной массой. Глобулины слабокислые или нейтральные белки ( ИЭТ = 6 - 7,3 ). Некоторые из глобулинов обладают способностью к специфическому связыванию веществ (специфические переносчики).