Курсовая работа (т): Анализ процесса термоконтактного крекинга на примере установки непрерывного коксования в псевдоожиженном слое
Анализ процесса термоконтактного крекинга на примере установки непрерывного коксования в псевдоожиженном слое
МИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательно учреждение
высшего профессионального образования
"Пензенский
государственный технологический университет"
КУРСОВАЯ РАБОТА
по дисциплине: "Химия и технология нефти и газа"
Тема:
"Анализ процесса термоконтактного крекинга на примере установки
непрерывного коксования в псевдоожиженном слое"
Студентки
Дендеря Екатерины Юрьевны
обучающейся в группе 10/2н
по специальности: 240404.51
"Переработка нефти и газа"
Пенза, 2014
Оглавление
Введение
. Технологическая часть
.1 Назначение и характеристика процесса
.2 Теоретические основы процесса
.3 Характеристика сырья и готовой продукции
.4 Описание технологической схемы
.5 Устройство и принцип работы оборудования
. Охрана окружающей среды
.Охрана труда
Заключение
Список используемых источников
Введение
Под термическими процессами подразумевают процессы химических превращений нефтяного сырья - совокупности реакций крекинга (распада) и уплотнения, осуществляемые термически, то есть без применения катализаторов.
Коксование - длительный процесс термолиза тяжелых остатков или ароматизированных высококипящих дистиллятов при невысоком давлении и температурах 470 - 540 °С. Основное целевое назначение коксования - производство нефтяных коксов различных марок в зависимости от качества перерабатываемого сырья. Побочные продукты коксования - малоценный газ, бензины низкого качества и газойли.
Процесс замедленного коксования является одним из самых динамично развивающихся в мировой нефтепереработке. В настоящее время мировые мощности коксования нефтяных остатков составляют 252,9 млн. тонн в год и за последние 6 лет они возросли на 47,3 млн. тонн в год.
В мировой практике наибольшим производственным потенциалом процессов коксования обладает Северо-Американский регион, и в частности промышленность Соединенных Штатов Америки - 53,9 % мировых мощностей коксования. С 1999 г. по 2005 г. мощности коксования в США возросли с 117,7 млн. тонн в год до 136,3 млн. тонн в год, при этом выработка кокса составляет 54 млн. тонн в год. Следует отметить, что мировое потребление кокса в алюминиевой промышленности и электрометаллургии находится на уровне 14 млн. тонн в год, поэтому в настоящее время основным назначением процесса замедленного коксования является получение в качестве целевого продукта газойлей для производства моторных топлив и углубление переработки нефти.
Помимо США, ведущие позиции среди стран мира занимают также: Китай - 15,4 млн. тонн в год (или 7,4% от мировых мощностей), Венесуэла - 8,8 млн. тонн в год (3,5%), Германия - 5,7 млн. тонн в год (2,3%), Япония и Россия по 5,3 млн. тонн в год (2,1%).
Доля процессов коксования нефтяных остатков по отношению к первичной переработке нефти в целом по миру в настоящее время составляет 6,1% и за последние 6 лет возросла на 0,9%. С 1999 г. по 2005 г. мировые мощности коксования возросли на 23,0% и их темпы роста значительно опережают темпы роста мощностей первичной переработки нефти (3,4%), что естественно приводит к экономии сырой нефти для производства моторных топлив.
Популярность замедленного коксования во всем мире связана с тем, что наряду с получением нефтяного кокса в процессе реализуется целый ряд технологий, которые и обеспечивают его широкое применение в производстве моторных топлив:
. В процессе замедленного коксования обеспечивается высокоэффективная термодеасфальтизация нефтяных остатков. Если исходное сырье имеет коксовые числа 25-30% и более, то продукты коксования не более 0,3-0,5%.
. На установках происходит деметализация нефтяного сырья. При исходном содержании металлов до 300 и более ppm, в продуктах коксования содержание их не превышает 3-5 ppm, а 95-98 % переходит в кокс.
. Процесс замедленного коксования является самым мощным "санитаром" на НПЗ. Многие образующиеся нефтешламы и другие отходы перерабатываются на установках, при этом получается топливный кокс, газообразные и жидкие продукты коксования, пригодные для производства моторных топлив.
. Наличие установки высокой производительности в схеме завода позволяет наиболее быстро адаптироваться к изменению состава перерабатываемой нефти, поскольку коксовые числа продуктов коксования и содержание в них металлов практически одинаковы как при переработке мазутов так и при переработке асфальтов, как малосернистых так и высокосернистых нефтей.
. При использовании нефтяного кокса в качестве энергетического топлива резко снижается загрязнение окружающей среды. Например, при сжигании 6 млн. тонн топочного мазута с содержанием серы 3% масс. в окружающую среду выбрасывается 360 тыс. т/год сернистых соединений. При коксовании такого же количества мазута образуется около 700 тыс. т/год нефтяного кокса с содержанием серы ~3,5% масс., при сжигании которого образуется 49 тыс. т/год сернистых соединений, что значительно ниже объема выбросов в окружающую среду при сжигании мазута. Это обстоятельство используется заводами и многие строят собственные энергетические установки используя кокс в качестве топлива.
В США около 30 тепловых электростанций переведено на сжигание нефтяного кокса в смеси с каменным углем, что полностью решает проблему сбыта нефтяного кокса, гарантирует круглогодичную бесперебойную работу заводов, так как кокс может храниться долго и проблема вывоза не столь актуальна по сравнению с проблемой вывоза мазута, когда при заполнении резервуарных парков приходится снижать производительность завода. Для отгрузки можно организовать склад, обеспечивающий годичный объем хранения кокса.
. На установках замедленного коксования можно перерабатывать сырье с широким диапазоном свойств от дистиллятов до гудронов, крекинг-остатков, асфальтов, битуминозных песков, продуктов нефтехимии, углехимии и ожижения углей.
Все вышеперечисленное и делает процесс перспективным, наиболее дешевым и экономически привлекательным в производстве моторных топлив из тяжелых нефтяных остатков, хотя существует еще ряд процессов, позволяющих перерабатывать нефтяные остатки в моторные топлива.
1. Технологическая часть
1.1 Назначение и краткая характеристика процесса
Среди термических процессов наиболее широкое распространение в нашей стране и за рубежом получил процесс замедленного коксования, который позволяет перерабатывать самые различные виды ТНО с выработкой продуктов, находящих достаточно квалифицированное применение в различных отраслях народного хозяйства. Другие разновидности процессов коксования ТНО - периодическое коксование в кубах и коксование в псевдоожиженном слое порошкообразного кокса - нашли ограниченное применение.
Основное целевое назначение УЗК - производство крупнокускового нефтяного кокса. Наиболее массовыми потребителями нефтяного кокса в мире и в нашей стране являются производства анодной массы и обожженных анодов для алюминиевой промышленности и графитированных электродов для электросталеплавления. Широкое применение находит нефтяной кокс при изготовлении конструкционных материалов, в производствах цветных металлов, кремния, абразивных (карбидных) материалов, в химической и электротехнической промышленностях, космонавтике, в ядерной энергетике и др.
Кроме кокса, на УЗК получают газы, бензиновую фракцию и коксовые (газойлевые) дистилляты. Газы коксования используют в качестве технологического топлива или направляют на ГФУ для извлечения пропан-бутановой фракции - ценного сырья для нефтехимического синтеза. Получающиеся в процессе коксования бензиновые фракции (5 -16% масс.) характеризуются невысокими октановыми числами (=60 по м.м.) и низкой химической стабильностью, повышенным содержанием серы (до 0,5 % масс.) и требуют дополнительного гидрогенизационного и каталитического облагораживания. Коксовые дистилляты могут быть использованы без или после гидрооблагораживания как компоненты дизельного, газотурбинного и судового топлив или в качестве сырья каталитического или гидрокрекинга.
.2 Теоретические основы процесса
Термолиз углеводородов происходит по гомолетическому механизму.
При гомолитическом разрыве пара электронов, принадлежащая ранее двум
связываемым атомам, поровну распределяется между ними:
Y - X →Y' + 'X
где Y-X - валентно-насыщенная молекула; Y', 'X - два свободных радикала.
СН3°- СН3°↔ СН3° + СН3°
СН3 -СН2°°Н ↔ СН3-СН2°
+ °Н
Гомолитический разрыв происходит чаще всего при термических превращениях углеводородов.
Радикалы, являясь химически ненасыщенными частицами, обладают исключительно высокой реакционной способностью и мгновенно вступают в различные реакции.
Радикалы высокой молекулярной массы
термически нестабильные и распадаются с образованием низкомолекулярного более
устойчивого радикала, в том числе водородного:
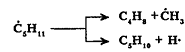
Концентрация радикалов в реакционной системе обычно невелика, и вероятность их столкновения между собой ничтожно мала. При термолизе более значительно преобладают взаимодействия между радикалом и молекулами исходного сырья. Поскольку радикал имеет свободный неспаренный электрон, то его реакция с молекулами, все электроны которых спарены, должна в силу принципа неуничтожимости свободной валентности привести к образованию нового вторичного радикала. Если последний не является малоактивным, то он, в свою очередь, вступит в реакцию с новой молекулой сырья и т.д.Так как число радикалов, могущих образоваться при термолизе, велико, на некоторой стадии образуется радикал, принимавший участие в одной из предыдущих стадий, и возникает регулярное чередование двух или более последовательно параллельных элементарных реакций с образованием конечных продуктов. Этот процесс продолжится до тех пор, пока радикал не "погибнет". Реакции такого типа называются цепными.
1.Зарождение цепи (образование свободных радикалов).
При термическом распаде всех алканов, начиная с этана, зарождение цепи
происходит в результате разрыва связи С - С. При этом образуются свободные
радикалы:
СН3-СН2- СН3 → СН3-СН2°+
СН3°
В случаи алканов с большими числом атомов углерода при не очень высоких температурах крекинга (350-450°С), разрыв углеродной цепи происходит посередине, т.е. по наиболее слабым связям С - С. При более высоких температурах могут рваться и другие С - С связи. Значительно менее вероятен при зарождении цепи разрыв С-Н связей углеводородов, и он возможен только для низших алканов (этан, пропан) при соударении молекул со стекой реактора при высоких температурах. Так как молекулы атома водорода являются внешними атомами в молекулах, то при соударении со стенкой реактора может произойти отрыв атома водорода:
СН3- СН2│Н → СН3-СН2°
+Н°
. Продолжение цепи (реакции свободных радикалов).
Свободные радикалы обладают высокой реакционной способностью, так как содержат неспаренный электрон. Поэтому они стремятся стабилизироваться и подвергаются различным превращениям. Реакции радикалов с молекулами углеводородов являются основными, приводящими к развитию цепи.
Низшие свободные радикалы (атомарный Н, СН3°, С2Н5°)
при столкновении с молекулами алканов отбирают у них атомы водорода.
СН3° + СН3-СН2- СН3 → СН4 + СН3-СН°- СН3
СН3-СН2° + СН3-СН2- СН3 → СН3- СН3 + СН3-СН°- СН3
СН3-СН2° → СН2 = СН2 + Н°
СН3-СН°- СН3 → СН3 = СН - СН3 + Н°
СН3-СН2- СН3 + Н° → СН3-СН°-
СН3 + Н2
. Обрыв цепи. Квадратичный обрыв происходит при взаимодействии двух
радикалов. Он характерен для жидкофазных реакций.
СН3°+ СН3° → СН3 - СН3
СН3° + СН3-СН2° →
СН3-СН2- СН3
Линейный обрыв цепи чаще встречается при газофазных реакциях. Он происходит при адсорбции свободных радикалов на стенки или другой твёрдой поверхности либо на ингибиторах.
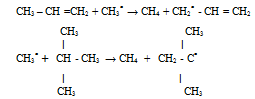
В случаи олефина стабилизация радикала происходит за счёт эффекта сопряжения двойной связи, а в случаи изопарафина - индукционного эффекта метильных групп.
Термолиз алканов приводит преимущественно к образованию более термостойких
низкомолекулярных алкенов и алканов. Из алканов наибольшей термостабильностью
обладает метан. Его термическая деструкция термодинамически возможна при
температуре выше 560 °С. С заметной скоростью распад метана протекает при
температуре выше 1000°С. Высокая термостабильность метана объясняется тем, что
в его молекуле отсутствуют связи С-С, энергия разрыва которых меньше, чем для
связей С-Н. При высокотемпературном пиролизе метана, кроме водорода (и пироуглерода),
образуются этилен, этан, ацетилен и арены. Синтез этих продуктов можно выразить
следующей схемой:
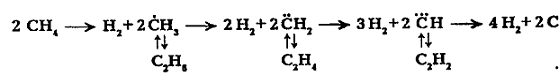
Ароматические углеводороды образуются в результате вторичных реакций синтеза из ацетилена и этилена.
Этан менее устойчив, чем метан: его
деструкция начинается при температуре = 500°С. При пиролизе этана образуются
преимущественно этилен и водород, а также метан и жидкие продукты, богатые
аренами и алкенами.
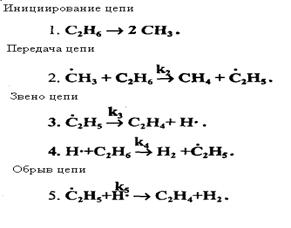
Чередование элементарных реакций (3) и (4) даёт реакцию распад этан по
стереохимическому уравнению:
![]()
Пропан и бутан термически менее устойчивы, чем этан. Пропан
начинает разлагаться при 460 °С, а н-бутан и изобутан - около 435°С. Основные
направления пиролиза пропана:
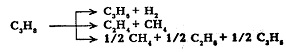
Начиная с бутана, при термолизе алканов преобладающим становится распад по связи С-С.
Относительная скорость их термолиза возрастает с увеличением молекулярной массы, что обусловливается уменьшением энергии разрыва С-С-связей по мере приближения к середине цепи и увеличения степени разветвленности молекул.
В процессе пиролиза н-бутана
преобладают следующие 2 реакции его распада:
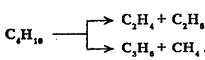
Характерно, что чем выше температура пиролиза бутана, тем больше отодвигается место его распада по С-С-связи к краю молекулы. На это указывает непрерывное возрастание содержания метана в газообразных продуктах реакции вплоть до 900°С. Аналогичные реакции распада характерны для термолиза более высокомолекулярных алканов. Для них при умеренных температурах (400 - 500 °С) наблюдается симметричный разрыв молекулы с образованием олефина и парафина приблизительно одинаковой молекулярной массы.При более высоких температурах в продуктах их термолиза обнаруживаются низшие алканы и высокомолекулярные алкены и арены, вероятно, как результат вторичных реакций.