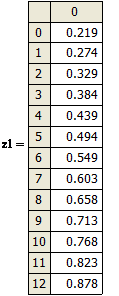Материал: Адсорбционная очистка газов
p' - парциальное давление паров дихлорэтана в газовой смеси;
β = 1,31 - коэффициент аффинности.
i=0…9,
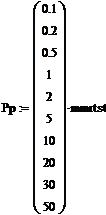
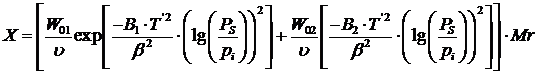
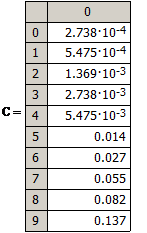
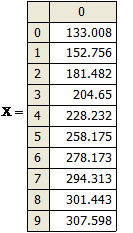
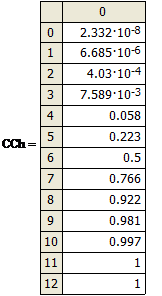
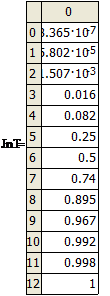
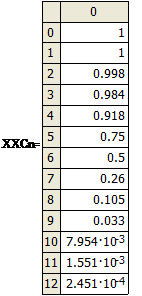
Вычисленные
равновесные концентрации дихлорэтана в активном угле представлены ниже
|
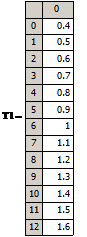
Парциальное давление паров дихлорэтана p’, Па |
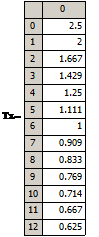
Концентрация дихлорэтана в газе C’, кг/м3 |
Равновесная концентрация дихлорэтана АУ X, кг/кг |
|
|
|
|
Ниже приведена изотерма адсорбции активным углем при 200C.
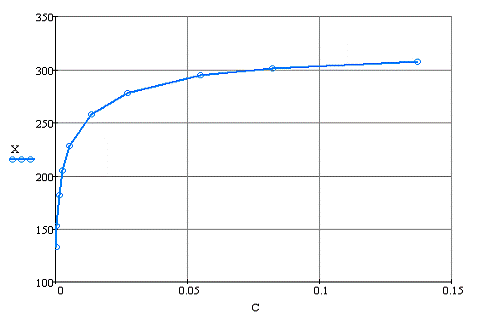
Рис. 2.1 - Изотерма адсорбции
Согласно рекомендациям начальный участок изотермы может рассматриваться
как линейный при условии
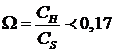 (по
бензолу)
(по
бензолу)
где
![]() - концентрация насыщенного пара дихлорэтана.
- концентрация насыщенного пара дихлорэтана.
Отношение
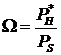 , соответствующее исходной концентрации дихлорэтана в
смеси, может быть найдено по уравнению потенциальной теории адсорбции:
, соответствующее исходной концентрации дихлорэтана в
смеси, может быть найдено по уравнению потенциальной теории адсорбции:
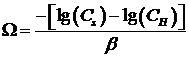
![]()
где
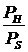 - отношение парциального давления к давлению
насыщенного пара бензола.
- отношение парциального давления к давлению
насыщенного пара бензола.
.3 Диаметр и высота адсорбера
Допустимую фиксированную скорость газа можно рассчитать по формуле,
полученной на основе технико-экономического анализа работы адсорберов,
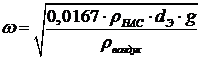 ,
,
где dэ=1,5×10-3 м; ρНАС=575 кг/м3 (для активного угля АР-A); ρвоздух=0,611 кг/м3 - плотность воздуха при t=200C.
Допустимая скорость газа в адсорбере ω=0,48 м/с.
Рабочую скорость примем на 25% ниже допустимой:
![]() ,
, ![]()
Диаметр
аппарата:
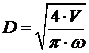 ,
,
=7,0 м.
Принимаем вертикальный адсорбер диаметром 7 м.
Высоту слоя активного угля для обеспечения достаточного времени работы адсорбера примем z=0,7 м ( в вертикальных адсорберах ВТР высота слоя адсорбента составляет 0,5-1,2 м). Общую высоту цилиндрической части принимаем равной Z=1,7 м.
Дополнительная высота (под крышкой и над днищем) необходима для размещения распределительного устройства для газа, штуцеров и датчиков контрольно-измерительных приборов.
.4 Коэффициент массопередачи
Находим коэффициент диффузии в главной фазе в системе дихлорэтан - воздух.
При T0=273,15 К и P735=9,8×104 Па коэффициент диффузии в
условиях адсорбента:
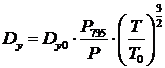 ,
,
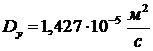 .
.
Вязкость
воздуха при 00C и P735=9,8×104 Па,
μ0=17,3 Па×с, постоянная Сатерленда C'=124.
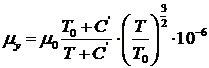 ,
,
μy=1,831×10-5 кг/(м×с).
Вязкость газовой фазы (воздуха) μy=1,831×10-5 кг/(м×с).
Коэффициент
массоотдачи в газовой фазе находим по уравнению:
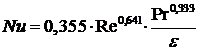 ,
,
где ε - порозность слоя (ε=0,3);
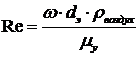 ;
; 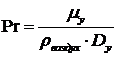 .
.
Подставив в выражение для Nu значения Re=18,5 и Pr=2,1, получим
Nu=9,68.
Тогда
коэффициент внешней массоотдачи:
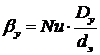 ,
, ![]() .
.
Концентрация
поглощаемого компоненте в поглотителе X_CH равновесная по отношению к Cн=8×10-3 кг/м3, может быть определена, если определить
парциальное давление поглощаемого компонента в газовой фазе:
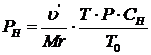 , PH=388,658 Па;
, PH=388,658 Па;
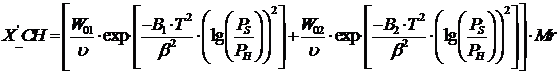 ,'_CH=0,19.
,'_CH=0,19.
Коэффициент
внутренней массотдачи в адсорбенте (коэффициент внутренней массоотдачи) находим
по уравнению:
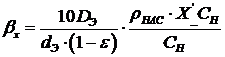 ,
,
βx = 0,049 м/с.
Коэффициент массопередачи:
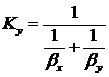 ,
,
![]() .
.
Снижение
движущей силы массопереноса в результате отклонения движения от режима
идеального вытеснения учтем введением дополнительного диффузионного
сопротивления продольного перемешивания. Коэффициент, учитывающий продольное
перемешивание, определяем по уравнению:
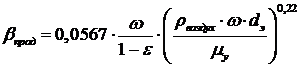 ,
,
βпрод=0,055 м/с.
Коэффициент
массопередачи с учетом продольного перемешивания:
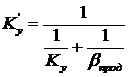 ,
,
![]()
Удельная
поверхность адсорбента:
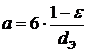 , a= 2,8 ×103 м2/м3.
, a= 2,8 ×103 м2/м3.
Объемный коэффициент массопередачи
Kyv = K’y×a, Kyv = 56,93
.5 Продолжительность адсорбции. Выходная кривая. Профиль концентрации в слое адсорбента
Продолжительность адсорбции дихлорэтана определяется по выходной кривой,
построение которой производится по уравнению Томаса для безразмерной
концентрации в потоке:
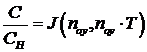 ,
,
где
![]() - общее число единиц переноса для слоя высотой z;
- общее число единиц переноса для слоя высотой z;
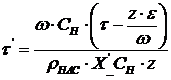 -
,безразмерно время.
-
,безразмерно время.
Выразим τ через безразмерное время τ”:
J=0…12, ![]() ;
; 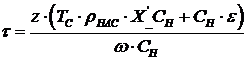 ;
;
![]() .
.
Число единиц переноса noy=110,49. Значение функций J(α,γ) найдем по следующим приближенным формулам
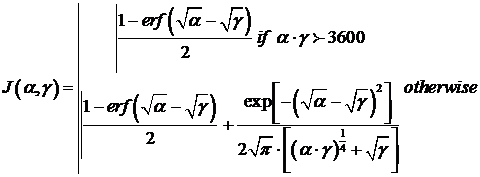
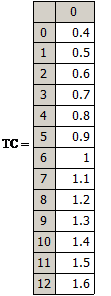
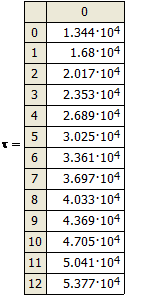
Результаты
расчета выходной кривой адсорбции приведены ниже
|
T |
τ |
C/CH |
|
|
|
|
![]()
![]()
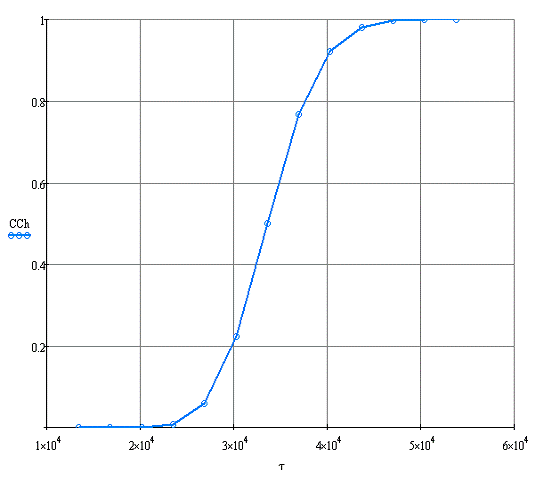
Рисунок 2.2 - Выходная кривая адсорбции (z=0,7 м)
Время достижения концентрации дихлорэтана в газе, выходящем из адсорбера (она составляет С/СH=0,05), равно длительности стадии адсорбции. В соответствии с выходной кривой (см. рис. 2.2) продолжительность адсорбции составляет θ=1,13×105 с.
Построение профиля концентраций ведет по уравнению Томаса, записанному
для безразмерной концентрации в адсорбенте,
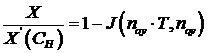 .
.
Выразим расстояние z от точки ввода смеси до точки с концентрацией X в виде функции от безразмерно го времени
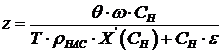 .
.
![]() ;
;
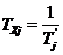 ,
,
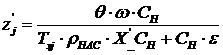 ,
,
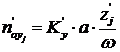 ,
,
![]() .
.
Расчет
профиля концентраций дихлорэтана в слое угля представлен ниже
|
1/T |
T |
z, м |
noy×T |
J(noyT, noy) |
X/X’(CH) |
|
|
|
|
|
|
|
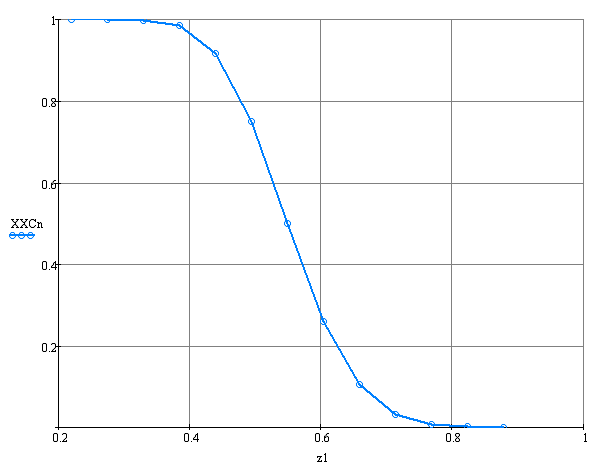
Рисунок. 2.3 - Профиль концентрации в адсорбенте
.6 Материальный баланс
Материальный баланс по дихлорэтану стадии адсорбции выражается
уравнением:
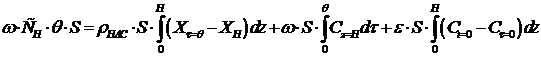
Записывается
уравнение материального баланса для концентраций в безразмерной форме, а также
учитывая, что XH=0 м и Cθ=0 c, получим
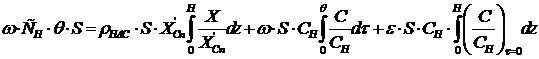
Значение
интегралов уравнения материального баланса определяется графическим
интегрированием выходной кривой (рис. 2.2) и профиля концентрации в адсорбенте
(рис. 2.3):
![]()
![]()
![]()
![]()
![]()
![]()
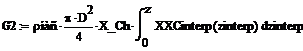
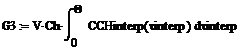
![]() =375,564 кг; G2=375,258 кг; G3=1,446 кг; G4=20,04×10-3 кг.
=375,564 кг; G2=375,258 кг; G3=1,446 кг; G4=20,04×10-3 кг.
Проверим сходимость материального баланса:
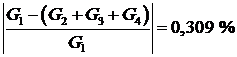 .
.
Ввиду малого количества адсорбтива, остающегося в аппарате в газовой фазе, для расчета массы дихлорэтана, оставшейся в свободном объеме адсорбера, примем концентрацию дихлорэтана, равную начальной.
.7 Вспомогательные стадии цикла
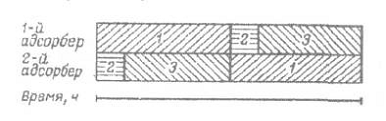
Ввиду того что по заданию установка включает два адсорбера, суммарная продолжительность вспомогательных операций (десорбция, сушка, охлаждение) должна быть равна продолжительности адсорбции, т. е. 4,8 ч.
Десорбция водяным паром-сложный тепломассообменный процесс, протекающий при переменных температуре и расходе паровой фазы. Надежных методик расчета продолжительности десорбции для этого случая неразработано. Продолжительность десорбции в рекуперациоиных установках ориентировочно составляет 0,5... 1,0 ч при условии использования острого пара давлением 0,1 ...0,4 МПа.
При десорбции веществ с небольшой молекулярной массой давление ближе к
минимальному значению указанного интервала. С учетом сказанного принимаем
продолжительность десорбции 1 ч, давление водяного пара 0,2 МПа. Тогда
продолжительность стадий сушки и охлаждения равна 3,8 ч, причем периоды сушки и
охлаждения могут быть приняты равными. В связи с этим условия сушки и
охлаждения должны быть выбраны исходя из указанного времени.
Заключение
На современном этапе для большинства промышленных предприятий очистка вентиляционных выбросов от вредных веществ является одним из основных мероприятий по защите воздушного бассейна.
В настоящее время используются различные методы улавливания и обезвреживания паро- и газообразных веществ из воздуха. На практике применяют следующие способы очистки газа: абсорбционный, адсорбционный, каталитический, термический.
Абсорбция - наиболее распространенный процесс очистки газовых смесей во многих отраслях, в том числе и в химической промышленности. Абсорбция - массообменный процесс очистки газа или парогазовой смеси, при котором происходит поглощение веществ из газа (обычно из газовой смеси) или жидкости жидкостями или - реже - твердыми телами.
Выбрать оптимальное контактное устройство для абсорбционной колонны из большого разнообразия типов тарелок довольно сложно. Решетчатые тарелки, в отличие от других типов тарелок, могут работать с высокими нагрузками по жидкости и газу. Они обладают минимальным гидравлическим сопротивлением и минимальной металлоемкостью, удобны для монтажа, осмотра, чистки и ремонта, менее других конструкций подвержены воздействию агрессивных сред, могут работать со взвесями. Однако устойчивый режим барботажа газа через слой жидкости, находящейся на решетчатой тарелке, возможен только в узком диапазоне скоростей. Это не позволяет использовать их при переменных нагрузках, что важно при обработке газовых выбросов.
дихлорэтан активный уголь адсорбер
Библиографический список
1. Баранцев В.И. Сборник задач по процессам и аппаратам пищевых производств. - М.: Агропромиздат, 1985.
2. Ветошкин А.Г. Процессы и аппараты защиты атмосферы от газовых выбросов: Учебное пособие по проектированию. - Пенза: Изд-во Пенз. технол. ин-та, 2003. - 163 с.
. Плановский А.Н. Процессы и аппараты химической технологии. - М.: Химия, 1987. - 540 с.
. Рамм В.М. Адсорбция газов. - М.: Химия, 1976.