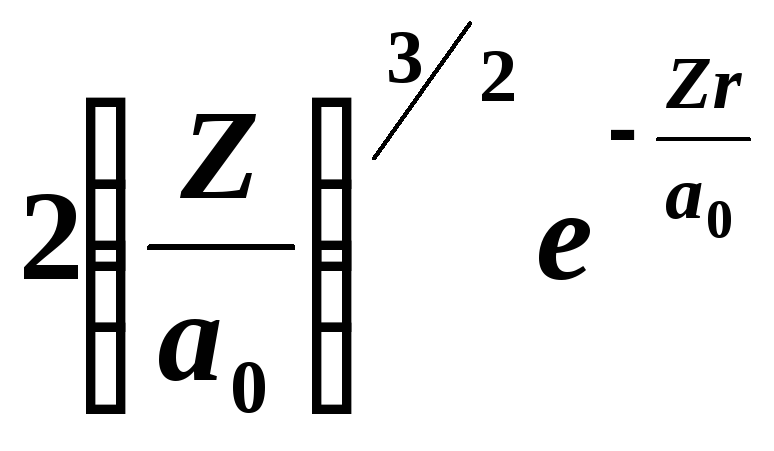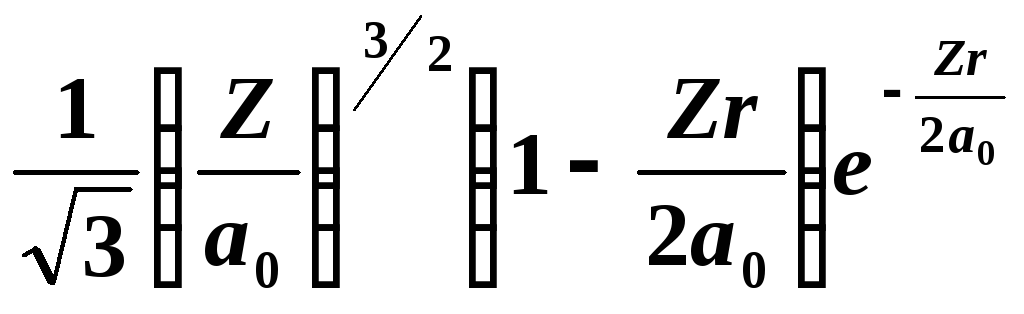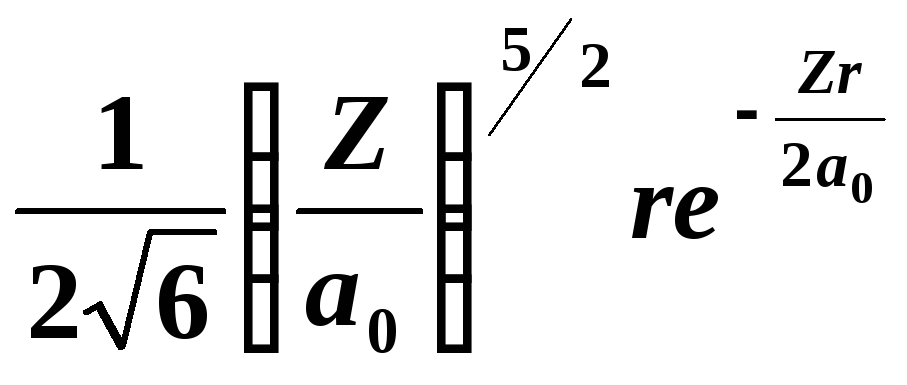Материал: SEMINAR1_
Семинар № 1
Атомные орбитали и их свойства.
При движении 1-го электрона в кулоновском поле ядра на него действует центральная сила F= -dV/dr.
Уравнение Шредингера для этой системы имеет вид:
H =Е ,
где гамильтониан
H = - (ђ2/2)2 – (e2/40)(1/r).
В сферической системе координат решение уравнения Шредингера ищут в виде
nlm (r,, ) = Rnl(r) Ylm(, ).
1)Угловые функции Ylm (, ) - собственные функции оператора квадрата угло-вого момента L2 - описывают в сферических координатах r,, угловую зависимость вероятности нахождения электронов в центральном поле атома. Они представляют собой сферические гармоники вида
Ylm
(,
) = (-1)(m+m)/2
{[(2l+1)/4](1-m)!
/ (1+m)!}1/2
![]() (cos)exp
(im)
(cos)exp
(im)
где
l=0,1,2,..-
орбитальное
квантовое число, характеризующее
угловой момент электрона, m=-l, ...+l –
магнитное квантовое число,
![]() (cos)
- присоединенные полиномы Лежандра.
(cos)
- присоединенные полиномы Лежандра.
Ylm (, ) - это комплексные ортонормированные функции:
![]() Ylm(,
)2
sin
dd
=1,
Ylm(,
)2
sin
dd
=1,
из которых легко построить действительные комбинации, оставляющие АО собственными функциями того же одноэлектронного уравнения:
ylm+ = (1/2)[(-1)mYlm+ Yl-m),
ylm- = -(i/2)[(-1)mYlm- Yl-m), l=0,1,2, .. , m=0, 1, 2 , .. , l.
Задание: Построить угловые части волновой функции атома, обладающего сферическим центральным полем .
(Результаты сведены в таблицу):
|
l |
m |
ylm |
Линейная Комбинация |
обозначение |
|
0 |
0 |
|
_ |
s |
|
1 |
0 |
|
_ |
pz |
|
1 |
- |
|
|
py |
|
1 |
+ |
|
|
px |
|
2 |
0 |
|
_ |
dz2 |
|
2 |
+ |
|
|
dxz |
|
2 |
- |
|
|
dyz |
|
2 |
+ |
|
|
dx2-y2 |
|
2 |
- |
|
|
dxy |
Действительные угловые функции имеют простую интерпретацию в декартовых координатах. Для них характерно наличие узлов и узловых плоскостей (объяснить!). Вероятность найти электрон в узле равна нулю.
Вид угловых частей АО :
При расчете одноэлектронных волновых функций многоэлектронного атома используются следующие приближения:
1) приближение независимых частиц,
2) приближение центрального поля,
3) метод самосогласованного поля.
Как следствие приближения центрального поля, угловая зависимость АО всех атомов одинакова.
2) Уравнение для радиальной части волновой функции имеет вид
(1/2r)2(rR)/ r2 + [e2/20r – l(l+1)ђ2/2r2 ] R = E R
Конкретный вид потенциала [……] возник после разделения переменных в сферических координатах: 1-й член – кулоновское притяжение, 2-й член – след-ствие наличия у электрона орбитального углового момента ( т.е. – следствие вращательного движения).
Потенциалы для l=0 и l0:
Точное значение нормированной радиальной функции Rnl для водородоподобного атома с зарядом ядра Z дается выражением:
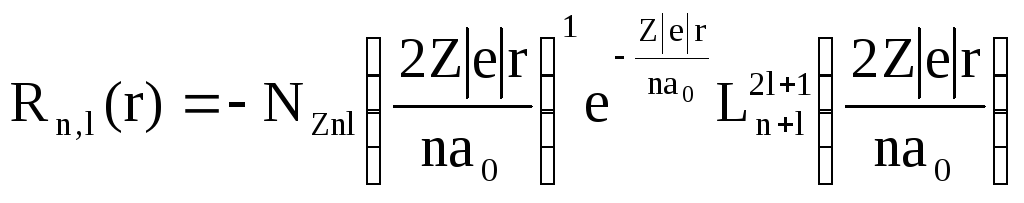 ,
,
где
![]() -
нормировочный множитель, зависящий от
Z, n и l ,
-
нормировочный множитель, зависящий от
Z, n и l ,
![]() - присоединенные полиномы Лягерра, l=
0,1,2,3,..., n
l+1.
- присоединенные полиномы Лягерра, l=
0,1,2,3,..., n
l+1.
Радиальные части, описывающие основное (n=1) и первое возбужденное (n = 2), состояния:
|
n |
l |
Rn,l ( r ) |
|
1 |
0
|
|
|
2
|
0
1 |
|
Классификация электронных состояний атома:
Главное квантовое число n характеризует энергию орбитали.
Орбитальное квантовое число l характеризует угловую зависимость орбитали (орбитальный угловой момент). Для каждого l приняты свои обозначения:
|
l |
0 |
1 |
2 |
3 |
4 |
5 |
|
Символ |
s |
p |
d |
f |
g |
h |
Зависимости радиальных частей Rnl от r для 1s , 2 s , 3s орбиталей атома водорода.
Cвойства радиальных функций.
-
Как следствие свойств полиномов Лягерра, радиальные функции с различными n и l ортогональны.
-
Имеются точки (поверхности), где функции Rn,l ( r ) обращаются в нуль; они называются узловыми точками (поверхностями) или просто узлами.
-
Радиальные функции с (n=1, l=0), (n=2, l=1), (n=3, l=2) и т.д. не имеют узловых точек; функции с (n=2, l=0), (n=3, l=1) и т.д. имеют одну узловую точку; функция с (n=3, l=0) – две узловые точки. Таким образом, число узлов радиальной функции равно (n-l-1).
4) Вероятность нахождения электрона в пространстве между значениями r и r+dr равна:
Pnl
(r) dr = Rn,l
( r ) 2
r 2dr
![]() Ylm(,
)2
sin
dd
Ylm(,
)2
sin
dd
Функция Pnl (r) , определяющая плотность вероятности нахождения электрона на расстоянии r от ядра, называется радиальной функцией распределения. Приравнивая нулю производную Pnl по r, можно найти наиболее вероятное положение электрона rвер на соответствующей орбитали.
Задание: Показать, что для основного состояния атома водорода rвер равно радиусу Бора a0=40ђ2/ e2m.
5) Вблизи ядра электрон-ядерный потенциал (e2/40)(1/r) становится неопределенным из-за стремления знаменателя к нулю. Чтобы волновая функция на ядре была непрерывна, необходимо, чтобы ее радиальная часть удовлетворяла асимптотическому условию
(R/r)r0 = -ZeRr0 .
6) На больших расстояниях от ядра атомная орбиталь зависит от r как
R ~ exp [ -(2I1)1/2 r],
где I1 - первый потенциал ионизации.
Д/з: 1)Вычислить положения максимумов 2s и 2p орбиталей .
2) Вычислить среднее положение электрона в атоме водорода по формуле
<r> = 1s r1s dr.
Использовать интеграл
xn exp(-ax) dx = n!/(an+1)
3) Показать, что условие (R/r)r0 = -ZeRr0 .справедливо лишь для функций с l = 0.