Материал: MU_SRS_AKhiFKhMA
3. Контрольная работа № 2
Приступая к выполнению заданий контрольной работы №2,студент должен проработать по рекомендуемой литературе следующие вопросы:
-сущность гравиметрического анализа, классификация методов в гравиметрии;
-требования, предъявляемые к реакциям, осадкам, выбору осадителя и его количеству;
-влияние различных факторов на растворимость осадков, явления соосаждения и окклюзии;
-образование кристаллических и аморфных осадков, их свойства;
-техника общих операций гравиметрического метода (растворение, осаждение, фильтрование, промывание, высушивание и прокаливание осадков);
-область применения и возможности титриметрических методов анализа, их классификации;
-стандартные вещества и предъявляемые к ним требования;
-рабочие и стандартные растворы, способы их приготовления и стандартизации, условия хранения;
-фактор эквивалентности и расчёт молярной массы эквивалента вещества;
-способы фиксирования точки стехиометричности;
-индикаторы, общая характеристика (интервал перехода, показатель титрования), предъявляемые к ним требования, механизм изменения окраски индикаторов;
-построение и анализ кривых титрования, выбор индикатора;
-расчёт результатов анализа.
3.1. Примеры расчётов в гравиметрическом методе
Для определения того или иного элемента (или соединения) в ходе гравиметрического анализа по методу осаждения взвешивают эквивалентное количество другого соединения - гравиметрическую (весовую) форму. Так, при определении бария в сульфате бария взвешивают не элементарный барий, а полученную при анализе гравиметрическую форму - BaSO4 ,а массу бария рассчитывают по формуле:
![]() ,
г (11)
,
г (11)
Вычисляют фактор пересчёта (гравиметрический фактор), т.е. отношение молярной массы определяемого компонента к молярной массе гравиметрической формы :
![]() (12)
(12)
Вместо формулы (11) можно записать :
m(Ba) = m(BaSO4) . F , г (13)
При анализе, имеющем практическое значение, в большинстве случаев рассчитывают массовую долю (%) определяемого компонента в анализируемом веществе :
![]() (14)
(14)
Р Е Ш Е Н И Е Т И П О В Ы Х З А Д А Ч
З а д а ч а 1. Вычислить навеску Ca3(PO4)2 ,если степень чистоты его 98 % и масса гравиметрической формы - CaO равна 0,6455 г.
Р е ш е н и е. 1) Рассчитывают гравиметрический фактор :
![]()
2) Находят массу чистого фосфата кальция, соответствующую 0,6455 г CaO:
m(Ca3(PO4)2) = m(CaO) . F = 0,6455 . 1,843 = 1,1897г.
Следует отметить, что точность гравиметрических методов определяется погрешностью взвешивания на аналитических весах (в зависимости от конструкции - (1 - 2).10-4 г), поэтому массу вещества (в граммах) записывают до четырёх цифр после запятой.
3) Рассчитывают навеску фосфата кальция по известной степени чистоты анализируемого вещества :
q(Ca3(PO4)2)
=
![]() = 1,2140 г.
= 1,2140 г.
О т в е т: навеска фосфата кальция равна 1,2140 г.
З а д а ч а 2. Рассчитать массовую долю алюминия в образце Al(NO3)3.9H2O, если навеска анализируемого образца равна 1,7000 г, а масса гравиметрической формы Al2O3 - 0,2865 г.
Р е ш е н и е. 1) Находят гравиметрический фактор :
![]()
2) Рассчитаем массовую долю алюминия по формуле (14) :
W
=
![]() = 8,92 %
= 8,92 %
О т в е т: массовая доля алюминия в образце составляет 8,92 %.
3.2. Примеры расчётов в титриметрическом методе
Расчёты результатов титриметрического анализа основаны на законе эквивалентов, согласно которому вещества реагируют между собой в эквивалентных количествах, которые рассчитываются по формуле :
![]() (15)
(15)
При решении задач рекомендуется придерживаться следующего плана:
1) выяснить метод анализа и составить соответствующую реакцию;
2) обратить внимание на достаточность данных в условии задачи (недостающие величины следует найти в справочной литературе);
3) обозначить количество каждого реагирующего вещества числом эквивалентов и составить расчётную формулу;
4) обратите внимание на размерность величин, они должны быть приведены к одной системе единиц;
5) ввести числовые значения в расчётную формулу и произвести вычисления.
РЕШЕНИЕ ТИПОВЫХ ЗАДАЧ
З а д а ч а 1. Рассчитать навеску тетрабората натрия, необходимую для приготовления 500 см3 раствора с молярной концентрацией эквивалента 0,1500 моль/дм3
Р е ш е н и е. 1) Вычисляют фактор эквивалентности и молярную массу эквивалента Na2B4O7.10H2O
Тетраборат натрия применяется в качестве стандартного вещества в методе кислотно-основного титрования : f(Na2B4O7).10H2O = 1/2.
М(1/2 Na2B4O7.10H2O) = 1/2M(Na2B4O7.10H2O) = 1/2.381,4 = 190,7 г/моль
2) Рассчитывают навеску тетрабората натрия по формуле (15) :
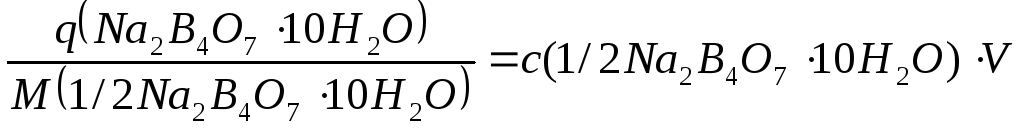
q =0,1500.0,5.190,7 = 14,3025 г.
О т в е т : для приготовления раствора требуется 14,3025 г тетрабората натрия.
З а д а ч а 2. Рассчитать навеску дихромата калия, необходимую для приготовления 250 см3 раствора с молярной концентрацией эквивалента 0,0500 моль/дм3.
Р е ш е н и е. 1) Вычисляют фактор эквивалентности и молярную массу эквивалента К2Cr2O7
Восстановление дихромата калия, являющегося стандартным веществом в методе йодометрии, протекает по реакции :
Cr2O72- + 14H+ + 6е = 2Cr3+ + 7H2O
Поскольку в полуреакции участвует 6 электронов, то f= 1/6 и
M(1/6 К2Cr2O7) = 1/6M(К2Cr2O7) = 1/6.294,18 = 49,03 г/моль.
2) Рассчитаем навеску К2Cr2O7 по формуле (15) :
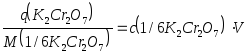
q = 0,0500.0,250.49,03 = 0,6129 г.
О т в е т : для приготовления раствора требуется 0,6129 г дихромата калия.
З а д а ч а 3. Вычислить объём раствора азотной кислоты плотностью р=1,180 г/см3, необходимый для приготовления 3 дм3 раствора с молярной концентрацией эквивалента приблизительно 0,20 моль/дм3.
Р е ш е н и е. 1) Рассчитывают массу безводной азотной кислоты, требующуюся для приготовления 3 дм3 раствора с молярной концентрацией эквивалента 0,20 моль/дм3.
F(HNO3) = 1 , M(1/1HNO3) = M(HNO3) = 63 г/моль.
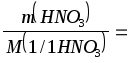 c(1/1HNO
).V(дм3)
c(1/1HNO
).V(дм3)
m(HNO3) = 0,20.3.63 = 37,8 г.
2) По плотности раствора HNO3 находят в справочнике массовую долю азотной кислоты. Раствор с массовой долей 30 % масс. имеет плотность 1,18 г/см3. Это значит, что в 100 г раствора содержится 30 г HNO3.
3) Рассчитывают, в каком количестве 30% масс. раствора содержится 37,8 г безводной азотной кислоты. Для этого составляют пропорцию :
В 100 г раствора содержится 30 г
В Х г 37,8 г
4) Рассчитывают объём раствора с массовой долей HNO3 - 30 % масс.
![]()
О т в е т : Необходимый объём раствора HNO3 равен 106,8 см3.
З а д а ч а 4. Сколько граммов H2SO4 содержится в 500 см3 раствора, если на титрование 25,00 см3 этого раствора расходуется 20,25 см3 раствора NaOH c молярной концентрацией эквивалента 0,1150 моль/дм3 ?
Р е ш е н и е. 1) Выясняют метод анализа и записывают реакцию. Эта задача относится к методу кислотно-основного титрования :
H2SO4 + 2NaOH = Na2SO4 + 2H2O
f(H2SO4) = 1/2, M(1/2 H2SO4) = 1/2M(H2SO4) = 49,04 г/моль.
2) Рассчитывают молярную концентрацию эквивалента H2SO4, применяя закон эквивалентов (количество моль эквивалента серной кислоты должно равняться количеству моль эквивалента гидроксида натрия) :
n(1/2 H2SO4) = n(1/1NaOH);
c(1/2 H2SO4) . V(H2SO4) = c(1/1NaOH) . V(NaOH)
откуда
с(1/2 H2SO4)
=
![]() = 0,09315 моль/дм3
= 0,09315 моль/дм3
-
Находят титр раствора серной кислоты :
![]()
4) Вычисляют массу H2SO4 в 500 см3 раствора :
m(H2SO4) = T(H2SO4) . V = 4,568.10-3 . 500 = 2,2840 г.
О т в е т : в 500 см3 раствора содежится 2,2840 г H2SO4.
З а д а ч а 5. Рассчитать массу перманганата калия в растворе, если после его замещения на I действием избытка KI и H2SO4 на титрование затрачено 24,50 см3 раствора тиосульфата натрия, титр которого равен 3,971.10-2 г/см3.
Р е ш е н и е. Выясняют метод анализа и составляют реакции. Эта задача относится к редоксиметрическому титрованию (йодометрия), которое проводят по методу замещения. При взаимодействии KMnO4 c раствором, содержащим избыток КI и H2SO4 ,происходит замещение KMnO4 эквивалентным количеством I :
 2
MnO4-
+ 8H+
+ 5е
= Mn2+
+ 4H2O
2
MnO4-
+ 8H+
+ 5е
= Mn2+
+ 4H2O
5 2I- - 2е = I2
2MnO4- + 10I- + 16H+ = 2Mn2+ + 5I2 + 8H2O
n(1/5KMnO4) = n(1/2I2)
Затем выделившийся йод оттитровывают раствором Na2S2O3 :
1 I2 + 2е = 2I-
