Материал: Khimia_42-45
42 Константа диссоциации. Закон разведения Оствальда.
Количественно электролитическую диссоциацию как равновесный обратимый процесс можно охарактеризовать константой диссоциации (ионизации), определяемой законом действующих масс. Если рассматривать электролитическую диссоциацию как равновесный обратимый процесс, диссоциацию электролита Kt„Anw (Kt+ - катион, Ап" - анион) можно представить в виде
![]()
Согласно закону действующих масс константу равновесия, называемую константой диссоциации, записывают следующим образом:

где [Kt" ] и [Апл ] - молярные равновесные концентрации ионов электролита; [Kt„Anm] - молярная равновесная концентрация недиссоциированных молекул электролита; Ка - константа диссоциации (моль/л).
Например, для диссоциации уксусной кислоты СН3СООН
![]()

константа диссоциации равна
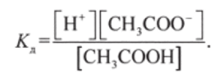
Уравнение (8.3) справедливо лишь для разбавленных растворов слабых электролитов. При использовании его для концентрированных растворов и растворов сильных электролитов уравнение (8.3) нужно видоизменить.
Чем больше константа диссоциации /Гд, тем сильнее диссоциирует электролит. В отличие от степени диссоциации Кя зависит только от природы растворителя, электролита и температуры, но практически не зависит от концентрации раствора (табл. 8.4). Таким образом, и константа Кау и степень электролитической диссоциации аи - количественные характеристики диссоциации. Естественно, что между ними существует связь.
Пусть имеется диссоциирующий на два иона слабый бинарный электролит KtAn, молярная концентрация которого с(Х), а степень диссоциации а„. В растворе этого электролита установится равновесие.
Применив закон действующих масс к ионному равновесию
![]()
получают выражение для Кл:
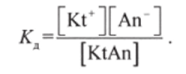
Подставив выражения для концентраций через степень диссоциации а„, получают:

Это соотношение называют законом разведения Оствальда (1888).
Уравнение (8.4) выражает зависимость степени диссоциации от концентрации раствора. Если электролит очень слабый, а„ « 1. Следовательно, величиной а„ в знаменателе можно пренебречь и уравнение (8.4) примет вид
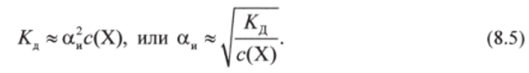
Соответственно закон Оствальда может быть сформулирован следующим образом.
Степень диссоциации слабого электролита возрастает с разбавлением раствора.
Сильные электролиты не подчиняются этому закону. Для них КД не является постоянной величиной и зависит от концентрации раствора (сильные электролиты не подчиняются закону действующих масс).
43 Сильные электролиты. Понятие активности и коэффициента активности. Ионная сила раствора.
В растворах сильных электролитов в результате их практически полной диссоциации создается высокая концентрация ионов.
Между катионами и анионами возникает электростатическое притяжение и эффективная, (то есть экспериментально определенная) концентрация этих ионов оказывается меньше, чем их истинная концентрация.
Для
оценки способности ионов к химическому
взаимодействию в растворах сильных
электролитов используют понятие -
активности ( ![]() ).
).
Активностью иона называют эффективную или условную концентрацию его, соответственно которой он действует в химических реакциях.
Между
активностью иона (
)
и его действительной концентрацией
( ![]() )
существует зависимость
)
существует зависимость
![]() ,
,
где ![]() -
коэффициент активности;
-
коэффициент активности; ![]() таким
образом, коэффициент
активности - это
отношение активности иона к его общей
концентрации. Так как
таким
образом, коэффициент
активности - это
отношение активности иона к его общей
концентрации. Так как ![]() ,
то
,
то ![]() ,
поэтому при точных расчетах в уравнение
закона действующих масс должны входить
активности ионов, а не их концентрации.
Если диссоциацию электролита изобразить
схемой
,
поэтому при точных расчетах в уравнение
закона действующих масс должны входить
активности ионов, а не их концентрации.
Если диссоциацию электролита изобразить
схемой
![]() ,-
,-
то
константа диссоциации ![]() будет
выражаться следующим образом:
будет
выражаться следующим образом:
![]()
В этом случае называют термодинамической константой.
Понятие
активности применимо не только к
отдельным ионам, но и к электролиту в
целом. Для электролита ![]() средняя
активность и средний коэффициент
активности связаны с активностями и
коэффициентами активности катионов
средняя
активность и средний коэффициент
активности связаны с активностями и
коэффициентами активности катионов ![]() и
анионов
и
анионов ![]() следующими
соотношениями:
следующими
соотношениями:
![]()
![]()
Коэффициенты
активности ионов зависят не только от
концентрации сильного электролита, но
и от концентрации всех других ионов,
присутствующих в растворе. Мерой
электростатического взаимодействия
между ионами является ионная
сила раствора- ![]() ,
которая вычисляется по формуле:
,
которая вычисляется по формуле:
![]()
где ![]() концентрации
различных ионов, моль/л;
концентрации
различных ионов, моль/л;
![]() заряды
этих ионов.
заряды
этих ионов.
44 Электролитическая диссоциация воды. Ионное произведение воды. Водородный показатель. Понятие об индикаторах.
Диссоциация воды.
Вода – слабый амфотерный электролит. И как слабый электролит в незначительной степени диссоциирует на ионы, которые находятся в равновесии с недиссоциированными молекулами:
H2O <-> H+ + OH-
KH2O = (H+)(OH-)/ (H2O)
Учитывая значение константы диссоциации воды и концентрацию недиссоциированных молекул воды в моль/л, получим выражение, называемое ионным произведением воды:
KH2O = (H+)(OH-)= 10-14
Постоянство произведения (H+)(OH-) означает, что в любом водном растворе ни концентрация ионов водорода, ни концентрация гидроксид-ионов не может быть равна нулю. Иными словами, любой водный раствор кислоты, основания или соли содержит как H+ , так и OH- -ионы. В чистой воде: (H+)= (OH-)= 10-7 моль/л. Если в неё добавить кислоту, то (H+)станет больше 10-7, а (OH-)меньше. И наоборот.
Из постоянства произведения (H+)(OH-) следует, что при увеличении концентрации одного из ионов воды соответственно уменьшает концентрация другого иона. Это позволяет вычислить концентрацию одного вида ионов, когда известна концентрация другого.
Концентрации ионов водорода, выраженные в моль/л, обычно составляют малые доли единицы. Использование таких чисел не всегда удобно. Поэтому введена особая единица измерения концентрации ионов водорода, называемая водородным показателем и обозначается рН.
Водородным показателем рН называется отрицательные десятичный логарифм концентрации ионов водорода: рН = -lg(H+)
Гидроксильный показатель рОН называется отрицательные десятичный логарифм ионов гидроксония: рОН = -lg(OH-)
рН + рОН = 14
рН = 7 – нейтральная среда;
рН < 7 – кислая среда;
рН > 7 – щелочная среда.
Одним из способов определения кислотности растворов является использование индикаторов (это сложные органические кислоты или основания):
Ио́нное произведе́ние воды́ — произведение концентраций ионов водорода Н+ и ионов гидроксида OH− в воде или в водных растворах, константа автопротолиза воды.
Вывод значения ионного произведения воды
Вода, хотя и является слабым электролитом, в небольшой степени диссоциирует:
H2O + H2O ↔ H3O+ + OH−
или
H2O ↔ H+ + OH−
Равновесие
этой реакции сильно смещено влево.
Константу диссоциации воды можно
вычислить по формуле: 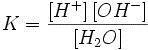 где:
где:
[H+] — концентрация ионов гидроксония (протонов);
[OH−] — концентрация гидроксид-ионов;
[H2O] — концентрация воды (в молекулярной форме) в воде;
Концентрация воды в воде, учитывая её малую степень диссоциации, величина практически постоянная и составляет (1000 г/л)/(18 г/моль) = 55,72 моль/л.
Константа Kв, равная произведению концентраций протонов и гидроксид-ионов, называется ионным произведением воды. Она является постоянной не только для чистой воды, но также и для разбавленных водных растворов веществ. C повышением температуры диссоциация воды увеличивается, следовательно, растёт и Kв, при понижении температуры — наоборот.
Практическое значение ионного произведения воды
Практическое значение ионного произведения воды велико, так как оно позволяет при известной кислотности (щёлочности) любого раствора (то есть при известной концентрации [H+] или [OH−]) найти соответственно концентрации [OH−] или [H+]. Хотя в большинстве случаев для удобства представления пользуются не абсолютными значениями концентраций, а взятыми с обратными знаком их десятичными логарифмами — соответственно, водородным показателем (pH) и гидроксильным показателем (pOH).
Так как Kв — константа, при добавлении к раствору кислоты (ионов H+), концентрация гидроксид-ионов OH− будет падать и наоборот. В нейтральной среде [H+] = [OH−] = моль/л. При концентрации [H+] > 10−7 моль/л (соответственно, концентрации [OH−] 10−7 моль/л (соответственно, концентрации [H+] < 10−7 моль/л) — щелочной. Чистая вода очень плохо проводит электрический ток, но всё же обладает измеримой электрической проводимостью, которая объясняется небольшой диссоциацией воды на ионы водорода и гидроксид-ионы. Для воды и разбавленных водных растворов при неизменной температуре произведение концентраций ионов водорода и гидросид-ионов есть величина постоянная. Эта постоянная величина называется ионным произведением воды. Растворы, в которых концентрация ионов водорода и гидроксид-ионов одинаковы, называются
нейтральными растворами.
Если концентрация ионов водорода в водном растворе известна, то тем самым определена и концентрация гидроксид-ионов. Поэтому как степень кислотности, так и степень щёлочности раствора можно количественно охарактеризовать концентрацией ионов водорода. Кислотность и щелочность раствора можно выразить другим, более удобным способом: вместо концентрации ионов водорода указывают её десятичный логарифм, взятый с обратным знаком.
Эта величина называется водородным показателем и обозначается через рН:
рН=-lg[H+]
Для измерения рН существуют различные методы. Приближённо реакцию
раствора можно определить с помощью специальных реактивов, называемых
индикаторами, окраска которых меняется в зависимости от концентрации ионов
водорода. Наиболее распространённый индикатор – метиловый оранжевый,
метиловый красный, фенолфтолеин.
ИНДИКАТОРЫ (от лат. indicator – указатель) – вещества, позволяющие следить за составом среды или за протеканием химической реакции. Одни из самых распространенных – кислотно-основные индикаторы, которые изменяют цвет в зависимости от кислотности раствора. Происходит это потому, что в кислой и щелочной среде молекулы индикатора имеют разное строение.
Кислотно-основные индикаторы — органические соединения, способные изменять цвет в растворе при изменении кислотности (рН). Индикаторы широко используют в титровании в аналитической химии и биохимии. Из-за субъективности определения цвета, индикаторы pH не всегда удобны, для точного измерения pH используют pH-метры с цифровой индикацией.
Измерение pH с помощью индикаторной бумаги
Ks: ![]()
Формы применения индикаторов
Индикаторы обычно используют, добавляя несколько капель водного или спиртового раствора, либо немного порошка (например, смесь мурексида с хлоридом натрия) к пробе исследуемого раствора. Так, при титровании, в аликвоту исследуемого раствора добавляют индикатор, и наблюдают за изменениями цвета в точке эквивалентности.
Другой способ применения - использование полосок бумаги, пропитанных раствором индикатора или смеси индикаторов и высушенных (например, "Универсальный индикатор"). Такие полоски выпускают в самых разнообразных вариантах - с нанесенной на них цветной шкалой - эталоном цвета (в том числе для окрашенных или мутных сред), или с напечатанными числовыми значениями рН; для точного измерения в узких диапазонах рН, и для ориентировочного исследования растворов; в рулончиках, коробках и пеналах, или в виде отрывных книжечек.
Современные индикаторные полоски могут быть изготовлены с красителем - индикатором, привитым к целлюлозе или иному полимеру. Это делает их устойчивыми к вымыванию, вплоть до многократного использования.