Материал: 4629
Механизм реакции рассмотрим на примере полимеризации стирола в присутствии амида натрия в жидком аммиаке:
|
NaNH2 ↔ Na+ + NH2− |
CH2=CH + (Na+ + NH2− ) → NH2−CH2−CH−Na+ |
|
│ |
│ |
C6H5 |
C6H5 |
стирол
Рост цепи происходит в результате присоединения молекулы мономера к образовавшемуся карбаниону:
NH2−CH2−CH−Na+ + CH2=CH → NH2−CH2−CH−CH2−CH −Na+ и т.д. |
|||
│ |
│ |
│ |
│ |
C6H5 |
C6H5 |
C6H5 |
C6H5 |
стирол |
|
|
|
Прекращение роста цепи может происходить за счет передачи ее на рас- |
|||
творитель: |
|
|
|
… −CH2−CH−Na+ |
+ NH3 |
→ … −CH2−CH2 + NaNH2 |
|
│ |
|
│ |
|
C6H5 |
|
C6H5 |
|
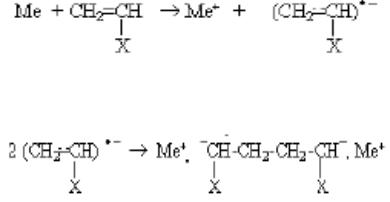
Если инициаторами являются щелочные металлы, то реакция начинается с образования ион-радикалов мономеров (ионно-координационная полимеризация):
Анионрадикалы рекомбинируют, образуя дианионы, рост цепи идёт в двух направлениях, на обоих концах инициатора:
Щелочные металлы впервые были применены в нашей стране для получения синтетического бутадиенового каучука академиком М.В.Лебедевым.
Анионной полимеризации характерно отсутствие реакций обрыва и передачи цепи, поэтому образуются «живые» полимеры. После завершения полимеризации (после полного исчерпания мономера) активные центры сохраняются, и при вводе новых порций мономера продолжается рост цепи.
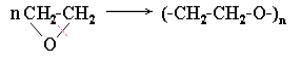
Полимеризация циклических мономеров
Данный вид полимеризации может протекать по ионному и ионнокоординационному механизмам. На практике используют полимеризацию ε-капролактама, окисей этилена и пропилена, пиридина, хинолина и др. Характерной особенностью такой полимеризации является то, что она протекает без возникновения новых типов химических связей и общее число химических связей не меняется.
этиленоксид полиэтиленоксид
n R − NH → … −NH – R – C− …
\ / |
││ |
C=O |
О |
лактам |
|
Лактамы – внутренние амиды аминокислот, содержащие в цикле группировку −С(О)−NR−, где R – H или органический радикал. В зависимости от числа атомов в цикле (3,4,5 и т.д.) различают α-лактамы, β-лактамы, γ-лактамы и т.д.
Практические способы проведения полимеризации
Применяют пять основных способов полимеризации: полимеризация в массе (блок-полимеризация), полимеризация в растворе, суспензии, эмульсии и в газообразной фазе.
При блочной полимеризации полимер сразу получают в виде изделий определенной формы – блоков. Представителем таких полимеров является полиметилметакрилат (органическое стекло), получаемый в виде прозрачных листов. При блок-полимеризации мономер с добавкой инициатора или катализатора заливают в формы и подвергают нагреву.
Полимеризацию в растворе применяют для получения продуктов с относительно короткими цепями, используемых при производстве лаков (лаковая полимеризация), клеев и др. В этом случае мономер предварительно переводят с помощью растворителя в раствор, а затем смешивают с инициатором.
При суспензионной и эмульсионной полимеризации мономер и инициатор диспергируются в воде до мельчайших капелек. Для обеспечения устойчи-
вости капелек в суспензии вводят защитные коллоиды (желатину и др.), а в эмульсии – поверхностно-активные вещества (эмульгаторы).
При газовой полимеризации мономер находится в газообразном состоянии. В зависимости от требований, предъявляемых к полимеру, дальнейшей
переработки и условий его практического применения, природы мономера и механизма процесса полимеризации выбирают определенный способ.
СОПОЛИМЕРИЗАЦИЯ
Сополимеризацией называется процесс совместной полимеризации двух или более мономеров. Получаемые при этом ВМС называются сополимерами.
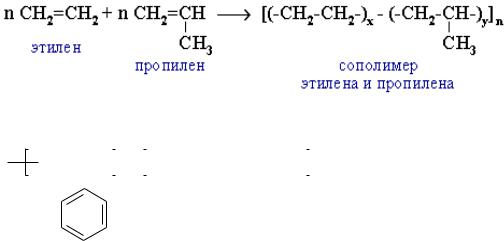
Пример 1. Сополимеризация этилена с пропиленом:
Пример 2. Сополимер стирола и бутадиена:
CH |
|
|
CH |
|
|
|
CH |
|
CH |
|
CH |
|
CH |
|
|
|
|
|
|
|
|
||||||||||
2 |
|
n |
|
2 |
|
2 |
m |
||||||||
|
|
|
|||||||||||||
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Различают регулярные и нерегулярные сополимеры, в которых структурные звенья расположены вдоль цепочки беспорядочно или упорядоченно.
Существуют следующие типы сополимеров:
чередующиеся (-A-B-)n
периодические (-A-B-A-)n
статистические (-A-A-B-A-A-A-B-B-A-B-)
блок-сополимеры (-A-)n-(-B-)m – состоят из нескольких
гомо-полимерных блоковпривитые (-A-A-A-A-A-A-A-A-A-A-)
\\
BB
\\
B B
Большое практическое значение реакции сополимеризации объясняется тем, что сополимеры часто обладают более ценными техническими свойствами, чем полимеры, образованные одним мономером. Кроме того, свойства сополимеров в значительной степени зависят от их состава, что определяет возможность их широкого изменения.
АБС-пластик – термопластичный тройной сополимер акрилонитрила, бутадиена и стирола (название пластика образовано из начальных букв наименований мономеров). Молекулярная масса АБС-пластика 120-180 тыс. Получают его радикальной полимеризацией.
nCH2=CH + nCH2=CH-CH=CH2 |
+ nCH2=CH → (-CH2-CH- CH2-CH=CH-CH2-CH2-CH-)n |
||
│ |
│ |
│ |
│ |
CN |
C6H5 |
CN |
C6H5 |
АБС-пластик – непрозрачный, обычно темноокрашенный материал, обладающий высокими влаго-, масло-, кислото- и щелочестойкостью, устойчивостью к действию органических растворителей. По механической прочности, ударной вязкости, теплостойкости и жесткости превосходит ударопрочный полистирол.
Наполнение АБС-пластика короткими стеклянными волокнами (15-30% по массе) или высокодисперсными веществами приводит к повышению его прочности. Широко применяют вспененный АБС-пластик.
АБС-пластик применяется для изготовления крупных деталей автомобилей (приборных щитков, элементов ручного управления), корпусов теле- и радиоаппаратуры, телефонов, деталей электроосветительных и электронных приборов, спортинвентаря, мебели, изделий сантехники. Его используют также как наполнитель, повышающий ударопрочность или улучшающий перерабатываемость композиций на основе поливинилхлорида, поликарбонатов, полистирола.
ВАЖНЕЙШИЕ ПОЛИМЕРИЗАЦИОННЫЕ ПОЛИМЕРЫ
Полимерные углеводороды
Полиэтилен (−СН2− СН2−)n получают:
радикальной полимеризацией этилена в присутствии инициаторов при высоком давлении (100…200МПа) и температуре 150…180оС, в среде ки-
слорода. Это полиэтилен высокого давления (ПВД) и низкой плотности. Мол. масса 3∙104…4∙105, наличие в цепи разветвлений;
ионной полимеризацией в присутствии катализатора (оксид хрома), Р=3…4 МПа и t=125…150оС, это полиэтилен среднего давления и средней плотности;
ионно-координационной полимеризацией (комплексные металлорганические катализаторы Циглера-Натта), Р=0,03…0,05 МПа и t ~80оС. Это полиэтилен низкого давления (ПНД) и высокой плотности, мол. мас-
са 5∙104 …106 .
Наибольшее распространение получили полиэтилены ПНД и ПВД.
Свойства: низкая плотность, высокие прочностные свойства, малая водопоглощаемость, высокая морозостойкость, хорошо поддается механической обработке, химически стоек, при нормальной температуре не растворим в органических растворителях. При высоких температурах быстро разрушается в растворах серной и азотной кислот. Стареет под действием солнечной радиации, горюч, непрозрачен.
Недостатки: низкий модуль упругости и твердость, малая теплостойкость, большой коэффициент теплового расширения.
Применение: для изготовления различных технических изделий, гидроизоляционных материалов, пленок, труб, для антикоррозийной защиты металлов, в фурнитуре мебели.
Полипропилен (−СН2−СН(СН3)−)n – получают катионной и анионной полимеризацией газообразного пропилена в присутствии катализаторов – хлоридов металлов и металл-органических соединений. P = 3 МПа, Т=60…90оС, в среде растворителей (гептан, изооктан и др.). Мол. масса ~ 35 000-150 000.
Получают пропилен различного пространственного строения:
…−CH2−CH−CH2−CH−CH2−CH−… |
изотактический, |
||
│ |
│ |
│ |
|
СН3 |
СН3 |
СН3 |
|
|
СН3 |
|
СН3 |
|
│ |
|
│ |
…−CH2−CH−CH2−CH−CH2−CH−CH2−CH−… синдиотактический, |
|||
│ |
|
│ |
|
СН3 |
|
СН3 |
|