Материал: 3 Лейкозы
Гемобластозы
Гемобластозы — опухоли, возникающие из кроветворных клеток гемопоэтической ткани.
Гемобластозы занимают первое место как причина смерти среди всех болезней системы крови.
Гемобластозы подразделяют на лейкозы (опухоли, диффузно — системно –поражающие гемопоэтические клетки костного мозга), лимфомы (внекостномозговые плотные, растущие в виде узла или нескольких узлов, опухоли из лимфопролиферативных кроветворных клеток) и миелопролиферативные новообразования (миеломы).
В клинической практике используют не родовое понятие «лейкоз», а названия конкретных нозологических форм лейкоза (разных его стадий и определённых иммуно-, фено- и генотипов), каждая из которых подразумевает конкретную программу лечения. Так, согласно МКБ–10, к злокачественным новообразованиям «лимфоидной, кроветворной и родственных им тканей» (коды МКБ — C81–C96) относятся болезнь Ходжкена (лимфогранулематоз), неходжкенские лимфомы (лимфосаркомы), злокачественные иммунопролиферативные болезни (в том числе макроглобулинемия Вальденстрёма), множественная миелома, лимфоидный лейкоз (лимфолейкоз), миелоидный лейкоз (миелолейкоз), истинная полицитемия и ряд других опухолей.
В клинической литературе лимфомы (растущих вне костного мозга очаговые опухоли из кроветворных клеток) обозначают как гематосаркомы (син.: лимфосаркомы). К гематосаркомам относят также миело-, эритро-, мегакариосаркомы, а также морфологически недифференцируемые гематосаркомы. При метастазировании гематосарком в костный мозг опухолевый процесс приобретает генерализованный характер. Этот феномен обозначают как лейкемизация гематосарком.
Общая характеристика лейкозов
Лейкоз — системное опухолевое поражение гемопоэтических клеток костномозговой ткани.
Для обозначения лейкозов не рекомендуется применять старый, предложенный еще Р. Вирховым, термин «лейкемия» (белокровие) в связи с тем, что к лейкозам относятся, помимо опухолей из лимфо- и миелопоэтических клеток, также и новообразования из клеток эритро- и мегакариоцитарных ростков.
Этиология
Причины
Причинами лейкозов являются те же группы факторов, которые вызывают опухоли (см. главу 17 «Опухоли»).
Факторы риска
• Наследственное предрасположение. Описаны доминантное и рецессивное наследование хронического лимфолейкоза (ХЛЛ), а также низкая заболеваемость этим лейкозом в одних этнических группах и высокая в других. Чаще в этих случаях наследуется не сам лейкоз, а нестабильность генома — сниженная резистентность хромосом к действию мутагенов, предрасполагающая родоначальные миелоидные или лимфоидные клетки к опухолевой (лейкозной) трансформации.
• Применение лекарственных средств с цитостатическим действием. Вероятность возникновения острых лейкозов у больных, лечившихся цитостатиками, повышается в сотни раз.
• Воздействие на организм проникающей радиации и/или рентгеновского излучения (в том числе- с лечебной целью). Минимальный интервал времени до возникновения лейкоза после облучения составляет 5–10 лет, а после химиотерапии — 2 года (максимум в течение 6–10 лет).
Патогенез
Трансформация нормальных гемопоэтических клеток в опухолевые является результатом изменений в генетической программе.
Основную роль при этом играют хромосомные нарушения. В большинстве случаев они определяют прогноз болезни и тип специфического лечения. Нестабильность генома лейкозных клеток приводит к появлению в первоначальном опухолевом клоне новых субклонов, среди которых в процессе жизнедеятельности организма, а также под воздействием лечения "отбираются" наиболее автономные (этот феномен получил название «опухолевая прогрессия»). Этим феноменом объясняют прогредиентность течения лейкозов, их «уход» из-под контроля цитостатиков и генерализация процесса.
Опухолевый атипизм
Атипизм гемобластозов — совокупность существенных качественных и количественных отличий биологических свойств гемобластозных клеток от нормальных и других патологически изменённых (но не трансформированных) клеток и тканей. В основе формирования атипизма гемобластозов лежит процесс опухолевой прогрессии.
Опухолевая прогрессия
Опухолевая прогрессия по своему существу является механизмом нарастания степени злокачественности клеток гемобластозов в результате изменений их генетической программы. Повышенная и постоянная изменчивость различных свойств гемобластозов, обусловливая их гетерогенность и автономность, создаёт условия для всё большей приспособленности их клеток к условиям среды, включая и возможность «ускользания» от цитостатической терапии.
Признаки опухолевой прогрессии гемобластозов
Проявления опухолевой прогрессии гемобластозов приведены на рис. 21–34.
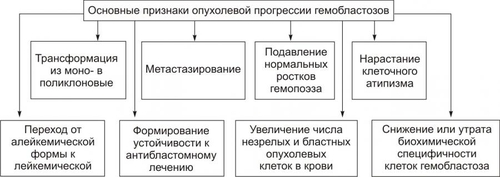
Рис. 21–34. Признаки опухолевой прогрессии гемобластозов.
Процесс опухолевой прогрессии ведет к формированию и/или нарастанию степени атипизма роста, обмена, структуры и функции лейкозов.
Атипизм роста
Проявления атипизма роста лейкозов представлены на рис. 21–35.
Лейкемическая:
число лейкоцитов превышает 30–50109/л.,
большое количество бластных форм
лейкозных клеток.
Сублейкемическая: Количество лейкоцитов выше нормы (но до 30–50
109/л), большое количество бластных клеток.Лейкопеническая: число лейкоцитов ниже нормы, сравнительно небольшое количество бластных лейкозных клеток.
Алейкемическая: количество лейкоцитов в диапазоне нормы, бластные клетки отсутствуют. Атипичные лейкоциты, их бластные и молодые формы находят лишь в ткани костного мозга.
Лейкемический «провал» (лейкемические «ворота» [hiatus leukaemicus], лейкемическое «зияние»). Выявляется при остром миелобластном лейкозе и характеризуется наличием в периферической крови бластных, молодых и зрелых форм лейкозных клеток и отсутствием одной или нескольких переходных форм гемопоэза. С этим и связано название признака — лейкемический «провал».
Анемия. Является спутником большинства лейкозов, в особенности острых.
Тромбоцитопения и снижение свёртываемости крови.
Геморрагический синдром. Характеризуется частыми кровотечениями, в том числе в полости тела и полые органы (желудок, кишечник, пищевод, мочевой пузырь и др.), а также кровоизлияниями.
Атипизм обмена
Атипизм обмена характеризуется отклонением от нормы биохимических характеристик клеток и/или продуктов их метаболизма. Помимо общих признаков опухолевого атипизма обмена углеводов, белков, липидов, ионов, минералов, КЩР (см. главу 17 «Опухолевый рост»), для лейкозов характерен ряд специфичных признаков.
• Прекращение синтеза лейкозными клетками отдельных ферментов (например, кислой фосфатазы, миелопероксидазы) и, как следствие — катализируемых или процессов.
• Пара‑ и диспротеинемии. Парапротеинемия наблюдается при миеломной болезни, макроглобулинемии Вальденстрёма, болезни тяжёлых цепей Франклина.
Атипизм структуры
Характеризуется развитием признаков клеточного (см. главу 17 «Опухолевый рост») и тканевого атипизма (проявляющегося наличием двух типов клеток в гемопоэтической ткани и периферической крови — нормальных и опухолевых). Подробнее характеристику атипизма структуры лейкозов см. в учебниках по патологической анатомии.
Атипизм функций
При лейкозах нарушаются функции как трансформированных (лейкозных), так и нормальных лейкоцитов. Это приводит к существенным нарушениям фагоцитарной активности, механизмов реализации клеточного и гуморального иммунитета. В совокупности указанные нарушения обусловливают развитие иммунодефицита и в том числе снижение противоинфекционной устойчивости и антибластомной резистентности организма.
Характеристика отдельных, наиболее часто встречающихся лейкозов.
Ниже рассмотрены острые и хронические формы лейкозов как пример современного подхода к патогенезу, типированию конкретных стадий, проявлениям и принципам лечения онкогематологических заболеваний.
Острый лейкоз
Клеточным субстратом острых лейкозов являются бластные опухолевые клетки. Острый лейкоз без лечения приводит к смертельному исходу в течение нескольких недель или месяцев. При правильном и своевременном лечении прогноз для детей часто благоприятен. Острые лейкозы подразделяют на миелоидные (острый миелолейкоз), лимфоидные (острый лимфолейкоз ), монобластные (миеломонобластные), эритромиелобластные и мегакариобластные.
Хронический лейкоз
Морфологический субстрат хронических лейкозов — относительно дифференцированные клетки кроветворной ткани. Больные могут жить без лечения в течение нескольких месяцев и лет. Хронические лейкозы нередко трансформируются в острые формы. Хронические лейкозы подразделяют на миелоидные (хронический миелолейкоз — ХМЛ), лимфоидные (хронический лимфолейкоз — ХЛЛ и волосатоклеточный лейкоз), моноцитарные (миеломоноцитарные), эритроцитарные (истинная полицитемия) и мегакариоцитарные.
Острые лейкозы
Острые лейкозы — злокачественные заболевания кроветворной системы, морфологический субстрат — бластные клетки. Наиболее часто диагносируются острый лимфобластный лейкоз (ОЛЛ) и острый миелоидный лейкоз.
Частота
Частота острых лейкозов 13,2:100 000 среди мужчин и 7,7:100 000 среди женщин. ОЛЛ чаще развивается в детском возрасте и после 40 лет. Частота острого миелоидного лейкоза одинакова во всех возрастных группах.
Патогенез
Патогенез острого лейкоза обусловлен пролиферацией клона опухолевых клеток с характерными цитогенетическими нарушениями, угнетением нормального кроветворения, выходом бластных клеток в кровь, метастазированием их в другие кроветворные (селезёнка, печень, лимфоузлы) и некроветворные (кожа, ЦНС, яички, лёгкие) органы.
Виды острого лейкоза
Существенный момент диагностики и последующей терапии любого лейкоза — типирование заболевания у конкретного больного. Критерии типирования лейкозов представлены на рис. 21–36.
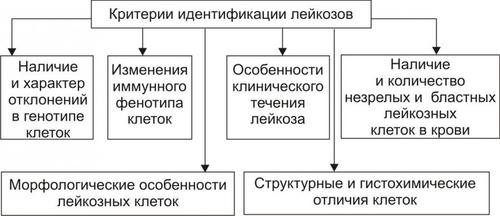
Рис. 21–36. Критерии типирования лейкозов.
Проявления
Начало заболевания, как правило, внезапное.
Тяжёлое состояние больного может быть обусловлено выраженной интоксикацией, геморрагическим синдромом (результат тромбоцитопении), дыхательной недостаточностью (вследствие сдавления дыхательных путей увеличенными внутригрудными лимфатическими узлами).
Возможно и постепенное развитие заболевания.
• Анемический (гипоксический) синдром: бледность, одышка, сердцебиение, сонливость.
• Снижение резистентности к инфекциям (бактериальным, грибковым и вирусным). У пациентов с лейкозами выявляют как лёгкие (локальные) формы инфекций (например, кандидозные стоматиты, гингивиты, поражения слизистых оболочек, вызванные вирусом простого герпеса), так и тяжёлые генерализованные процессы (пневмонии, сепсис).
• Геморрагический синдром. При осмотре пациентов обнаруживают петехии и экхимозы на коже (самопроизвольные, в местах инъекций или механического трения). Возможны тяжёлые носовые и внутренние кровотечения (метроррагии, желудочно-кишечные кровотечения, кровоизлияния в мозг).
• ДВС-синдром.
• Интоксикация.
Проявляется лихорадкой, снижением массы
тела и аппетита, слабостью, повышенной
потливостью.
• Болезненность костей. В наибольшей мере выражена в трубчатых костях и позвоночнике, в области суставов (артралгии). Обусловлена опухолевой гиперплазией костномозговой гемопоэтической ткани.
• Лимфаденопатия. Возможно увеличение любой группы лимфатических узлов в связи с пролиферацией в них лейкозных лимфоидных клеток.
• Печень и селезёнка увеличены. Увеличение их размеров связано с метастазированием лейкозных клеток в эти органы и образованием экстрамедуллярных очагов гемопоэза в них.
• Нейролейкемия. Поражение ЦНС (нейролейкемия) возникает особенно часто при ОЛЛ и значительно ухудшает прогноз. Возникновение нейролейкемии обусловлено метастазированием лейкозных клеток в оболочки головного и спинного мозга или в вещество мозга.
• Гипертрофия тимуса обусловлена метастазами лейкоза в вилочковую железу. Может вызвать сдавление органов средостения.
Лабораторная и инструментальная диагностика
Анализ крови
Подозрение
на лейкоз должно возникать при наличии
клинических симптомов и изменений в
периферической крови: нормохромная
нормоцитарная анемия; количество
лейкоцитов может быть различным —
низким (менее 5109/л),
нормальным (от 5109/л
до 10109/л),
повышенным (свыше 20109/л,
достигая в некоторых случаях 200109/л);
нейтропения (не зависит от общего
количества лейкоцитов); абсолютный
лимфоцитоз; тромбоцитопения (присутствует
почти всегда); лейкемический «провал»
— присутствие бластов, зрелых форм на
фоне отсутствия промежуточных форм;
при остром миелобластном лейкозе можно
обнаружить азурофильные гранулы и
палочки Ауэра.
Пункция костного мозга
Пункция костного мозга — основной метод исследования при лейкозах. Его применяют с целью подтверждения диагноза и идентификации (морфологической, иммунофенотипической, цитогенетической) типа лейкоза.
Миелограмма (количественная характеристика всех клеточных форм костного мозга) при острых лейкозах характеризуется увеличением содержания бластных клеток более 5% и до тотального бластоза. Структура бластов при этом различна в зависимости от типа лейкоза. Выявляется увеличение переходных форм клеток, лимфоцитоз. Красный росток кроветворения угнетён (за исключением острого эритромиелоза). Мегакариоциты отсутствуют или количество их незначительно (за исключением острого мегакариобластного лейкоза).
Цитохимическое исследование — основной метод диагностики форм острых лейкозов. Его проводят с целью выявления специфических для различных бластов ферментов. Так, при ОЛЛ определяется положительная ШИК-реакция на гликоген, отрицательная реакция на липиды, пероксидазу, хлорацетат эстеразу. При острых миелобластных лейкозах — положительная реакция на миелопероксидазу, липиды, хлорацетат эстеразу.
Иммунофенотипирование бластов позволяет определить с помощью моноклональных АТ наличие или отсутствие кластеров дифференцировки бластных клеток (CD-маркёры). Его проведение в первую очередь необходимо для точной диагностики ОЛЛ (см. табл. 21–7 и рис. 21–36), а также в случаях невозможности дифференциальной диагностики острых морфологически недифференцируемых лимфобластных и миелобластных лейкозов.
Цитогенетическое исследование лейкозных клеток позволяет определить хромосомные аномалии, уточнить диагноз и прогноз.
Лечение острых лейкозов
• Специфическая химиотерапия. Направлена на достижение и закрепление ремиссии заболевания. Состоит из нескольких этапов. Различна для лимфобластного и миелобластного лейкозов и проводится по стандартным схемам (в зависимости от результатов типирования заболевания).
• Сопутствующая (сопроводительная) терапия. Её проводят для борьбы с инфекциями, обусловленными агранулоцитозом, для снижения интоксикации при лизисе опухолевых лейкоцитов, для уменьшения побочных токсических эффектов химиотерапевтических препаратов.
• Заместительная терапия. Необходима при угрожающей тромбоцитопении, тяжёлой анемии, нарушениях свертывания крови.
• Трансплантация стволовых кроветворных клеток или костного мозга.
Общие принципы сопутствующего лечения
Профилактика инфекций — главное условие выживания пациентов с нейтропенией, возникшей вследствие химиотерапии.
• Необходима
полная изоляция пациента при количестве
лейкоцитов менее 1109/л,
строгий санитарно-дезинфекционный
режим.
• При повышении температуры тела проводят клиническое и бактериологическое исследования и немедленно начинают лечение комбинациями антибиотиков широкого спектра действия: цефалоспоринами, аминогликозидами, полусинтетическими пенициллинами, меропенемом (меронем), имипенемом+циластатином (тиенам). При вторичных подъёмах температуры тела, возникших после лечения антибиотиками, обычно эмпирически назначают противогрибковые средства (флуконазол, амфотерицин В). При пневмоцистных пневмониях применяют ко-тримоксазол (бисептол) в дозе 240 мг/кг в/в, при цитомегаловирусных инфекциях — ганцикловир.
• Для профилактики и лечения нейтропении можно назначить препараты гранулоцитарного [филграстим (нейпоген)] и гранулоцитарно-макрофагального [ленограстим (граноцит)] колониестимулирующих факторов. При острых миелобластных лейкозах эти препараты противопоказаны.
Методы заместительной терапии
• Трансфузия эритроцитарной массы. Показания: содержание Hb менее 70 г/л при клинических проявлениях анемии (одышка, сердцебиение в покое).
• Трансфузия
тромбоцитарной массы или тромбоконцентрата.
Показания: кровоточивость на фоне
содержания тромбоцитов менее 20109/л.
• Трансфузии компонентов крови совершаются всегда по жизненным показаниям.
• Трансплантация стволовых клеток крови или костного мозга.
ПРОГНОЗ
Острый лимфобластный лейкоз
У детей в 95% и более случаев наступает полная ремиссия. У 70–80% больных детей болезнь не проявляется в течение 5 лет, их считают здоровыми. При возникновении рецидива в большинстве случаев можно достичь второй полной ремиссии. Больные со второй ремиссией — кандидаты на трансплантацию костного мозга с вероятностью долговременного выживания 35–65%. Взрослые редко болеют ОЛЛ. Длительной ремиссии (более 5 лет) удаётся достичь в 15–25% случаев.
Острый миелобластный лейкоз
Полной ремиссии при большинстве вариантов острого миелобластного лейкоза удаётся добиться у 60–70% больных. При различных постиндукционных схемах средняя длительность ремиссии — 12–15 мес; у 25–35% больных нет рецидивов в течение 24 мес, часть из них достигает стойкой ремиссии («излечивается»).
Прогностически неблагоприятные признаки
Мужской
пол и возраст более 50 лет. Мегакариобластный
и эритробластный тип острого миелоидного
лейкоза. Ph-позитивный острый лимфолейкоз.
В дебюте заболевания — гиперлейкоцитоз
свыше 50109/л,
тромбоцитопения менее 50109/л,
нейролейкемия. Предшествующее неадекватное
лечение («предлеченность»).
Возможные исходы острых лейкозов
• Смерть больного. Причины смерти при острых лейкозах — нейролейкемия, геморрагический синдром (ДВС), почечная недостаточность (при синдроме лизиса опухолевых клеток), сердечная недостаточность, инфекционные осложнения (сепсис), острая надпочечниковая недостаточность (вследствие гипотрофии коры надпочечников при отмене длительно применяемых глюкокортикоидов).
• Ремиссия заболевания в течение 5 лет от завершения курса терапии. • Выздоровление. О полном выздоровлении говорят при отсутствии рецидива в течение 5 лет после завершения полного курса терапии.
• Рецидив заболевания. Может быть ранним и поздним: ранний — во время лечения; поздний — после проведённого лечения.