Материал: 116
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ВОРОНЕЖСКАЯ ГОСУДАРСТВЕННАЯ ЛЕСОТЕХНИЧЕСКАЯ АКАДЕМИЯ
Х И М И Я
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
к лабораторной работе по теме:
«АДСОРБЦИЯ. АДСОРБЦИОННОЕ РАВНОВЕСИЕ»
для студентов 1 курса всех специальностей
(с элементами УИРС)
ВОРОНЕЖ 2003
2
УДК 541.183
Бельчинская Л.И., Стрельникова О.Ю. Химия. Методические указания к лабораторной работе по теме: « Адсорбция. Адсорбционное равновесие», для студентов 1 курса всех специальностей (с элементами УИРС) – Воронеж: Воронеж. гос. лесотехн. акад., 2003. – 10 с.
Печатается по решению редакционно-издательского совета ВГЛТА
Работа предназначена для студентов 1 курса всех факультетов ВГЛТА при изучении темы: «Равновесия в гетерогенных системах»
Рецензент: д-р техн. наук, проф. В.М. Перелыгин
Научный редактор: канд. техн. наук, доц. А.И. Дмитренков
3
Теоретическая часть
Сорбция – процесс поглощения одного вещества (сорбата) другим (сор-
бентом). Если вещество поглощается всем объемом другого вещества, то происходит абсорбция, если только поверхностью – адсорбция.
Вещество, на поверхности которого происходит адсорбция, называется адсорбентом. В качестве адсорбентов используют непористые материалы,
пористые тела с развитой внутренней поверхностью – активные угли, силикагели, цеолиты и др.
Вещество, которое концентрируется на поверхности адсорбента, называется адсорбатом.
Таким образом, адсорбцией называется изменение концентрации адсорбата в поверхностном слое по сравнению с объемной фазой, отнесенное к единице поверхности адсорбента (г/м2, моль/м2). Часто из-за сложности определения величины поверхности адсорбентов количество адсорбированного вещества относят к единице массы (г/г, моль/г).
Адсорбция – самопроизвольный процесс, сопровождающийся убылью свободной энергии Гиббса G < 0. Энтальпия адсорбции также имеет отрицательное значение Н < 0, так как адсорбция - это экзотермический процесс.
Чем больше энергия взаимодействия адсорбата с поверхностью адсорбента, тем больше времени молекулы адсорбируемого вещества удерживаются на поверхности раздела фаз, то есть находятся в адсорбированном состоянии. Время адсорбции (τ) молекул на поверхности адсорбента определя-
ется уравнением: |
|
τ = τ0 е - Н/R T, |
(1) |
где τ0 – постоянная, зависящая от природы адсорбента и адсорбата; Н – энтальпия (тепловой эффект адсорбции);
R – универсальная газовая постоянная; Т – температура.
При адсорбции смеси веществ у границы раздела фаз будет накапливаться тот компонент, молекулы которого имеют большее время адсорбции.
Различают два вида адсорбции: физическую и химическую (хемосорбцию).
При физической адсорбции между частицами адсорбента и адсорбата возникают относительно непрочные межмолекулярные взаимодействия (силы Ван-дер-Ваальса). Физическая адсорбция характеризуется невысоким тепловым эффектом и малыми временами адсорбции. Примером физической адсорбции является адсорбция газов или растворенных веществ активированным углем.
4
При хемосорбции между частицами адсорбента и адсорбата возникают химические взаимодействия. Тепловой эффект хемосорбции близок к тепловому эффекту химических реакций. Примером химической адсорбции является адсорбция кислорода металлами.
Процесс адсорбции может быть обратимым. Явление, обратное адсорб-
ции, называется десорбцией.
Таким образом, десорбцией называется процесс удаления поглощенного вещества (адсорбата) с поверхности адсорбента.
Если в системе адсорбат – адсорбент при заданных условиях скорость
адсорбции равна скорости десорбции, то состояние системы называется адсорбционным равновесием.
Зависимость количества адсорбированного вещества (а) от его равновесной концентрации (С), т.е. концентрации адсорбата при адсорбционном
равновесии (или равновесного парциального давления (Р)) при постоянной температуре называется изотермой адсорбции. Изотермы адсорбции из вод-
ных растворов и газовых сред описаны уравнениями Лэнгмюра и Фрейндлиха. Уравнение Лэнгмюра выведено на основании допущения об адсорбции
монослоя на однородной поверхности адсорбента. Уравнение адсорбции Лэнгмюра имеет вид:
|
k C |
|
|
а = аmax |
|
, |
(2) |
|
|||
|
1+ k C |
|
|
где а – количество адсорбированного вещества (адсорбция), мг/г;
аmax – предельное количество вещества, которое может адсорбироваться, мг/г; С – равновесная концентрация вещества;
k – константа адсорбционного равновесия.
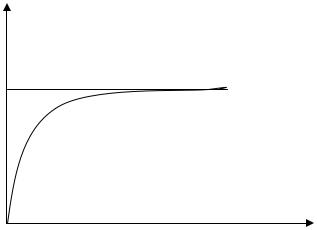
Графически изотерма адсорбции имеет вид, приведенный на рис.1.
а
аmax
23
1
0 |
С |
Рис.1. Изотерма адсорбции Лэнгмюра |
|
5
На изотерме Лэнгмюра можно выделить три участка:
1)при малых концентрациях адсорбата наблюдается линейная зависимость количества адсорбированного вещества от равновесной концентрации (участок 0-1);
2)в широком интервале средних концентраций количество адсорбированного вещества возрастает пропорционально С1/n (участок 1-2). Для этого участка справедливо уравнение изотермы адсорбции Фрейндлиха
а = k С1/n, |
(3) |
где k и n – константы.
Уравнение Фрейндлиха используется для описания адсорбции на неоднородных поверхностях.
3)при больших концентрациях адсорбированное количество адсорбата остается постоянным и не зависит от концентрации, достигается предел адсорбции аmax (участок 2-3);
Такой вид изотермы адсорбции может быть объяснен со следующих позиций. В результате введения малого количества адсорбата только небольшая часть поверхности адсорбента окажется занятой в данный момент, поэтому адсорбция следующих вводимых порций практически не будет зависеть от адсорбции предыдущего количества. Адсорбция будет пропорциональна равновесной концентрации. С дальнейшим увеличением концентрации адсорбата все большая часть поверхности адсорбента окажется занятой и вероятность попадания молекул адсорбируемого вещества на незаполненную поверхность уменьшается. Это приводит к росту адсорбции пропорционально некоторой дробной степени концентрации. При больших концентрациях адсорбата вся поверхность адсорбента занята. Абсорбция постоянна.
Величина адсорбции зависит от следующих факторов:
•природы адсорбента и адсорбата;
•температуры;
•концентрации (давления) адсорбата.
Адсорбция растет с увеличением концентрации или давления адсорбирующихся веществ согласно изотермам адсорбции (уравнения 2,3). С ростом температуры адсорбция уменьшается (уравнение 1). При увеличении температуры адсорбционное равновесие смещается в сторону десорбции. Т.е. десорбцию можно осуществить путем повышения температуры, снижения давления, а также вытеснения адсорбата другими веществами (десорбентами).