Материал: 11-15
Вопрос 14 Ферменты, определение. Особенности ферментативного катализа. Специфичность действия ферментов, виды. Классификация и номенклатура ферментов, примеры.
Ферменты, или энзимы – класс веществ белковой природы, используемый
живыми организмами для осуществления с высокой скоростью взаимосвязанных химических реакций.
Особенности ферментативного катализа:
Скорость ферментативных реакций выше
Обладают высокой специфичностью к субстрату
По своей химической природе белки
Подвержены регуляции (есть активаторы и ингибиторы ферментов)
Обладают конформационной лабильностью – способностью к небольшим изменениям своей структуры за счет разрыва и образования новых слабых связей.
Реакции протекают только в физиологических условиях (определенные значения температуры, давления и рН)
Специфичность – важное свойство ферментов, определяющее биологическую
значимость этих молекул. Различают субстратную и каталитическую специфичности фермента, определяемые строением активного центра:
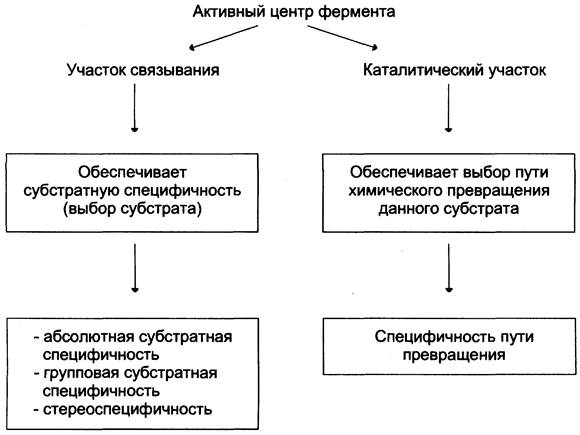
1. Абсолютная субстратная специфичность – активный центр ферментов,
обладающих абсолютной субстратной специфичностью, комплементарен только одному субстрату (уреаза, катализирующая гидролиз мочевины до диоксида углерода и аммиака).
2. Групповая субстратная специфичность – фермент катализирует однотипные
реакции с небольшим количеством (группой) структурно похожих субстратов
(панкреатич. липаза катализирует гидролиз любой молекулы жира (триацилглицерола) до молекулы моноацилглицерола и двух молекул высших жирных кислот)
3. Стереоспецифичность – при наличии у субстрата нескольких стереоизомеров
фермент проявляет абсолютную специфичность к одному из них (большинство моносахаридов и продуктов их обмена в организме человека и других млекопитающих относят к D-стереоизомерам. Ферменты, осуществляющие их метаболизм, имеют специфичность к D-, а не к L-сахарам).
4. Каталитическая специфичность (специфичность пути превращения
субстрата) - фермент катализирует превращение присоединённого субстрата по одному из возможных путей его превращения, который обеспечивается строением каталитического участка активного центра фермента
Например: молекула глюкозо-6-фосфата в клетках печени человека – субстрат 4
различных ферментов: фосфоглюкомутазы, глюкозо-6-фосфатфосфатазы, фосфоглюкоизомеразы и глюкозо-6-фосфатдегидрогеназы. Из-за особенностей строения каталитических участков этих ферментов происходит различное превращение этого соединения с образованием 4 различных продуктов: глюкоза, глюкозо-1-фосфат, 6-фосфоглюконолактон, фруктозо-6-фосфат).
Номенклатура ферментов:
1. Рабочее название: в названии большинства ферментов содержится суффикс
«аза», присоединённый к названию субстрата реакции (уреаза, сахараза, липаза, нуклеаза) или к названию хим. превращения определённого субстрата (лактатдегидрогеназа, аденилатциклаза, фосфоглюкомутаза, пируваткарбоксилаза).
Сохранился ряд тривиальных названий: трипсин, пепсин, ренин, тромбин.
2. Систематическое название: в соответствии с классификацией каждый фермент
получил систематическое название, однозначно характеризующее катализируемую им химическую реакцию.
Например: D-глицеральдегид-3-фосфат: NAD–оксидоредуктаза
(рабочее название – глицеральдегидфосфатдегидрогеназа).
Из названия следует, что субстратом фермента служит D-глицеральдегид-3-фосфат, тип катализируемой реакции: О-В в присутствии кофермента NAD+.
3. Кодовое название: четырёхзначное цифровое обозначение, где первая цифра
обозначает класс фермента, вторая цифра (подкласс) уточняет преобразуемую группировку, третья (подподкласс) –уточняет дополнительных участников реакции (например, донора и акцептора) и четвёртая – порядковый номер фермента в данной подгруппе. (Малатдегидрогеназа имеет кодовый шифр 1.1.1.38)
Классы ферментов:
Каждый из 6 классов имеет свой порядковый номер, строго закреплённый за ним.
1. Оксидоредуктазы - катализируют различные овр с участием 2 субстратов
(перенос е- или атомов водорода с одного субстрата на другой).
Систематическое наименование «донор: акцептор–оксидоредуктаза»,
Рабочее: субстрат – подкласс оксидоредуктаз.
Дегидрогеназы. В этот подкласс входят ферменты, катализирующие реакции
дегидрирования (отщепления водорода).
В качестве акцепторов электронов используются коферменты NAD+, NADP+, FAD, FMN.
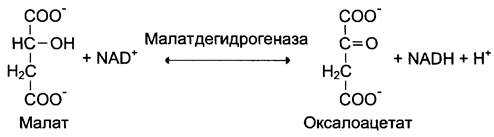
Оксидазы. Акцептором электрона служит молекулярный кислород. Пример:
![]()
Оксигеназы (гидроксилазы) – атом кислорода из молекулы кислорода присоединяется к субстрату
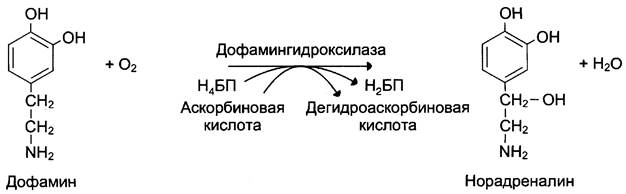
2. Трансферазы – катализируют перенос функц. Гр. От одного соед-я к другому.
Подразделяют в зависимости от переносимой группы.Название «донор: акцептор-транспортируемая группа-трансфераза».
Например: аминотрансферазы, ацилтрансферазы, метилтрансферазы,
гликозилтрансферазы, киназы (фосфотрансферазы).
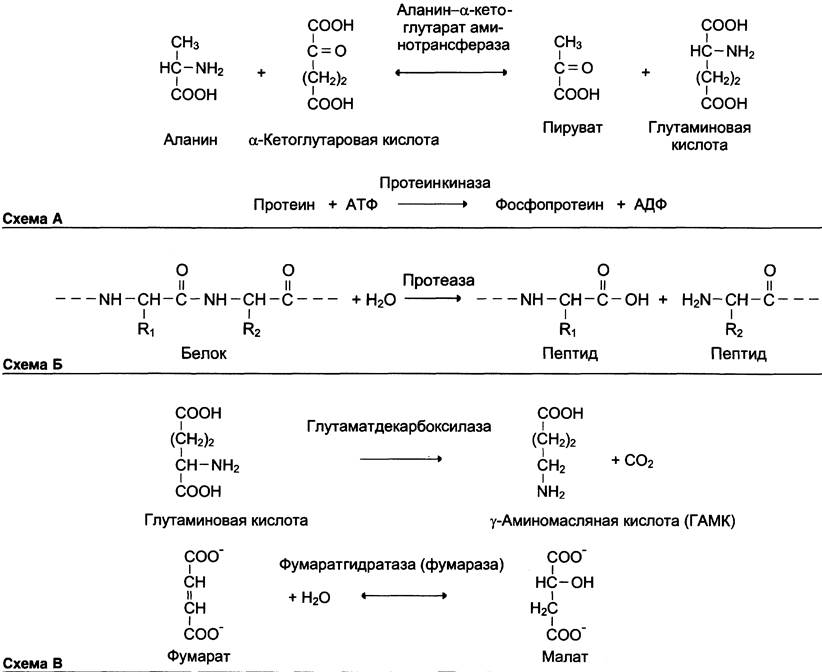
3. Гидролазы – катализируют реакции гидролиза (расщепления ковалентной
связи с присоединением молекулы воды по месту разрыва). Подразделяют в зависимости от расщепляемой связи.
Наименование «субстрат—гидролаза» или прямым присоединением к названию субстрата суффикса «аза», например, протеаза, липаза, фосфолипаза, рибонуклеаза. Пример реакции
Для отдельных классов гидролаз применимы специальные термины, характеризующие гидролиз определённой химической связи: эстеразы, фосфатазы и др.
4. Лиазы - ферменты, отщепляющие от субстратов негидролитическим путём
определённую группу (при этом могут отщепляться СО2, Н2О, NН2, SН2 и др.) или присоединяющие чаще всего молекулу воды по двойной связи.
Наименование «субстрат-отщепляемая или присоединяемая группировка».
5. Изомеразы - катализируют различные внутримолекуляр. Превращения.
Подразделяют в зависимости от типа реакции изомеризации.
Как общее название ферментов этого класса применяют термин «изомеразы», например,
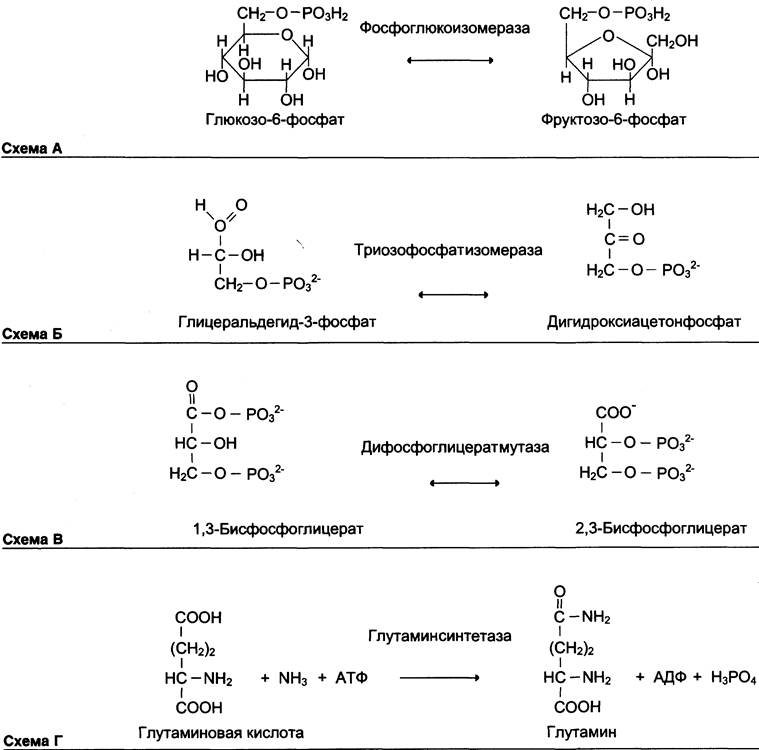
Изомеразы могут катализировать внутримолекулярные ОВР, осуществляя
взаимопревращения альдоз и кетоз, кетонных и енольных групп, перемещения двойных связей внутри молекулы
Когда изомеризация состоит во внутримолекулярном переносе группы, фермент
называют «мутазой»
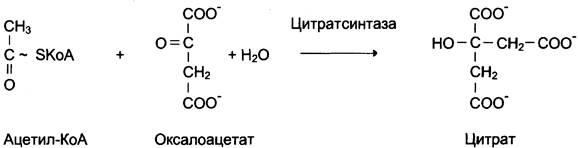
6. Лигазы (синтетазы) – катализируют реакции присоединения друг к другу
двух молекул с образованием ковалентной связи. Этот процесс сопряжён с разрывом фосфоэфирной связи в молекуле АТФ (или других нуклеозидтрифосфатов) или с разрывом макроэргических связей других соединений.
При использовании энергии гидролиза АТФ – называют лигазами, или синтетазами
Если источником энергии служит любое другое макроэрг. соединение (не АТФ) – называют синтазами
Вопрос 15
Строение ферментов. Каталитический и регуляторный центры. Взаимодействие ферментов с лигандами. Механизм действия ферментов. Формирование ферментсубстратного комплекса. Гипотеза «ключ-замок» и гипотеза индуцированного соответствия
По химическому строению различают:
Простые ферменты (состоят только из АК)
Сложные ферменты (имеют небелковую часть или простетическую группу).
Апофермент – белковая часть.
Кофермент – небелковая часть, м.б. связана ковалентно с апоферментом (тогда называют простетической группой – это FАD, FMN, биотин), но м.б. и нековалентно связана (NAD+)
Кофактор – небелковая часть (ионы Zn, Cu, K)
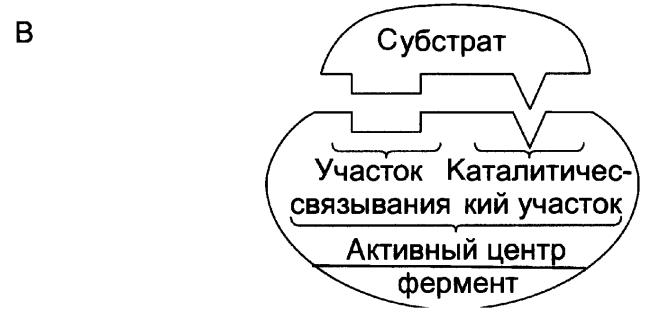
АЦ фермента – центр соединения фермента с субстратом в процессе катализа.
В АЦ различают две зоны:
Центр связывания, ответственный за присоединение субстрата
Каталитический центр, отвечающий за химическое превращение субстрата.
Свойства АЦ:
Эффект сближения и ориентации реагентов: в АЦ фермента субстраты
располагаются таким образом, чтобы участвующие в реакции функциональные группы субстратов находились в непосредственной близости друг к другу. Такое упорядоченное расположение субстратов вызывает уменьшение энтропии и, как следствие, снижение энергии активации (Еа), что определяет каталитическую эффективность ферментов.
Эффект деформации субстрата: АЦ фермента также способствует
дестабилизации межатомных связей в молекуле субстрата, что облегчает протекание химической реакции и образование продуктов
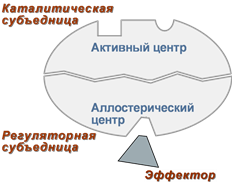
Регуляторный (аллостерический) центр – с этой зоной фермента
взаимодействуют вещества, влияющие на его каталитическую активность.
Гипотезы соответствия:
1. Гипотеза «Ключ-замок» - АЦ фермента комплементарен субстрату, т.е.
соответствует ему как "ключ замку". После взаимодействия субстрата ("ключ") с активным центром ("замок") происходят химические превращения субстрата в продукт. АЦ при этом рассматривался как стабильная, жёстко детерминированная структура.
2. «Гипотеза индуцированного соответствия» (рука-перчатка) – АЦ является
гибкой стр-рой по отношению к субстрату. Субстрат, взаимодействуя с АЦ фермента, вызывает изменение его конформации, приводя к формированию фермент-субстратного комплекса, благоприятного для химических модификаций субстрата. При этом молекула субстрата также изменяет свою конформацию, что обеспечивает более высокую эффективность ферментативной реакции.
Механизм действия ферментов:
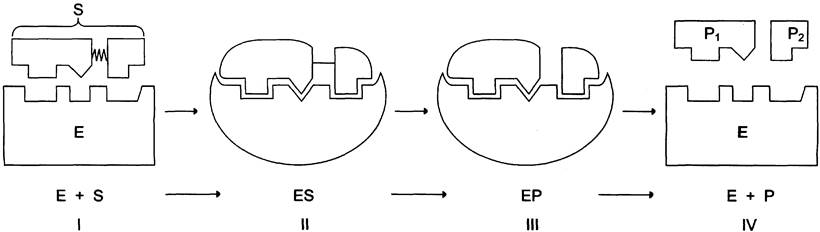
I – этап сближения и ориентации субстрата относительно активного центра фермента;
II – образование фермент субстратного комплекса (ES) в результате индуцированного соответствия;
III – деформация субстрата и образование нестабильного комплекса фермент-продукт (ЕР);
IV – распад комплекса (ЕР) с высвобождением продуктов реакции из активного центра фермента и освобождением фермента.