Материал: 1 аттестация патфиз (5 семестр)
Гемоглобинопатии (серповидно-клеточная анемия)
Патогенез — генетический дефект в структурном гене ⇒ нарушается структура β-цепей глобина в связи с заменой одной аминокислоты (чаще глютамина) на другую (валин).
В основе образования серповидных клеток лежит свойство HbS полимеризоваться при переходе в восстановленную форму. Образующиеся полимеры (длинные нити) группируются в тактоиды, они изменяют форму и вид эритроцитов. Полимеризация восстановленного HbS связана с его низкой растворимостью (в 25 раз ↓ растворимости HbA). Образование тактоидов зависит от концентрации HbS в эритроците и парциального давления кислорода в крови.
Болезнь протекает в виде кризов. Различают болевые (тромботические, вазоокклюзионные), гемолитические, секвестрационные и апластические. У взрослых наиболее часто выявляют болевые кризы, у детей гемолитические.
Талассемия
Талассемия (греч. talasia — море) ⇒ дефицит HвA без качественных нарушений его глобиновых цепей.
Возникает вследствие патологии генов-регуляторов ⇒ в процессе эмбриогенеза не происходит нормального переключения синтеза глобиновых цепей и начинается образование аномальных гемоглобинов в ущерб синтезу основного нормального гемоглобина (HbA).
В зависимости от того, синтез каких цепей (α или β) снижен, выделяют две группы талассемий: α-талассемию и β-талассемию.
При α-талассемии этиологическим фактором является частичная или полная делеция α-глобиновых генов-регуляторов, в результате ↓ синтез этих цепей. Недостаточное их количество компенсируется в эмбриональном периоде избыточным синтезом ץ-глобиновых цепей. Этот гемоглобин называется Нb Bart's (от названия госпиталя Святого Варфоломея в Лондоне). После рождения недостаток α-глобиновых цепей восполняется синтезом β-глобиновых цепей. Такой гемоглобин называют HbH (HbBart's и HbH - маркеры α-талассемии).
Клиническое проявление α-талассемии — гипоксия, которая возникает вследствие высокого сродства HbBart's и HbH к килороду. Анемия усугубляется повышенным разрушением эритроцитов в увеличенной селезенке.
К анемиям, развивающимся вследствие нарушений синтеза глобинов (гемоглобинопатии), относятся множество заболеваний, в том числе талассемии и серповидно-клеточная анемия.
Патогенез гемолитических анемий
Общий механизм лизиса эритроцитов (рис. 21–7) заключается в дезорганизации фосфолипидно‑белковой структуры их мембраны.
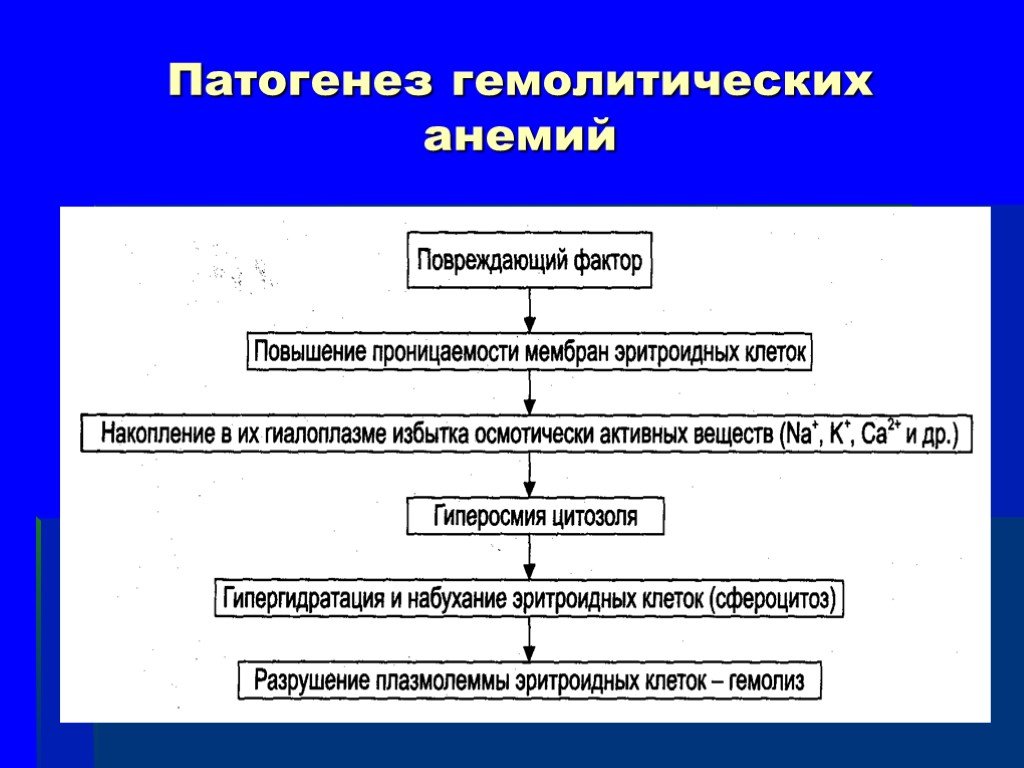
Рис. 21–7. Изменения в эритроцитах, ведущие к их гемолизу.
Проявления гемолитических анемий
Проявления гемолитических анемий разнообразны и в значительной степени определяются конкретным заболеванием. Наиболее общие проявления представлены на рис. 21–8.
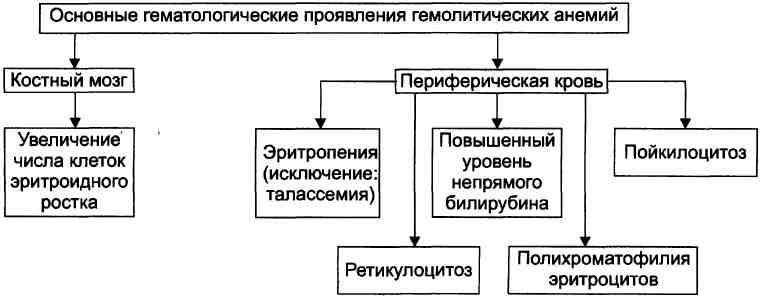
Рис. 21–8. Основные гематологические проявления гемолитических анемий.
В костном мозге. Как правило, сохраняется нормобластический тип кроветворения. Однако после выраженных гемолитических кризов могут появляться мегалобласты.
В периферической крови. Выраженность анемии различна в зависимости от их причин и состояния организма.
- При гемолитических кризах ⇒ Нb может ↓ до 40–50 г/л.
- В периоды стабильного состояния ⇒ 90–110 г/л. Количество эритроцитов, как правило, ↓ в разной степени. Содержание ретикулоцитов ↑, обычно от 5 до 12%.
Уровень Нb в эритроцитах (ЦП) как при приобретенных, так и наследуемых ГА близок к норме или несколько выше ее.
При приобретенных ГА хронического течения часто цветовой показатель < 0,85.
Дизэритропоэтические анемии
В зависимости от происхождения делят на две группы:
Обусловленные нарушением эритропоэза в связи с преимущественным повреждением стволовых клеток: гипо- и апластические анемии.
Обусловленные нарушением эритропоэза в связи с преимущественным повреждением клеток- предшественников миелопоэза и/ или эритропоэтинчувствительных клеток:
- вследствие нарушения синтеза нуклеиновых кислот эритроплазмоцитов (мегалобластические): витамин В12 — и/или фолиево-дефицитные анемии (болезнь Аддисона–Бирмера); - в результате нарушения синтеза гема (железодефицитные анемии); - вследствие нарушения синтеза глобина: талассемии; серповидно-клеточная анемия.
Дизэритропоэтические анемии дифференцируют в зависимости от происхождения (рис. 21-9).
Гипопластическая и апластическая анемии
Как правило, не представляют собой определенной нозологической формы, а являются синдромом других патологических процессов.
По происхождению могут быть: а) приобретенными (вторичными) или б) наследуемыми (первичными).
Приобретенные — чаще результат действия одного или нескольких из трех групп причинных факторов:
1) физического характера (ионизирующая радиация);
2) химического характера (чаще лекарственные: левомицетин, бутадион, аминазин, цитостатики);
3) биологического происхождения (чаще вирусы: инфекционный гепатит, инфекционный мононуклеоз).
Патогенез. Любой из указанных факторов (или их комбинация) обусловливает нарушение пролиферации и/или гибель стволовых гемопоэтических клеток, включая эритропоэтические, что и ведет к гипо- или апластическим анемиям.
Наследственная апластическая анемия (Фанкони)
Причина — наследуемый по рецессивно-аутосомному типу дефект гемопоэтических клеток.
Патогенез нарушение процессов репарации ДНК стволовых клеток.
Проявления. В костном мозге значительное ↓ числа ядросодержащих клеток миелоидного ряда. Нередко обнаруживается ↑ числа лимфоидных клеток различной степени зрелости.
В периферической крови панцитопения (↓ числа всех видов клеток крови). Исключение - лимфоциты. Содержание Нв в каждом эритроците в норме, однако общая концентрация его в крови резко ↓ (в связи с эритропенией), достигая нередко уровня 20–30 г/л. Количество ретикулоцитов ↓. Многие эритроциты превышают нормальный размер (макроцитоз, анизоцитоз) в связи с элиминацией незрелых клеток из костного мозга. Продолжительность жизни эритроцитов ↓.
Клинически ⇒ признаки гипоксии, тромбоцитопении (кровотечения), лейкопении (инфекции).
В12-дефицитная анемия
Причины: нарушение поступления с пищей в организм витамина В12 или нарушение его усвоения.
Недостаток витамина в результате снижения его всасывания может быть следствием:
1) ↓или прекращения синтеза внутреннего фактора (Кастла);
2) нарушения всасывания комплекса витамин + гликопротеин в подвздошной кишке;
3) повышенного расходования витамина, «конкурентного» использования его в кишечнике микробами.
Неусвоение В12 в кишечнике может быть обусловлено паразитарной инфекцией. Конкурент широкий лентец. Вспомогательный диагностический признак дифилоботриозна эозинофилия. Парентеральное введение В12 в количестве, потребляемом лентецом, способно вызвать у хозяина ремиссию. Фиксация паразита ниже подвздошной кишки — основного места всасывания В12, не приводит к развитию анемии.
Патогенез. Недостаток витамина В12 любого происхождения обусловливает нарушение синтеза нуклеиновых кислот в эритрокариоцитах, а также обмена жирных кислот в них и в клетках других тканей.
Проявления. В костном мозге обнаруживаются мегалобласты (d > 15 мкм), а также мегалокариоциты. Нарушается дифференцировка и других клеток миелоидного ряда.
В периферической крови значительно ↓ число эритроцитов, иногда до 0,7-0,8 х10¹²/л. Они большего размера, овальной формы, без центрального просветления. Встречаются мегалобласты. В эритроцитах обнаруживаются остатки ядерного вещества (тельца Жолли) и нуклеолеммы (кольца Кебота). Характерны анизоцитоз и пойкилоцитоз. ЦП=1,1–1,3. Однако общее содержание Нb в крови существенно ↓ в связи с уменьшением числа эритроцитов. Количество ретикулоцитов чаще ↓, как правило, наблюдается лейкопения (за счет нейтрофилов). В связи с ↑гемолизом — билирубинемия.
В12-дефицитная анемия сопровождается и другими признаками авитаминоза: изменения в слизистых оболочках ЖКТ глоссит, формирование «полированного» языка (атрофия его сосочков), стоматит, гастроэнтероколит и неврологический синдром (вследствие изменений в нейронах). Все это усугубляет течение анемии.
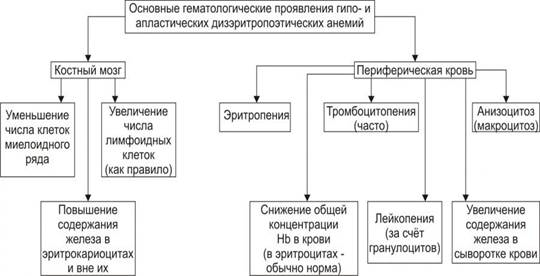
Рис. 21–10. Основные гематологические проявления гипо‑ и апластических дизэритропоэтических анемий.
Анемии, развивающиеся при нарушениях обмена железа
Составляет 2/3 от всех разновидностей анемий.
Причина превышение потерь организмом железа в сравнении с его поступлением. ↓ содержание железа в плазме крови, костном мозге и в тканевых депо.
Железодефицитные анемии возникают при следующих состояниях:
1) хронических кровопотерях;
2) ↑ потребности в железе на фоне его экзогенной недостаточности (при беременности, лактации);
3) ↑ потоотделении (с потом выводится много железа, при проживании в жарком климате, работе в горячих цехах и тд);
4) неусвоении железа организмом: при ахлоргидрии (HCL ионизирует железо -необходимо для усвоения); при авитаминозе С (витамин C стабилизирует железо в двухвалентном состоянии, а трехвалентное железо не усваивается); при энтеритах и массивной резекции тонкой кишки;
5) у новорожденных при длительном однообразном (с дефицитом железа) вскармливании.
Патогенез. Дефицит железа в плазме крови и клетках организма обусловливает ↓ его содержания в митохондриях эритрокариоцитов костного мозга. Это тормозит синтез гема, соединение его с глобином.
Нарушается синтез других железосодержащих соединений как в эритроцитах, так и в других клетках (цитохромы, каталазы, пероксидазы). Это обусловливает ↓ резистентности к повреждающему действию перекисных соединений, ↑ их гемолиз и ↓ продолжительность жизни.
Проявления. В костном мозге нормобластический тип кроветворения, часто наблюдается умеренная гиперплазия клеток красного ростка гемопоэза.
Проявления железодефицитных анемий приведены на рис. 21–14.
Рис. 21–14. Основные гематологические проявления железодефицитных анемий.
Легкая степень анемии – содержание Fe²+↓ до 9 мкмоль/л;
Средняя степень тяжести - Fe²+ ↓до 7 мкмоль/л;
Тяжелая форма - Fe²+ < 7 мкмоль/л;
Нормальное содержание железа в сыворотке крови составляет 9-31 мкмоль/л
Прелатентная фаза. Истощается депо железа (гемосидерина, ферритина), не изменяется уровень сивороточного железа, показатели периферической крови, но появляются симптомы анемии;
Латентная стадия характеризуется ↓ концентрации сывороточного Fe²+ и степени насыщения им трасферрина ► ↓ траспорта Fe²+ в костный мозг;
Стадия выраженных клинических проявлений. В крови появляются гипохромные эритроциты, ЦП- 06 и <, гипорегенераторные проявления (Рет<0,2%).
Ткани и органы. В большинстве тканей организма развиваются различные дистрофии. Они вызваны дефектами структуры и функциональной активности железосодержащих ферментов и других соединений (например, глутатионпероксидаз, каталазы, пероксидаз, цитохромов, миоглобина). В связи с этим, а также вследствие развития тканевой гипоксии, выявляются мышечная слабость (миастения), шелушение, трещины кожи и слизистых оболочек, повышенная ломкость ногтей, выпадение волос, изменения стенки ЖКТ (сопровождающиеся гипотрофическим глосситом, гастритом, энтеритом).
Лечение дизэритропоэтических анемий
Терапия дизэритропоэтических анемий направлена на: — устранение или прекращение действия причинных факторов, вызывающих нарушение пролиферации и дифференцировки эритроидных клеток (этиотропная терапия); — разрыв патогенетических звеньев анемических состояний: гипоксии, гемосидероза, нарушений КЩР (патогенетическое лечение); — устранение последствий и неприятных симптомов анемий (симптоматическая терапия).
Вопрос 5 Проявления анемий в полости рта
Пациенты отмечают неприятный, гнилостный запах изо рта. Наблюдают кровоточивость десен, которая может быть спонтанной при нанесении мелких травм слизистой оболочки полости рта в период гемолитического криза. Также могут появляться долго незаживающие язвы, которые образуются при механической травме или при наличии неполноценного ортопедического протеза, или ортодонтической конструкции. В зависимости от течения процесса изменяется цвет зубов от желтого до серо-грязного и отмечается частое поражение твердых тканей зубов кариесом. В редких случаях может отмечается желтушность слизистой оболочки полости рта. Пациенты отмечают извращение вкуса (расстройство вкусовой чувствительности), преобладает чувство горечи. Язык блестящий, гладкий, болезненный и резко чувствителен (порог реакции на раздражитель уменьшается). У некоторых пациентов может нарушаться прикус из-за чрезмерной гипертрофии альвеолярного края: зубы выдвигаются, тем самым образуются большие промежутки между ними, также может формироваться остеопороз челюстей.
Лечение. Наряду с патогенетической заместительной терапией проводят симптоматическое лечение. Гнилостный запах изо рта может появиться вследствие отложения в пришеечной области зубного камня. Чтобы от него избавиться проводят профессиональную гигиену полости рта, но с осторожностью, ведь десна легко кровоточит. Методы лечения включают лекарственные средства местного применения, средства для полоскания рта и лекарства для полости рта.
Вопрос 6 Патофизиология системы лейкоцитов
В
крови взрослого здорового человека в
условиях покоя до приёма пищи содержится
4–9109/л
лейкоцитов. Большое число лейкоцитов
находится также за пределами сосудистого
русла — в тканях, где они участвуют в
реализации реакций иммунного надзора.
Типовые изменения в системе лейкоцитов характеризуются сочетанными или парциальными отклонениями по ряду параметров (рис. 21–18).
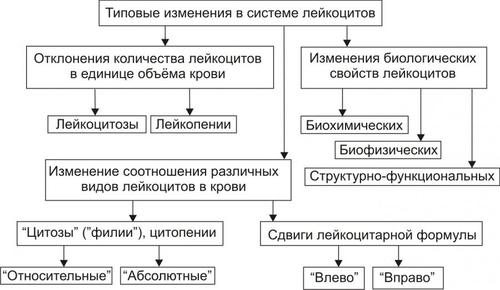
Рис. 21–18. Типовые изменения в системе лейкоцитов.
Типовые изменения количества лейкоцитов в единице объёма крови
К типовым изменениям количества лейкоцитов в единице объёма крови относятся лейкопении и лейкоцитозы.
И лейкопении, и лейкоцитозы, как правило, не являются самостоятельными заболеваниями, а относятся к реакциям, развивающимся при различных болезнях, патологических процессах и состояниях. Излечение болезни, ликвидация патологического процесса или болезненного состояния приводят к более или менее быстрой нормализации общего числа или количества отдельных форм лейкоцитов, соотношения их зрелых клеток, исчезновению признаков дегенерации и не требуют специального лечения.
Отклонения количества находящихся в периферической крови лейкоцитов, а также качественные изменения в них в определённой степени позволяют судить о наличии патологического процесса и динамике его течения, т.е. имеют диагностическое значение (в отличие, например, от лейкозов — самостоятельных заболеваний, имеющих определённые причины, механизмы развития, проявления и требующие специального лечения).
Лейкопении
Лейкопении
— состояния, характеризующиеся
уменьшением количества лейкоцитов в
единице объёма крови ниже нормы (обычно
менее 4109/л).
Различают первичные (врождённые или
наследственные) и вторичные (приобретённые)
лейкопении.
Первичные лейкопении
К первичным лейкопениям (в подавляющем большинстве случае речь идёт о нейтропениях) относятся врождённая алейкия, семейные нейтропении, периодическая наследственная нейтропения, болезнь Костманна, синдромы Грисчелли, «ленивых» лейкоцитов, Шедьяка‑Хигаси и некоторые другие.
Вторичные лейкопении
Вторичные лейкопении
Причины вторичных (приобретённых) лейкопений:
• Чаще всего это физические и химические агенты: ионизирующая радиация; химические вещества — бензол, инсектициды, ЛС (к нейтропении и даже агранулоцитозу могут привести НПВС, антиметаболиты, сульфаниламиды, барбитураты, диакарб, левомицетин, изониазид, алкилирующие вещества (циклофосфамид), противоопухолевые антибиотики.