Материал: шпоры материаловедение
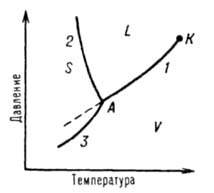
Рис. 1 Диаграмма состояния однокомпонентной системы. S, L и V - соотв. области существования твердой, жидкой и паровой фаз; 1, 2 и 3 кривые кипения (испарения), плавления и возгонки (сублимации) соотв., К критич. точка; А тройная точка.
Д и а г р а м м ы п л а в к о с т и. Такие Д. с. служат для установления условий равновесия между твердыми и жидкими фазами. Рассмотрим их осн. типы. Простейший вариант соответствует случаю, когда компоненты А и В образуют одну жидкую фазу (расплав или р-р), при охлаждении к-рой только выделяются (кристаллизуются) индивидуальные в-ва (не образуются ни твердые р-ры, ни хим. соед.).
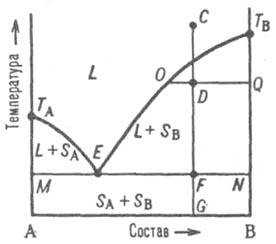
Рис. 2. Диаграмма плавкости двойной системы, компоненты к-рой А и В не образуют твердых р-ров. L - область существования жидкости (расплава), (L + SA) и (L + SB) области сосуществования жидкой фазы и твердых А и В соотв.; (SA + SB) область существования мех. смеси твердых А и В. ТАETВ и MEN - линии ликвидуса и солидуса соотв., E-эвтектич. точка. С, D, F, G, О и Q фигуративные точки (пояснения в тексте).
На Д. с. (рис. 2) линия, изображающая зависимость от состава т-ры начала выделения из жидкой фазы твердого компонента (начала равновесной кристаллизации), наз. линией ликвидуса. Она состоит из двух ветвей ТАЕ и ТВЕ, отграничивающих фазовое поле жидкости L от полей сосуществования жидкой фазы с твердыми А и В соотв. (поля L + SA и L + SB). Линия, изображающая зависимость от состава т-ры окончания равновесной кристаллизации при охлаждении (или начала плавления при нагр.), наз. линией солидуса. Ниже нее расположено фазовое поле SA + SB твердого состояния системы, отвечающее условиям сосуществования двух твердых фаз. Происходящие в системе фазовые изменения описываются след. образом. При охлаждении жидкой фазы, напр., из начального состояния С, фигуративная точка системы в целом движется вниз вдоль прямой CG. В точке ее пересечения с линией ликвидуса начинается кристаллизация компонента В, система становится двухфазной и дивариантной или, поскольку давление фиксировано, условно моновариантной.
Рис. 3. Диаграмма плавкости двойной системы эвтектич. типа с ограниченными твердыми р-рами. L, a и b - области существования жидкой фазы (расплав) и твердых р-ров В в А и А в В соотв.; (L + a) и (L + b) - области сосуществования жидкой фазы и твердых р-ров a и b соотв.; (a + b) - область сосуществования двух твердых р-ров. ТАЕТВ и MEN - линии ликвидуса и солидуса соотв., E - эвтектич. точка.
При охлаждении затвердевшей смеси ниже линии солидуса MN происходит изменение концентраций твердых р-ров a и b соотв. по линиям MF и NG, к-рые дают температурную зависимость растворимости в твердом состоянии В в А и А в В. 2) Равновесие при т-ре Тр, к-рая является промежуточной между т-рами плавления ТА и ТB. Если, напр., т-ра начала кристаллизации расплава с высоким содержанием А выше ТА (рис. 4), а с высоким содержанием В - ниже ТB, линия ликвидуса состоит из двух ветвей ТАР и ТВР, соответствующих кристаллизации твердых р-ров a и b.
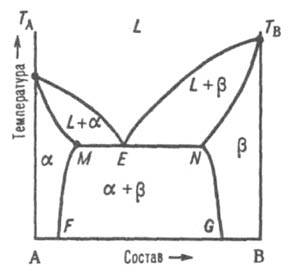
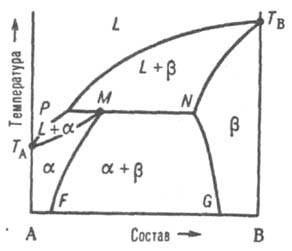
Рис. 4. Диаграмма плавкости двойной системы перитектич. типа. Р - перитектич. точка, остальные обозначения те же, что и на рис. 3.
Эти ветви пересекаются в т. наз. перитектич. точке Р - фигуративной точке жидкой фазы, к-рая может равновесно сосуществовать одновременно с двумя твердыми р-рами a и b, составы к-рых определяются точками М и N. Линия солидуса состоит из трех ветвей: ТAМ, MN и NTB. При охлаждении двухфазной системы (L + b) до перитектич. т-ры Тр в системе появляется третья фаза - р-р a. При протекании перитектич. превращения (фазовой р-ции) жидкость (расплав) + твердый р-р b D твердый р-р a система моновариантна, или условно нонвариантна, т. е. при данном давлении равновесие возможно лишь при постоянных т-ре и составах каждой из фаз. Если после окончания перитектич. р-ции остается избыток жидкой фазы, система переходит в двухфазное поле (L + a). При дальнейшем охлаждении происходит кристаллизация твердого a-раствора. Послед. понижение т-ры (ниже линии МF) приводит к тому, что однородный твердый a-раствор становится неустойчивым и, распадаясь, выделяет нек-рое кол-во р-раствора, состав к-рого отвечает линии NG. Если после окончания перитектич. р-ции полностью исчезает жидкая фаза, система переходит в двухфазное поле a + b; по мере снижения т-ры составы a- и b-растворов изменяются в соответствии с ходом линий MF и NG. Возможны и др. трехфазные равновесия, напр., при наличии у одного из компонентов полиморфных модификаций, когда все три сосуществующие фазы являются твердыми. Полиморфная модификация g может участвовать в т. наз. эвтектоидном превращении g D a + b или в перитектоидном превращении g + a D b, в принципе аналогичных рассмотренным выше эвтектич. и перитектич. превращениям. При метатектическом превращении модификация g при охлаждении распадается на твердую и жидкую фазы: g D a + L. Третий тип диаграммы описывает состояния двойной системы, компоненты к-рой А и В образуют устойчивое хим. соед., к-рое не разлагается вплоть до т-ры плавления и переходит в жидкую фазу того же состава, т. е. плавится конгруэнтно.
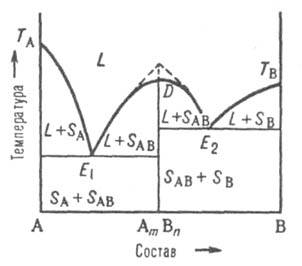
Рис. 5. Диаграмма плавкости двойной системы, компоненты к-рой А и В образуют конгруэнтно плавящееся хим. соед. АmВn. D - сингулярный максимум, Е1 и Е2 - эвтектич. точки; остальные обозначения те же, что и на рис. 3 и 4.
В точке плавления, соответствующей стехиометрич. составу АmВn, на линии ликвидуса имеется сингулярный максимум (рис. 5); это значит, что линия D - АmВn разделяет систему на две подсистемы. На диаграмме максимуму отвечает излом (показан пунктиром на рис. 5). В каждой из подсистем взаимод. между компонентами, соотв. А и АmВn, В и АmВn, может быть представлено диаграммами эвтектич. или перитектич. (или любого другого) типа. Если соед. AmBn частично диссоциировано в жидкой фазе, максимум на кривой ликвидуса несколько сглажен в соответствии со степенью диссоциации. Если соед. АmВn диссоциирует и в твердом состоянии, то сглаженный максимум будет и на линии солидуса. Однако независимо от вида максимума, общий характер фазового равновесия в системе определяется характером взаимод. соед. АmВn с компонентами А и В.
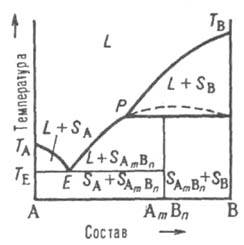
Рис. 6. Диаграмма плавкости двойной системы, компоненты к-рой А и В образуют инконгруэнтно плавящееся хим. соед. АmВn, обозначения те же. что и на рис. 4 и 5.
Четвертый тип диаграмм. Компоненты А и В образуют хим. соед., разлагающееся ниже т-ры плавления (т. наз. инконгруэнтное плавление). Напр., при охлаждении жидкости (расплава) до нек-рой т-ры Тр (рис. 6) кристаллизуется только компонент В; при Тр происходит перитектич. р-ция с образованием хим. соед. АmВn в твердом состоянии, т. е. р-ция твердая фаза SВ + расплав перитектич. состава D твердая фаза SА(m)В(n). Если при этом в твердой фазе компонент В имеется в избытке, в результате перитектич. р-ции исчезает жидкая фаза и при дальнейшем охлаждении ниже Тр остается смесь двух твердых фаз SB и SА(m)B(n). Если же в твердой фазе компонента В недостает, в результате р-ции исчезают кристаллы В и жидкость при дальнейшем охлаждении выделяет кристаллы соед. АmВn, изменяя свой состав по линии ликвидуса РЕ. При т-ре ТЕ происходит эвтектич. кристаллизация AmBn и А. Возможны и др. варианты диаграммы. Описанные типы диаграмм плавкости могут усложняться из-за полиморфизма как компонентов А и В, так и соед. АmВn.
Диаграммы растворимости. При отсутствии в системе твердых фаз Д. с. состоит из области существования одной жидкой фазы (т. наз. области гомогенности) и области сосуществования двух насыщенных жидких р-ров разного состава, образующих несмешивающиеся друг с другом слои (рис. 7). Кривая, разделяющая эти области, наз. бинодалью. Так, при т-ре Т1 в равновесии находятся р-р компонента В в А (его состав отвечает точке С) и р-р А в В (его состав отвечает точке D). Если однородный р-р 1 охладить до т-ры Т1, он распадется на две жидкие фазы.
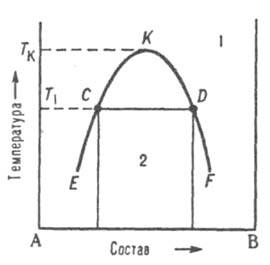
Рис. 7 Диаграмма растворимости двойной системы, компоненты к-рой А и В ограниченно растворимы друг в друге; 1 область существования однородного р-ра, 2 область сосуществования двух насыщенных р-ров; ECKDF - бинодаль, CD - нода, К -верхняя критич. точка растворимости.
Обычно при повышении т-ры взаимная растворимость жидкостей увеличивается, поэтому по своим св-вам оба насыщенных р-ра, составы к-рых изменяются по отрезкам бинодали ЕК и KF, сближаются. Наконец, при т-ре Tк различие между ними исчезает; эта т-ра наз. критической т-рой растворимости (смешения), выше нее может существовать лишь одна жидкая фаза. Большинство систем с расслоением р-ров характеризуются только одной критич. т-рой р-римости, чаще всего верхней, т. е. на Д. с. имеют незамкнутую снизу бинодаль. Если в таких системах не образуются хим. соед., область сосуществования двух жидких фаз ограничена снизу кривой кристаллизации одного из компонентов при т-ре превращения жидкая фаза 1 D жидкая фаза 2 + твердая фаза. Такое трехфазное равновесие наз. монотектическим; оно по своей термодинамич. природе аналогично эвтектическому или эвтектоидному. При синтектическом трехфазном равновесии две жидкие фазы взаимодействуют с образованием твердого соед. Такое равновесие аналогично перитектическому. В нек-рых системах бинодаль имеет форму замкнутой кривой (овал), т. е. система имеет две т-ры смешения верхнюю и нижнюю. Диаграмма равновесия жидкость-пар. При р = const каждому составу жидкой смеси отвечает определенная т-ра равновесия с паром и определенный состав пара, отличающийся, как правило, от состава жидкой смеси.
На Д. с. (рис. 8, а) кривые кипения и конденсации изображают зависимости т-р начала кипения и конденсации от состава и отделяют поля жидкости L и пара V от поля (L + V)гетерог. состояний жидкость-пар. На кривой кипения м. б. экстремум: максимум (рис. 8, б) или минимум (рис. 8, в); в этих точках кривая кипения касается кривой конденсации, т. е. составы равновесных жидкости и пара совпадают Жидкие смеси такого состава полностью выкипают, подобно чистым жидкостям, при постоянной т-ре без изменения состава (см. Азеотропные смеси). Д. с., описывающие равновесия двухкомпонентных твердых р-ров с жидкими р-рами и жидких р-ров с паром, подобны.
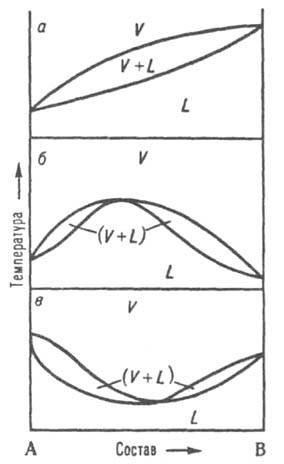
Рис. 8. Диаграммы состояния, двойной системы, описывающие равновесие жидкость - пар. L и V области существования жидкости и пара соотв.. (L + V) область сосуществования жидкой и паровой фаз; а система без азеотропной точки; б и в два типа азеотропных смесей
№13. Свойства сплавов. В металловедение различают три типа сплавов: твердый раствор, механическую смесь, химическое соединение. Если атомы входящие в состав сплава элементов незначительно отличаются строением и размером, они могут образовывать общую кристаллическую решетку, то такой сплав называется твердым раствором. Если каждый элемент сплава кристаллизуется самостоятельно, то это механическая смесь. Если элементы сплава химически взаимодействуют, образуя новое вещество, то такой сплав называют химическим соединением.Железо имеет четыре полиморфные модификации и переход из одной в другую происходит при критических температурах при охлаждении с выделением теплоты, а при нагревании — с поглощением теплоты. Большое значение для практики имеет свойство y-Fe растворять до 2,14% углерода при температуре 1147°С с образованием твердого раствора и с внедрением атомов углерода в кристаллическую решетку.Твердый раствор углерода в y-Fe называется аустенитом, почти в 100 раз меньше углерода, может раствориться в a-Fe, причем твердые растворы углерода и других элементов в a-Fe называют ферритом. Кроме твердых растворов в железе в железоуглеродистых сплавах может быть химическое соединение железа с углеродом — карбид железа Fe3C. Это соединение, называемое цементитом, со держит 6,67 % углерода, имеет сложное кристаллическое строение с плотно упакованной ромбической кристаллической решеткой В сплавах цементит является метастабильной фазой. Его темпера тура плавления равна примерно 1500°С.Феррит отличается мягкостью и пластичностью; его прочность сравнительно невысока — предел прочности при растяжении 250 МПа, относительное удлинение 50%, твердость НВ составляет 800 МПа. Аустенит также имеет высокую пластичность, низкий предел прочности при растяжении. Твердость аустенита НВ 1700 — 2200 МПа. Цементит обладает низкой пластичностью, высокой твердостью НВ, равной 10 000 МПа, и хрупкостью.При охлаждении жидких сплавов сначала происходит кристаллизация, а затем после отвердения — фазовые структурные превращения вследствие полиморфизма железа и изменения растворимости углерода в аустените и феррите. По содержанию углерода железоуглеродистые сплавы подразделяют на стали, содержащие до 2,14% углерода, и чугуны с содержанием углерода более 2,14 %. Принятая граница между сталями и чугунами соответствует наибольшей растворимости углерода в аустените.Стали после отвердения не содержат легкоплавкой эвтектики — ледебурита, — характерной для чугуна при содержании углерода 4,3 %. При высоком нагреве стали имеют структуру чистого аустенита. В зависимости от процентного содержания углерода желез-ноуглеродистые сплавы имеют следующие наименования:техническое железо (С < 0,02 %);доэвтектоидные стали (С = 0,02...0,8 %);эвтектоидные стали (С = 0,8 %);заэвтектоидные стали (С = 0,8... 2,14 %);доэвтектические чугуны (С = 2,14...4,3 %);эвтектика — ледебурит (С = 4,3 );заэвтектические чугуны (С = 4,3...6,67 %).Сплавы железа с углеродом после окончания кристаллизации имеют различную структуру, но одинаковый фазовый состав; при температурах ниже 727 °С они состоят из феррита и цементита.
Механические свойства сплавов
Механические свойства сплавов определяли при статическом растяжении. Чувствительность к концентрации напряжений устанавливали по отношению предела прочности образца с надрезом к пределу прочности основного материала ( аав ). Механические свойства сплавов при 7 = 300 и 77 К
При температуре 300 К с увеличением содержания олова прочность сплавов монотонно увеличивается, причем разность между пределом прочности и пределом текучести у всех сплавов почти не изменяется. У сплавов с содержанием олова до 8% удлинение и сужение уменьшаются незначительно, тогда как у сплавов с большим содержанием олова наблюдается значительное уменьшение пластичности.
Химические свойства характеризуются способностью металлов и сплавов отдавать электроны при взаимодействии с другими веществами. При этом происходит окисление металлов. Следовательно, при всех химических взаимодействиях металлы являются восстановителями. По легкости отдачи электронов металлы располагаются в ряд активности: Mg, Al, Zn, Cr, Fe, Co, Ni, Sn, Pb, H, Cu, Sb, Bi, Ag, Pt, Au и т. д. Чем левее в ряду активности находится металл, тем легче он окисляется и труднее восстанавливается из своих ионов. Каждый металл, находящийся в ряду активности левее, вытесняет любой последующий из растворов его солей. При этом менее активный металл восстанавливается. Наиболее химически активные металлы и сплавы способны окисляться на воздухе при нормальных условиях и при нагревании. С повышением температуры особенно активно происходит окисление металлов. К технологическим свойствам металлов и сплавов относятся: литейные, ковкость, или деформируемость, в горячем и холодном состоянии, свариваемость, прокаливаемость и об-рабатываемость резанием.
№14. Понятие об упругой и пластической деформации металлов
Действие приложенные к металлу мех. нагрузки вызывают ее деформацию, которая бывает упругой и пластической. При упругой деформации происходит незначительное изменение в вмежатомном расстоянии кристаллической решетки металла, а также в его структуре и свойствах. Все эти изменения при сжатии деф. силы исчезают и кристаллы металла преобретают форму и размеры которые имели до деформации.
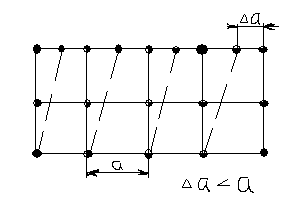
При пластичной диформации происходит необратимые изминения в межатомном расстоянии а также в его структуре и свойствах. После снятия нагрузки все эти изменения остаются.
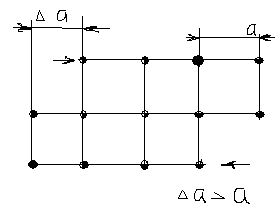
При пласт. деф. смещение атомов больше межатомного расстояния. Пласт. деф. осуществляется скольжением и двойникованием. При пластич. диф. скольжении происходит смещение одной части металла относительно второй. При пласт. диф. двойникование одна часть кристалла смещается относительно другой на некоторый угол. Наибольшей пластичностью при деф. обладают металлы с ГЦК и ОЦК. В результате пластической деф. зерно металла деформируется, вытягивается вдоль действующей силы (вдоль линии течения металла).
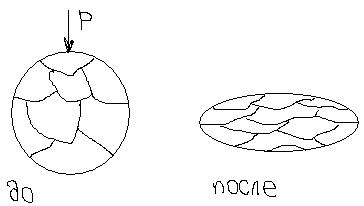
№15. Пластической называют такую деформацию, при которой после снятия внешней нагрузки тело не восстанавливает первоначальную геометрическую форму и размеры. Наклёп — упрочнение металлов и сплавов вследствие изменения их структуры и фазового состава в процессе пластической деформации, при температуре ниже температуры рекристаллизации. Пластичность — это свойство металлов изменять под действием внешних сил свою форму без разрушения. Некоторые металлы и сплавы пластичны в холодном состоянии (свинец, алюминий), другие обладают хорошей пластичностью лишь в нагретом состоянии (сталь), третьи хрупки как в холодном, так и в нагретом состоянии (чугун)..При горячей обработке давлением свойства металлов улучшаются: происходит уплотнение металла, образуется мелкозернистая структура, более однородная, чем в литом металле. Одновременно металл получает волокнистое строение, что обусловливает его различные механические свойства вдоль и поперек волокон и является недостатком процесса горячей обработки металлов давлением. Температурный интервал горячей пластической деформации для металлов и сплавов различен. Например, ля углеродистой стали верхний предел нагрева в зависимости от марки равен 1200—1000° С, а нижний 850— 900° С. Пластическая деформация металлов в теплом и холодном состоянии сопровождается его упрочнением. С увеличением степени деформации увеличивается сопротивление деформации.
Применяя отжиги между проходами при волочении, можно понизить прочность проволоки, однако при дальнейшем волочении прочность возрастает еще более интенсивно.
№16. Хрупкое и вязкое разрушение имеют разные виды разрушенной поверхности. Возможно обнаружить дефекты на этой поверхности. Дефекты в зонах растягивающих напряжений обычно - главный источник усталостных трещин.
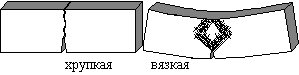
Вязкость разрушения - это относительное повышение растягивающих напряжений в устье трещина при переходе ее от стабильной к не стабильной стадии роста. Вязкость разрушения тесно связана с показателями прочности материала увеличение прочности сопровождается снижением пластичности и вязкости разрушения. Это объясняется тем, что у высокопрочных материалов мала энергия, поглощаемая при разрушении уровень которой определяется величиной пластической деформации у вершины трещины.Вязкая трещина определяется относительным развитием нормально и наклонно участков разрушения. У достаточно толстых образцов с высоко развитой поверхность нормально разрушения вязкость разрушения приближается к предельному значению в условиях плоской деформации. Основным недостатком испытаний на вязкость разрушения в условиях плоской деформации является необходимость использования больших образцов при исследовании материалов средней и низкой прочности.Металлы в твердом состоянии и отчасти в жидком состоянии обладают высоко тепло - и электропроводностью, а также положительным температурным коэффициентом электросопротивления. Большое количество металлов обладает сверхпроводимостью, термоэлектронной эмиссией хорошей отражательной способностью. Устойчивость металла, представляющего собой иона - электронную решетку, определяется электрическим притяжением между положительно заряженными ионами и обобщенными электронами. Такое взаимодействие имеет название металлической связи.
№17.Рекристаллизация;первичная и вторичная ; рекристаллизационный отжиг
Величина зерна после рекрист. и ее влияние на структуру и свойства Ме. действие пластической деформация приводит Ме в структурно неустойчивое состояние. Вернуть Ме в структурно устойчивое состояние можно с помощью нагрева.. В результате нагрева в упрочнённом металле протекают два процесса: возврат и рекристаллизация, которые возвращают упрочненному металлу все его свойства до деформации, т.е :1-снятие искажения кристаллической решётке Ме; 2- зарождение и рост новых равноостных зёрен взамен старых деформируемых.
Процесс возврата протекает при t ниже 0,2÷0,3 t плавления Ме в результате которого :1-уменьшается количество точечных и линейных дефектов;2-снемаются искажения кристаллической решётки Ме .Структура и свойства упрочненного Ме при возврате изменяются не значительно .Поцес рекрестализации протекает при Т >0.4 t плавления Ме и состоит из 2-х процессов :первичный и вторичный (собирательной ).при первичной крестализации в результате нагрева упрочненного Ме происходит зарождение и рост мелких ровноостных зерен замен старых деформированных.
Вторичная рекристаллизация состоит в обьединении мелких ровноостных зерен полученных при первой рекристаллизации в более крупные. 2-я рекристаллизация нежелательна так как Ме с крупным зерном хрупок и плохо обрабатывается режущим инструментом .если необходимо быстро снять упрочнение Ме и искажение его кристаллической решетки назначают терм. Обр.- рекристаллизационный отжиг где t отжига >t рекристаллизации
№18 ДИАГРАММА СОСТОЯНИЯ Fe-C.
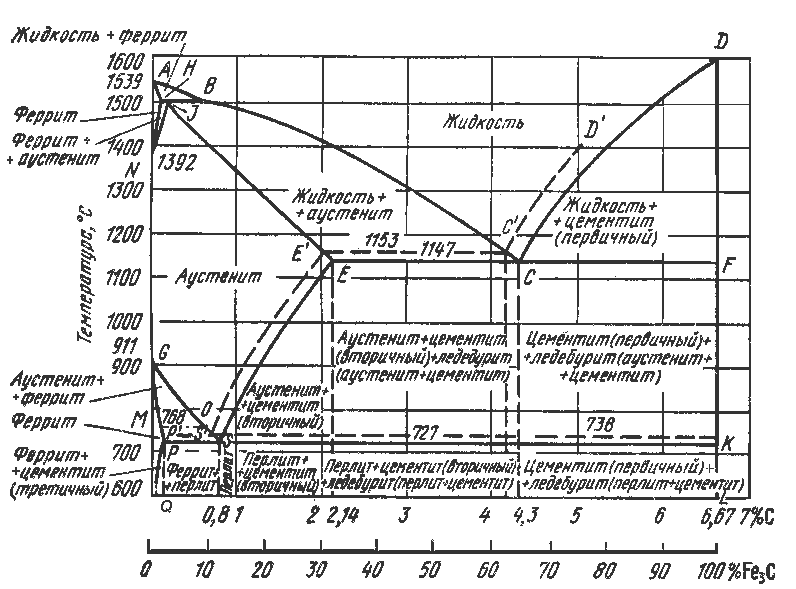
Равновесное состояние железоуглеродистых сплавов в зависимости от содержания углерода и температуры описывает диаграмма состояния железо - углерод. На диаграмме состояния железоуглеродистых сплавов (рис. 1) на оси ординат отложена температура, на оси абсцисс - содержание в сплавах углерода до 6,67%, то есть до такого количества, при котором образуется цементит Fе3С. По диаграмме состояния системы железо - углерод судят о структуре медленно охлажденных сплавов, а также о возможности изменения их микроструктуры в результате термической обработки, определяющей эксплуатационные свойства.