Материал: Расчет процесса горения топлива и установки для его сжигания
Расчет процесса горения топлива и установки для его сжигания
Министерство образования и науки Российской Федерации
ИРКУТСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
Кафедра
металлургии цветных металлов
Курсовая работа
Расчет
процесса горения топлива и установки для его сжигания
Выполнил
Бубникович А.С.
Иркутск, 2014 г.
Содержание
Введение
. Классификация металлургических печей
.1 Классификация печей по принципу теплогенерации
.2 Классификация печей по технологическому назначению и по режиму работы
.3 Характеристика вращающихся печей
.4 Барабанно-вращающие печи
.5 Тепловая работа вращающихся печей
. Расчет горения топлива
.1 Задание
.2 Расчет горения топлива
. Итоговая таблица. Характеристика различных условий процесса горения топлива
Заключение
Список используемой литературы
Введение
Топливо - вещество <#"793154.files/image001.gif">
Рис. 1. Барабанная вращающая печь: 1- железный
барабан, 2- холодный конец, 3 - горячий конец, 4 - ролики, 5 - бандажи, 6 -
подшипники, 7 - приспособление, препятствующее сходу барабана с опор, 8 -
двигатель, 9 - венцовая шестерня, 10 - топливная головка. 11 - кольцо с
кромкой, 12 - загрузочная коробка, 13 - отбойное приспособление (стальная
болванка)
.5 Тепловая работа вращающихся печей
Тепловая работа любой печи характеризуется рядом показателей, важнейшими из которых являются тепловой и температурный режимы, производительность печи, удельный расход топлива и коэффициент полезного действия. Тепловой режим характеризует изменение во времени тепловой нагрузки, т.е. количества теплоты, подаваемой в печь в каждый момент времени, а температурный режим представляет собой изменение температуры печи во времени или по длине печи.
В рабочем пространстве вращающейся печи протекают процессы выделения теплоты при сжигании топлива, движения газовой среды и материала, внешнего и внутреннего теплообмена. Эффективность тепловой работы печи зависит от того, насколько совершенно осуществляются в ней эти процессы. От организации тепловой работы вращающихся печей зависят не только производительность и экономичность процесса производства глинозема, но и срок службы печи и качество конечного продукта. Процесс спекания осуществляют при достаточно высоких температурах. По мере изменения температуры по длине рабочего пространства вращающихся печей происходят процессы с образованием различных неустойчивых соединений.
В пламенных печах одним из основных и наиболее эффективных способов улучшения их тепловой работы является интенсификация теплообменных процессов за счет совершенствования процессов горения. Рациональное сжигание топлива позволяет создать в рабочем пространстве вращающихся печей необходимые температурный и газовый режимы, предусмотренные технологией глиноземного производства.
При нагреве сыпучих материалов во вращающихся печах теплота поступает в зону технологического процесса за счет одновременного протекания всех трех видов теплообмена. На участках, где температура продуктов сгорания достигает 1200-1600 °С, осуществляется радиационный режим работы печи. По мере продвижения продуктов сгорания топлива по длине печи они охлаждаются до нескольких сот °С и режим тепловой работы печи постепенно становится конвективным. Конкретное распределение в печи зон с конвективным и радиационным режимами работы зависит от вида и параметров технологического процессов. С точки зрения внешнего (по отношению к нагреваемому материалу) теплообмена вращающаяся печи может быть условно разделена на энергетически однородные участки - тепловые зоны, в пределах которых температуру, радиационные характеристики и коэффициент теплоотдачи от газов к материалу можно считать постоянными величинами. Кроме того, в рабочем пространстве происходит и так называемый внутренний теплообмен: поступившая в слой материала теплота распределяется в нем путем теплопроводности. При вращении барабана печи происходит энергичное перемешивание сыпучего материала, температура по высоте слоя практически выравнивается и его можно считать тонким в тепловом отношении телом, нагрев которого может сопровождаться эндо- и экзотермическими реакциями. Перенос теплоты в кладке печи происходит также вследствие теплопроводности. Изменение температуры внутренней поверхности футеровки во времени носит циклический характер. Время цикла равно времени полного оборота печи. Условно его делят на два периода. В первом периоде поверхность кладки находится в контакте с греющими газами и постепенно нагревается, получая от нее теплоту излучением и конвекцией. Ко второму периоду относят время ее контакта с нагреваемым материалом, в течение которого температура поверхности кладки снижается. Анализ данных расчета поля температур кладки, полученных при решении уравнения теплопроводности с использованием численных методов, показал, что колебания температуры во времени происходят на определенном расстоянии от поверхности футеровки, получившим название глубины проникновения тепловой волны. Колебания температуры, достигающие на внутренней поверхности барабана при входе и выходе ее из-под слоя шихты нескольких сотен градусов, распространяются на глубину 1-5 см, чем ближе к поверхности, тем выше термические напряжения, возникающие в кладке, и тем больше вероятность ее разрушения.
Температурный режим работы вращающихся печей не изменяется во времени, индивидуален для каждого вида технологического процесса и в значительной мере определяется химическим и фракционным составом перерабатываемых материалов. Обычно его устанавливают опытным путем и организуют таким образом, чтобы в печи строго соблюдался график нагрева шихты, соответствующий технологии данного процесса.
Рассмотрим температурный режим процесса. Все рабочее пространство вращающейся печи можно условно разделить на четыре зоны, в которых происходят определенные изменения обрабатываемой шихты.
Первая зона, которую называют зоной сушки и обезвоживания, находится в верхней части печи со стороны загрузки шихты. Вначале из шихты испаряется внешняя влага, и температура материала при этом остается практически неизменной близкой к 100 °С. Затем температура высушенной шихты возрастает до 600 °С. Движущиеся навстречу ей газы охлаждаются от 1100 до 240 °С.
Во второй зоне, температура шихты продолжает расти и достигает 1000 °С. В этой зоне происходит полное разложение веществ, требующее затрат теплоты, поэтому температура газов снижается с 1300 до 1100 °С.
Третья зона - зона спекания - характеризуется максимальными значениями температур как шихты (1000-1200 °С), так и газов (1350-1450 °С), так как именно здесь происходит горение.
Четвертая зона - зона охлаждения - располагается за срезом заглубленного в печь топливо сжигающего устройства. Благодаря потоку идущего из холодильника воздуха, имеющего температуру 150-300 °С, обеспечивается охлаждение спека до температуры 1000 °С, что резко увеличивает его механическую прочность (по сравнению с размягченным состоянием), необходимую для перегрузки в расположенный в низу холодильник.
Нужно учитывать, что качество готового продукта, получаемого во вращающихся печах, определяется не только кинетикой, но и движением материала, т.е. временем его пребывания в печи. В зависимости от того, насколько мгновенные скорости отдельных частиц отличаются от средней скорости движения материала. Наличие в печи частиц с различными скоростями движения и неопределенность соотношения таких частиц из-за технологических возмущений, нарушающий установившийся режим, затрудняют надежный контроль и регулирование тепловой работы печей. В то же время одной из главных задач оперативного управления является поддержание всех параметров на заданном уровне, что возможно только при своевременной и непрерывной информации о качестве целевого продукта.
Основное назначение металлургической печи
состоит в том, чтобы создать в рабочем пространстве, изолированном от
окружающей среды, наиболее благоприятные условия для реализации
соответствующего технологического процесса.
2. Расчет горения топлива
.1 Задание
Рассчитать процесс горения топлива, заданного состава на воздухе. Состав воздуха: 21 об. % О2и 79 об. % N2. Коэффициент избытка воздуха α = 1. Состав топлива: Сг = 90,0%; Нг = 4,2%; Nг = 1,5 %; Ог= 2,1%; Sг = 2,2%; Ас = 12,0%; Wр = 3,0%.
Рассчитать процесс сжигания топлива заданного состава на воздухе. Состав воздуха: 30 об. % О2и 70 об. % N2. Коэффициент избытка воздуха α = 1.
Рассчитать количество кислорода воздуха, продукт полного сгорания топлива. Определить теплотворную способность топлива, калориметрическую и действительную температуру процессов сгорания.
Рассчитать процесс горения топлива на воздухе, обогащённом кислородом. Состав воздуха: 100 об.% О2. Коэффициент избытка воздуха α = 1.
Рассчитать процесс сгорания топлива в обогащённом кислородом воздухе. Состав воздуха: 21 об.% О2 и 79 об.% N2. Коэффициент избытка воздуха α = 1,3.
Рассчитать количество кислорода воздуха, продукт полного сгорания топлива, определить калориметрическую и действительную температуру полного сгорания.
Рассчитать процесс горения топлива в атмосфере чистого кислорода.
Состав воздуха: 30 об.% О2и 79 об.% N2. Коэффициент избытка воздуха α = 1.3.
Рассчитать процесс горения топлива заданного состава в атмосфере чистого кислорода. Состав воздуха: 100 об.% О2. Коэффициент избытка воздуха α = 1,3.
Рассчитать количество кислорода воздуха, продукт полного сгорания топлива, определить калориметрическую и действительную температуру полного сгорания.
Сопоставить результаты расчета.
.2 Расчет горения топлива
Перевод состава топлива на рабочую массу (масс.
%):
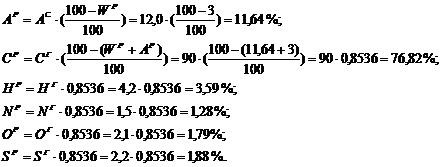
Проверка:
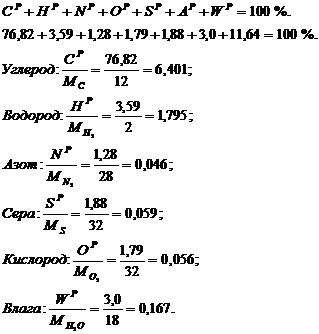
Мольные объёмы O2на 100 кг топлива
заданного состава.
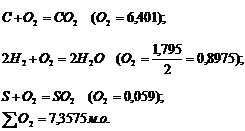
Расход кислорода на горение топлива заданного состава
Так как в топливе уже имеется 0,056 мольных объёмов O2 → из воздуха нужно добавить 7,3575 - 0,056 =7,3015 мольных объёмов.
Определение теплоты сгорания топлива
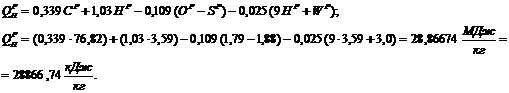
Расчет процесса горения топлива при составе
воздуха:- 21 об.%; N2- 79 об.%; α = 1.из
воздуха:
![]() мольных объемов.
мольных объемов.
Общее количество воздуха,
поступившее в топку при сжигании 100 кг топлива заданного состава:
![]() мольных объемов.
мольных объемов.
Количество воздуха необходимое на сгорание 1 кг (удельный расход):
Т - теоретическая (когда все идет по стехиометрическим коэффициентам);
д - действительный удельный расход.
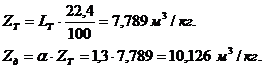
Определение состава и количества
продуктов горения при теоретическом расходе топлива (табл. 1)
Таблица 1 - Состав и количество
продуктов горения (O2 - 21 об. %;
N2 - 79 об. %;
α
= 1)
Вещество
Мольные
объемы
Молекулярный
вес
m, кг
Масс.
%
Об.
%
CO2
6,401
44
281,644
25,81
17,81
H2O
1,795+0,167=
= 1,962
18
35,316
3,24
5,46
SO2
0,059
64
3,776
0,35
0,16
N2возд
27,47+0,046
=27,516
28
770,448
70,60
76,57
Ʃ
35,938
1091,184
100
100
VГ - объем
газа = Vпр - продуктов
сгорания.
VГ = При сгорании 1 кг топлива заданного
состава образуется 8,050 м3 газа.
Таблица 2 - Балансовая таблица
сжигания топлива O2 - 21 об. %;
N2 - 79 об. %;α = 1
Приход
m, кг
Расход
m, кг
Топливо
100,0
Продукты
сгорания
Воздух
CO2
281,644
О2
= 7,3015 N2
= 27,47 Всего
1102,83
N2
770,448
АР
11,64
Всего
без АР
1091,184
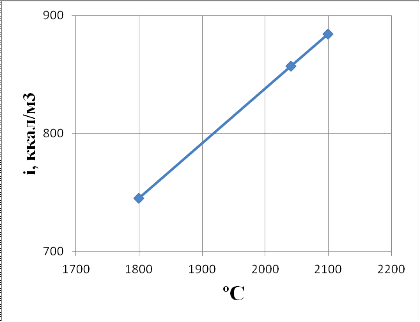
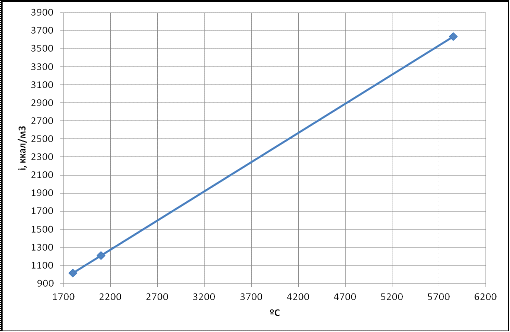
Определение калориметрической температуры
горения топлива в необогащенном воздухе
i0 - начальная
энтальпия.
m - масса
сгоревшего топлива.
Vпр. сг. - объем
продуктов сгорания, м3. Vпр. сг. = 8,050 м3/кг.
t1 = 1800 ℃
CO2 0,2581 H2O 0,0324 SO2 0,0035 N20,7060 N20,7060 Рисунок 2
Расчет процесса горения топлива при составе
воздуха: O2 - 30 об.%; N2- 70 об.%; α = 1.
N2
из воздуха:
Общее количество воздуха,
поступившее в топку при сжигании 100 кг топлива заданного состава:
Количество воздуха необходимое на
сгорание 1 кг ( удельный расход):
Определение состава и количества
продуктов горения при теоретическом расходе топлива (табл. 3)
Таблица 3 - Состав и количество
продуктов горения: (30 об.%; N2 - 70 об.%; α = 1)
Вещество
Мольные
объемы
Молекулярный
вес
m, кг
Масс.
%
Об.
%
CO2
6,401
44
281,644
35,25
25,10
H2O
1,962
18
35,316
4,42
7,69
SO2
0,059
64
3,776
0,47
0,23
N2возд
17,037+0,046
=17,083
28
478,324
59,86
66,98
Ʃ
25,505
799,060
100
100
VГ = Vпр. сг.
VГ = При сгорании 1 кг топлива заданного
состава образуется 5,71 м3 газа.
Таблица 4 - Балансовая таблица
сжигания топлива (O2 - 30 об. %;
N2 - 70 об. %;α = 1)
Приход
m, кг
Расход
m, кг
Топливо
100,0
Продукты
сгорания
Воздух
CO2
281,644
О2
= 7,3015 N2
= 17,037 Всего
810,688
N2
478,324
АР
11,640
Всего
без АР
799,060
Определение калориметрической температуры
горения топлива в обогащенном воздухе
i0 - начальная
энтальпия.
m - масса
сгоревшего топлива.
Vпр. сг. - объем
продуктов сгорания, м3. Vпр. сг. = 5,71 м3/кг.
t1 = 1800 ℃
CO20,3525 H2O 0,0442 SO2 0,0047 N20,5986 N20,5986 Рисунок 3
Расчет процесса сгорания топлива в атмосфере
чистого O2: O2 - 100 об.%; α = 1.
N2
из воздуха:
Общее количество воздуха поступившее
в топку при сжигании 100 кг топлива заданного состава:
Количество воздуха необходимое на
сгорание 1 кг ( удельный расход):
Определение состава и количества
продуктов горения при теоретическом расходе топлива (табл. 5)
Таблица 5 - Состав и количество
продуктов горения: O2 - 100 об.%; α = 1
Вещество
Мольные
объемы
Молекулярный
вес
m, кг
Масс.
%
Об.
%
CO2
6,401
44
281,644
87,46
75,59
H2O
1,962
18
35,316
10,97
23,17
SO2
0,059
64
3,776
1,17
0,70
N2 (в
топливе)
0,046
28
1,288
0,40
0,54
Ʃ
8,468
322,024
100
100
VГ = При сгорании 1 кг топлива заданного
состава образуется 1,897 м3 газа.
Таблица 6 - Балансовая таблица
сжигания топлива (O2 - 100 об.%; α = 1)
Приход
m, кг
Расход
m, кг
Топливо
100,0
Продукты
сгорания
Воздух
CO2
281,644
О2
= 7,3015 Всего
333,648
SO2
3,776
N2
1,288
АР
11,64
Всего
без АР
322,024
Определение калориметрической температуры
горения топлива
i0 - начальная
энтальпия.
m - масса
сгоревшего топлива.
Vпр. сг. - объем
продуктов сгорания, м3. Vпр. сг. = 1,897 м3/кг.
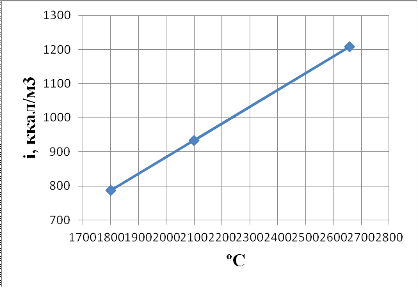
t1 = 1800 ℃
CO20,8746 H2O0,1097 SO2 0,0117 N20,0040 N20,0040 Рисунок 4
Расчет процесса горения топлива при составе
воздуха: O2 - 21 об. %; N2 - 79 об. %; α = 1,3.
N2
из воздуха:
Общее количество воздуха поступившее
в топку при сжигании 100 кг топлива заданного состава:
Количество воздуха необходимое на
сгорание 1 кг ( удельный расход):
д - действительный удельный расход.
Определение состава и количества
продуктов горения при действительном расходе топлива (табл. 7)
Таблица 7 - Состав и количество
продуктов горения: (O2 - 21 об.%; N2 - 79 об.%; α = 1,3)
Вещество
Мольные
объемы
Молекулярный
вес
m, кг
Масс.
%
Об.
%
CO2
6,401
44
281,644
27,82
19,51
H2O 18
35,316
3,49
5,98
SO2
0,059
64
3,776
0,37
0,18
N2возд
27,47 O2возд
2,190
32
70,08
6,93
6,68
Ʃ
46,369
1392,012
100
100
VГ = При сгорании 1 кг топлива заданного
состава образуется 7,35 м3 газа.
Таблица 8 - Балансовая таблица
сжигания топлива (O2 - 21 об. %;
N2 - 79 об. %;α = 1,3)
Приход
m, кг
Расход
m, кг
Топливо
100,0
Продукты
сгорания
Воздух
CO2
281,644
О2
= 7,3015 N2
= 27,17 Всего
1392,730
N2
1001,196
АР
11,64
O2
70,08
Всего
без АР
1392,724
Определение калориметрической температуры
горения топлива в необогащенном воздухе
i0 - начальная
энтальпия.
m - масса
сгоревшего топлива.
Vпр. сг. - объем
продуктов сгорания, м3. Vпр. сг. = 7,35 м3/кг.
t1
= 1800 ℃2
0,2782 N20,6139 O20,0693 N2 0,6139 O2 0,0693 Рисунок 5
Расчет процесса горения топлива при
составе воздуха: O2 - 30 об.%; N2 - 70 об.%; α = 1,3.
N2
из воздуха:
Общее количество воздуха поступившее
в топку при сжигании 100 кг топлива заданного состава:
Количество воздуха необходимое на
сгорание 1 кг ( удельный расход):
Определение состава и количества
продуктов горения при действительном расходе топлива (табл. 9)
Таблица 9 - Состав и количество
продуктов горения: O2 - 30 об.%; N2 - 70 об.%; α = 1,3
Вещество
Мольные
объемы
Молекулярный
вес
m, кг
Масс.
%
Об.
%
CO2
6,401
44
281,644
27,83
19,51
H2O
1,962
18
35,316
3,49
5,98
SO2
0,059
64
3,776
0,37
0,18
N2возд
17,037 O2возд
2,190
32
70,08
6,92
6,68
Ʃ
32,806
1012,248
100
100
VГ = При сгорании 1 кг топлива заданного
состава образуется 7,348 м3 газа.
Таблица 10 - Балансовая таблица
сжигания топлива (O2 - 30 об.%; N2 - 70 об.%;α = 1,3)
Приход
m, кг
Расход
m, кг
Топливо
100,0
Продукты
сгорания
Воздух
CO2
281,644
О2
= 7,3015 N2
= 17,037 Всего
1023,889
N2
621,432
АР
11,640
O2
70,080
Всего
без АР
1012,248
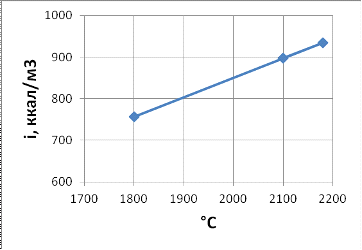
Определение калориметрической температуры
горения топлива в обогащенном воздухе
Vпр. сг. = 7,384 м3/кг.
t1 = 1800 ℃
CO20,2783 H2O 0,0349 SO2 0,0037 N20,6139 O20,0692 N20,6139 O20,0692 Рисунок 6
Расчет процесса сгорания топлива в
атмосфере чистого O2: O2 - 100 об.%; α = 1,3.из воздуха:
Общее количество воздуха поступившее
в топку при сжигании 100 кг топлива заданного состава:
Количество воздуха необходимое на
сгорание 1 кг ( удельный расход):
Определение состава и количества
продуктов горения при действительном расходе топлива (табл. 11)
Таблица 11 - Состав и количество
продуктов горения: (O2 - 100 об.%; α = 1,3)
Вещество
Мольные
объемы
Молекулярный
вес
m, кг
Масс.
%
Об.
%
CO2
6,401
44
281,644
71,83
60,06
H2O
1,962
18
35,316
9,01
18,41
SO2
0,059
64
3,776
0,96
0,55
N2 (в
топливе)
0,046
28
1,288
0,33
0,43
O2возд
2,190
32
70,08
17,87
20,55
Ʃ
10,658
392,104
100
100
VГ = При сгорании 1 кг топлива заданного
состава образуется 2,387 м3 газа.
Таблица 12 - Балансовая таблица
сжигания топлива (O2 - 100 об.
%; α=1)
Приход
m, кг
Расход
m, кг
Топливо
100,0
Продукты
сгорания
Воздух
CO2
281,644
О2
= 7,3015 Всего
403,742
SO2
3,776
N2
1,288
АР
11,640
O2
70,080
Всего
без АР
392,104
Определение калориметрической температуры
горения топлива в обогащенном воздухе
Vпр. сг. = 2,387 м3/кг.
t1 = 1800 ℃
CO2 0,7183 H2O 0,0901 SO2 0,0096 N20,0033 O20,1787 N20,0033 O20,1787 Рисунок 7
3. Итоговая таблица. Характеристика
различных условий процесса горения топлива
Все полученные результаты сгорания топлива при различных
условиях приведены в таблице 13.
Таблица 13. Характеристика различных условий
процесса горения топлива
Сравнительная
таблица
О2
= 21 об. %
О2
= 30 об. %
О2
= 100 об. %
α
=1
α
=1,3
α
=1
α
=1,3
α
=1
α
=1,3
Qрнизш.
28866,74(кДж
/ кг)
СО2,
кг
281,644
281,644
281,644
281,644
281,644
281,644
Н2О,
кг
35,316
35,316
35,316
35,316
35,316
35,316
SO2, кг
3,776
3,776
3,776
3,776
3,776
3,776
N2, кг
770,448
1001,196
478,324
621,432
1,288
1,288
О2,
кг
-
70,080
-
70,080
-
70,080
Vг,
м3/кг
8,050
7,350
5,710
7,348
1,897
2,387
tк,
°С
2041
2198
2658
2179
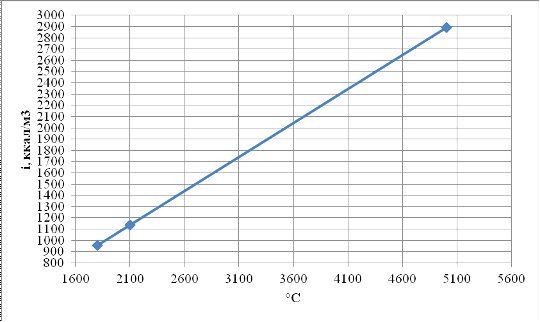
5849
5001
tд,
°С
1531
1648,5
1994
1634,25
4387
3750,75
Заключение
Целью данного расчета являлось определение
расхода воздуха, количества и состава продуктов горения, а также определение
калориметрической и действительной температуры горения при разных составах
воздуха и значений коэффициента избытка воздуха (α).
Результаты расчета показывают, что обогащение
воздуха, расходуемого на горение топлива, кислородом уменьшает расход воздуха,
количество продуктов сгорания, а следовательно, увеличивает калориметрическую
температуру горения. По расчетам мы видим, что увеличение величины коэффициента
избытка воздуха приводит к увеличению количества образующихся продуктов
сгорания, что снижает начальную энтальпию и калориметрическую температуру
горения.
Исходя из выше сказанного, наиболее
предпочтительным вариантом для нас является состав воздуха: O2
- 30 об.%; N2
- 70 об.%; коэффициент избытка воздуха α = 1,3. Существует
вероятность того, что из-за низкого коэффициента α в
процессе будет недостаточно кислорода, поэтому желательно установить α
= 1,3.
металлургический печь топливо
горение
Список используемой литературы:
1. Прибытков И.А. Теоретические
основы теплотехники: учеб. - М.; Академия, 2004. - 463 с.
. Клец В.Э., Немчинова Н.В.,
Кокорин В.С. Основы пирометаллургических производств: учеб. пособие - Иркутск:
Изд-во ИрГТУ, 2009. - 144 с.
. Самохвалов В.Г.
Металлургические электропечи: учеб. пособие. - М.: Теплотехник, 2009. - 304 с.
. Процессы и аппараты цветной
металлургии: учеб. для вузов / С.С. Набойченко, Н.Г. Агеев, А.П. Дорошкевич [и
др.], Екатеринбург, ГОУ ВПО УГТУ-УПИ, 2005. - 700 с.
. Кузьмина М.Ю. Теплотехника:
программа и метод. указания к выполнению курсового проекта - Иркутск: Изд-во
ИрГТУ, 2005. - 76 с.
![]()
![]() м3/кг.
м3/кг.
![]() 1 м3 газов имеет вес
1,355 кг.
1 м3 газов имеет вес
1,355 кг.
![]() 32
32![]() 1233,648H2O35,316
1233,648H2O35,316
![]() 28
28![]() 1769,16SO23,776
1769,16SO23,776
![]()
![]() = 28866,74кДж/кг.
= 28866,74кДж/кг.
![]()
![]() 1041,48 = 268,806ккал/м3;
1041,48 = 268,806ккал/м3;
![]() 819,18 =26,541ккал/м3;
819,18 =26,541ккал/м3;
![]() 1000,80 = 3,503ккал/м3;
1000,80 = 3,503ккал/м3;
![]() 632,16 =446,305ккал/м3;
632,16 =446,305ккал/м3;
![]() 2
= 2100 ℃20,2581
2
= 2100 ℃20,2581![]() 1238,79 =
319,732ккал/м3;2O0,0324
1238,79 =
319,732ккал/м3;2O0,0324![]() 984,68 =
31,903ккал/м3;20,0035
984,68 =
31,903ккал/м3;20,0035![]() 1265,00 =4,427ккал/м3;
1265,00 =4,427ккал/м3;
![]() 748,02 =528,102ккал/м3;
748,02 =528,102ккал/м3;
![]()
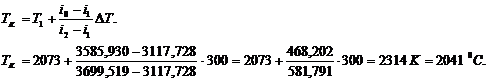
![]() мольных объемов.
мольных объемов.
![]() мольных объемов.
мольных объемов.
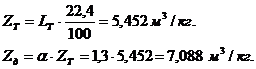
![]()
![]() м3/кг.
м3/кг.
![]() 1 м3 газов имеет вес
1,399 кг.
1 м3 газов имеет вес
1,399 кг.
![]() 32
32![]() 1233,648H2O35,316
1233,648H2O35,316
![]() 28
28![]() 1477,04SO23,776
1477,04SO23,776
![]()
![]() = 28866,74 кДж/кг.
= 28866,74 кДж/кг.
![]()
![]() 1041,48 = 367,122ккал/м3;
1041,48 = 367,122ккал/м3;
![]() 819,18 = 36,208ккал/м3;
819,18 = 36,208ккал/м3;
![]() 1000,80 = 4,704ккал/м3;
1000,80 = 4,704ккал/м3;
![]() 632,16 = 378,411ккал/м3;
632,16 = 378,411ккал/м3;
![]() 2
= 2100 ℃20,3525
2
= 2100 ℃20,3525![]() 1238,79 =
436,673ккал/м3;2O0,0442
1238,79 =
436,673ккал/м3;2O0,0442![]() 984,68
=43,523ккал/м3;20,0047
984,68
=43,523ккал/м3;20,0047![]() 1265,00 = 5,946ккал/м3;
1265,00 = 5,946ккал/м3;
![]() 748,02 =447,765ккал/м3;
748,02 =447,765ккал/м3;
![]()
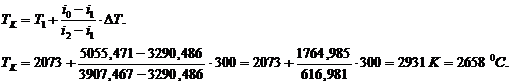
![]()
![]() мольных объемов.
мольных объемов.
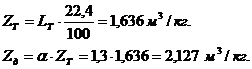
![]()
![]() м3/кг.
м3/кг.
![]() 1 м3 газов имеет вес
1,697 кг.
1 м3 газов имеет вес
1,697 кг.
![]() 32
32![]() 1233,648H2O35,316
1233,648H2O35,316
![]()
![]() = 28866,74 кДж/кг.
= 28866,74 кДж/кг.
![]()
![]() 1041,48 = 910,878ккал/м3;
1041,48 = 910,878ккал/м3;
![]() 819,18 = 89,864ккал/м3;
819,18 = 89,864ккал/м3;
![]() 1000,80 = 11,709ккал/м3;
1000,80 = 11,709ккал/м3;
![]() 632,16 = 2,529ккал/м3;
632,16 = 2,529ккал/м3;
![]() 2
= 2100 ℃20,8746
2
= 2100 ℃20,8746![]() 1238,79 =
1083,446ккал/м3;2O0,1097
1238,79 =
1083,446ккал/м3;2O0,1097![]() 984,68 =
108,019ккал/м3;20,0117
984,68 =
108,019ккал/м3;20,0117![]() 1265,00 =14,801ккал/м3;
1265,00 =14,801ккал/м3;
![]() 748,02 =2,992 ккал/м3;
748,02 =2,992 ккал/м3;
![]()
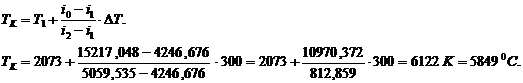
![]() мольных объемов.
мольных объемов.
![]() мольных объемов.
мольных объемов.
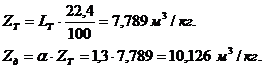
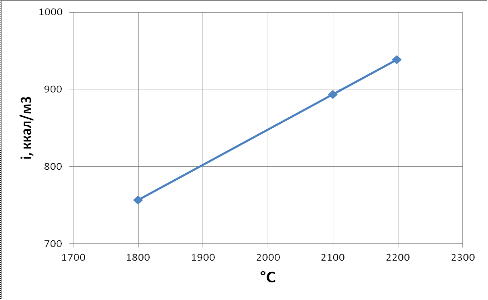
![]() 1,3+0,046
=35,757281001,19661,3967,65
1,3+0,046
=35,757281001,19661,3967,65
![]()
![]() м3/кг.
м3/кг.
![]() 1 м3 газов имеет вес
1,377 кг.
1 м3 газов имеет вес
1,377 кг.
![]() 32
32![]() 1,3303,742H2O35,316
1,3303,742H2O35,316
![]() 28
28![]() 1,3988,988SO23,776
1,3988,988SO23,776
![]()
![]() = 28866,74 кДж/кг.
= 28866,74 кДж/кг.
![]()
![]() 1041,48 =
289,740ккал/м3;2O
0,0349
1041,48 =
289,740ккал/м3;2O
0,0349![]() 819,18 =
28,589ккал/м3;2 0,0037
819,18 =
28,589ккал/м3;2 0,0037![]() 1000,80 = 3,703ккал/м3;
1000,80 = 3,703ккал/м3;
![]() 632,16 = 388,083ккал/м3;
632,16 = 388,083ккал/м3;
![]() 668,88 = 46,353ккал/м3;
668,88 = 46,353ккал/м3;
![]() 2
= 2100 ℃2
0,2782
2
= 2100 ℃2
0,2782![]() 1238,79 =
344,631ккал/м3;2O
0,0349
1238,79 =
344,631ккал/м3;2O
0,0349![]() 984,68 =
34,365ккал/м3;2 0,0037
984,68 =
34,365ккал/м3;2 0,0037![]() 1265,00 = 4,681ккал/м3;
1265,00 = 4,681ккал/м3;
![]() 748,02 = 459,209ккал/м3;
748,02 = 459,209ккал/м3;
![]() 791,7 = 50,590ккал/м3;
791,7 = 50,590ккал/м3;
![]()
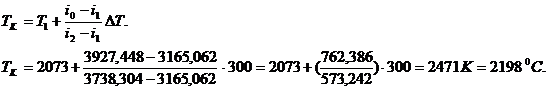
![]() мольных объемов.
мольных объемов.
![]() мольных объемов.
мольных объемов.
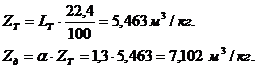
![]() 1,3+0,046
=22,19428621,43261,3967,65
1,3+0,046
=22,19428621,43261,3967,65
![]()
![]() м3/кг.
м3/кг.
![]() 1 м3 газов имеет вес
1,336 кг.
1 м3 газов имеет вес
1,336 кг.
![]() 32
32![]() 1,3303,742H2O35,316
1,3303,742H2O35,316
![]() 28
28![]() 1,3620,147SO23,776
1,3620,147SO23,776
![]()
![]() = 28866,74 кДж/кг.
= 28866,74 кДж/кг.
![]()
![]() 1041,48 = 289,844ккал/м3;
1041,48 = 289,844ккал/м3;
![]() 819,18 = 28,589ккал/м3;
819,18 = 28,589ккал/м3;
![]() 1000,80 = 3,703ккал/м3;
1000,80 = 3,703ккал/м3;
![]() 632,16 = 388,083ккал/м3;
632,16 = 388,083ккал/м3;
![]() 668,88 = 46,286ккал/м3;
668,88 = 46,286ккал/м3;
![]() 2
= 2100 ℃20,2783
2
= 2100 ℃20,2783![]() 1238,79 =
292,231ккал/м3;2O0,0349
1238,79 =
292,231ккал/м3;2O0,0349![]() 984,68 =
58,884ккал/м3;20,0037
984,68 =
58,884ккал/м3;20,0037![]() 1265,00 = 1,139ккал/м3;
1265,00 = 1,139ккал/м3;
![]() 748,02 = 452,402ккал/м3;
748,02 = 452,402ккал/м3;
![]() 791,7 = 78,062ккал/м3;
791,7 = 78,062ккал/м3;
![]()
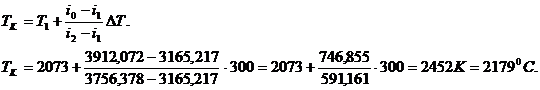
![]()
![]() мольных объемов.
мольных объемов.
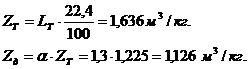
![]()
![]() м3/кг.
м3/кг.
![]() 1 м3 газов имеет вес
1,643 кг.
1 м3 газов имеет вес
1,643 кг.
![]() 32
32![]() 1,3303,742H2O35,316
1,3303,742H2O35,316
![]()
![]() = 28866,74 кДж/кг.
= 28866,74 кДж/кг.
![]()
![]() 1041,48 = 748,095ккал/м3;
1041,48 = 748,095ккал/м3;
![]() 819,18 = 73,808ккал/м3;
819,18 = 73,808ккал/м3;
![]() 1000,80 = 9,608ккал/м3;
1000,80 = 9,608ккал/м3;
![]() 632,16 = 2,086ккал/м3;
632,16 = 2,086ккал/м3;
![]() 668,88 = 119,529ккал/м3;
668,88 = 119,529ккал/м3;
![]() 2
= 2100 ℃20,7183
2
= 2100 ℃20,7183![]() 1238,79 =
889,823ккал/м3;2O0,0901
1238,79 =
889,823ккал/м3;2O0,0901![]() 984,68 =
88,720ккал/м3;20,0096
984,68 =
88,720ккал/м3;20,0096![]() 1265,00 =12,144ккал/м3;
1265,00 =12,144ккал/м3;
![]() 748,02 =2,468ккал/м3;
748,02 =2,468ккал/м3;
![]() 791,70 = 141,427ккал/м3;
791,70 = 141,427ккал/м3;
![]()
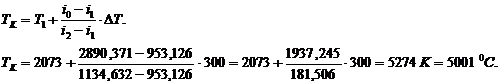
![]()
![]() , кг/м31,3551,3771,3991,3361,6971,643
, кг/м31,3551,3771,3991,3361,6971,643