Материал: promiwteh
Отечественная промышленность выпускает два вида нитрагина: почвенный и сухой. Впервые культура клубеньковых бактерий на почвенном субстрате была приготовлена в 1911 году на бактериально-агрономической станции в Москве. В настоящее время его производство имеет ограниченное значение, так как технология довольно сложна и трудоёмка при выполнении отдельных операций. Более перспективна технология производства сухого нитрагина.
Сухой нитрагин - порошок светло-серого цвета, содержащий в 1 г не менее 9 млрд. жизнеспособных бактерий в смеси с наполнителем. Влажность не превышает 5-7%. Промышленное производство имеет типичную схему. Необходимо отметить, что важно подбирать штаммы, устойчивые к высушиванию. Для производства посевного материала исходную культуру клубеньковых бактерий выращивают на агаризованной среде, содержащей отвар бобовых семян, 2% агара и 1% сахарозы, затем культуру размножают в колбах на жидкой питательной среде в течение 1-2 суток при 28-30оС и рН 6.5-7.5. На всех этапах промышленного культивирования применяют питательную среду, включающую такие компоненты, как меласса, кукурузный экстракт, минеральные соли в виде сульфатов аммония и магния, мел, хлорид натрия и двузамещенный фосфат калия. Основная ферментация идет при тех же условиях в течение 2-3 суток. Готовую культуральную жидкость сепарируют, получается биомасса в виде пасты с влажностью 70-80%. Пасту смешивают с защитной средой, содержащей тиомочевину и мелассу (1:20) и направляют на высушивание. Сушат путем сублимации ( в вакуум-сушильных шкафах). Высушенную биомассу размалывают. Производительнее высушивание в распылительных сушках, но при этом 75% клеток теряют жизнеспособность. Препараты сухого нитрагина фасуют и герметизируют в полиэтиленовые пакеты по 0.2 - 1 кг, хранят при температуре 15оС не более 6 месяцев. Семена опудривают перед посевом. Внесение нитрагина повышает урожайность в среднем на 15-25%.
Препарат клубеньковых бактерий может выпускаться и в виде ризоторфина. Впервые торфяной препарат клубеньковых бактерий был приготовлен в 30-х годах, но технология была создана в 1973-77 гг. Для приготовления ризоторфина торф сушат при температуре не выше 100оС и размалывают в порошок. Наиболее эффективным способом стерилизации является облучение его гамма-лучами. Перед стерилизацией размолотый, нейтрализованный мелом и увлажненный до 30-40% торф расфасовывают в полиэтиленовые пакеты. Затем его облучают и заражают клубеньковыми бактериями, используя шприц, с помощью которого впрыскивается питательная среда, содержащая клубеньковые бактерии. Прокол после внесения бактерий заклеивается липкой лентой. Каждый грамм ризоторфина должен содержать не менее 2.5 млрд. жизнеспособных клеток с высокой конкурентоспособностью и интенсивной азотфиксацией. Препарат хранят при температуре 5-6оС и влажности воздуха 40-55%. Пакеты могут быть весом от 0.2 до 1.0 кг. Доза препарата составляет 200 г на га. Заражение семян производят следующем образом: ризоторфин разбавляют водой и процеживают через двойной слой марли. Полученной суспензией обрабатывают семена. Семена высевают в день обработки или на следующий.
Обработка семян бобовых культур прочно вошла в мировую сельскохозяйственную практику. Крупнейшими производителями таких препаратов являются США и Австралия.
Бактериальные удобрения. Технология получения фосфобактерина
Фосфобактерин - бактериальное удобрение, содержащее споры микроорганизма Bacillus megaterium var. phosphaticum. Представляет собой порошок светло-серого или желтоватого цвета.
Бактерии обладают способностью превращать сложные фосфорорганические соединения (нуклеиновые кислоты, нуклеопротеиды и т.д.) и трудноусвояемые минеральные фосфаты в доступную для растений форму. Кроме этого бактерии вырабатывают биологически активные вещества (тиамин, пиридоксин, биотин, пантотеновую и никотиновую кислоты и др.), стимулирующие рост растения. Фосфобактерин относится к числу препаратов со стимулирующим эффектом.
Bacillus megaterium var. phosphaticum представляют собой мелкие, грамположительные аэробные спорообразующие палочки размером 2*6 мкм. Клетки содержат значительное количество соединений фосфора. В ранней стадии развития это подвижные одиночные палочки, при старении образуют эндоспоры, локализующиеся в одном из концов клетки. В силу вышеизложенного технология выращивания сводится к получению спор.
В целом производство фосфобактерина похоже на производство азотобактерина и препаратов клубеньковых бактерий. Состав питательной среды в процентах: кукурузный экстракт -1.8, меласса - 1.5, сульфат аммония - 0.1, мел - 1, остальное - вода. Культивирование ведется глубинным методом в строго асептических условиях при постоянном перемешивании и принудительной аэрации до стадии образования спор. Основные параметры проведения процесса: температура 28-30оС, рН 6.5-7.5, длительность культивирования 1.5-2 суток.
Полученную в ходе культивирования биомассу клеток отделяют центрифугированием и высушивают в распылительной сушилке при температуре 65-75оС до остаточной влажности 2-3%. Высушенные споры смешивают с наполнителем. Готовый препарат должен содержать не менее 8 млрд. клеток в 1 г. Расфасовывают препарат в полиэтиленовые пакеты по 50-500 г. В отличие от нитрагина и азотобактерина фосфобактерин обладает большей устойчивостью при хранении.
Фосфобактерин рекомендуют применять на черноземных почвах, которые содержат наиболее значительное количество фосфороорганических соединений. Необходим для повышения урожайности зерновых, картофеля, сахарной свеклы и др. сельскохозяйственных растений. Семена обрабатывают смесью сухого фосфобактерина с наполнителем (золой, почвой и др.) в соотношении 1:40. На 1 гектарную порцию требуется 5 г препарата и 200 г наполнителя. Клубни картофеля равномерно увлажняют суспензией спор, приготовленной из расчета 15 г препарата на 15 л воды. Урожай при этом повышается на 10%.
Антибиотики для сельского хозяйства
Антибиотики применяют в нескольких целях:
- для борьбы с болезнями животных;
- для борьбы с болезнями растений;
- как стимуляторы роста животных;
- при консервировании продуктов;
- в научных исследованиях (в области биохимии, молекулярной биологии, генетике, онкологии).
Современное определение термина "антибиотик" принадлежит М.М.Шемякину и А.С.Хохлову (1961), которые предложили считать антибиотическими веществами все продукты обмена любых организмов, способные избирательно убивать или подавлять рост и развитие микроорганизмов.
Полная химическая структура установлена только для трети антибиотиков, а может быть получена химическим путем лишь половина из них. Синтез микроорганизмами антибиотиков - одна из форм проявления антагонизма, связан с определенным характером обмена веществ, возникшим и закрепленным в ходе эволюции. Воздействуя на постороннюю микробную клетку, антибиотик вызывает нарушения в её развитии. Некоторые антибиотики способны подавлять синтез оболочки бактериальной клетки в период размножения, другие изменяют проницаемость цитоплазматической мембраны, некоторые ингибируют реакции обмена веществ. Механизм действия антибиотиков выявлен не полностью.
В течение многих лет антибиотики используют как стимуляторы роста сельскохозяйственных животных и птицы, как средства борьбы с заболеваниями растений и посторонней микрофлорой в ряде бродильных производств, как консерванты пищевых продуктов. Механизм стимулирующего действия антибиотиков также не до конца выяснен. Предполагают, что стимулирующий эффект низких концентраций антибиотиков на организм животного связан с двумя факторами:
Бактериальные удобрения. Технология получения азотобактерина
Азотобактерин - бактериальное удобрение, содержащее свободноживущий почвенный микроорганизм Azotobacter chroococcum, способный фиксировать до 20 мг атмосферного азота на 1 г использованного сахара. Внесенные в качестве удобрения в почву бактерии также выделяют биологически активные вещества (никотиновую и пантотеновую кислоты, пиридоксин, биотин, гетероауксин, гиббереллин и др.). Эти вещества стимулируют рост растений. Кроме того, продуцируемые Azotobacter фунгицидные вещества из группы анисомицина угнетают развитие некоторых нежелательных микроскопических грибов в ризосфере растения.
Все виды Azotobacter строгие аэробы. Чувствительны к содержанию в среде фосфора и развиваются лишь при высоком его содержании в питательной среде. Азотфиксирующая способность культуры подавляется аммиаком (вообще содержание в среде связанного азота угнетает азотфиксацию). Стимулируют процесс фиксации азота соединения молибдена.
Установлено, что при фиксации азота процесс его восстановления протекает на одном и том же синтезируемом азотобактером ферментном комплексе и лишь конечный продукт (аммиак) отделяется от фермента. Нитрогеназная азотфиксирующая система представляет собой мультиферментный комплекс, содержащий не связанное с геном железо, молибден и SH-группы.
Микробиологическая промышленность выпускает несколько видов азотобактерина: сухой, почвенный и торфяной. Технология получения сухого азотобактерина имеет много общего с технологией производства сухого нитрагина. Сухой азотобактерин - активная культура высушенных клеток азотобактера с наполнителем. В 1 г препарата содержится не менее 0.5 млрд. жизнеспособных клеток. Культуру микроорганизма выращивают методом глубинного культивирования на среде, содержащей те же компоненты, что и при культивировании клеток Rhizobium. Дополнительно вводят только сульфаты железа и марганца, а также сложную соль молибденовой кислоты, рН 5.7-6.5.
Процесс ферментации проводят до стационарной фазы развития культуры, так как в этой фазе биологически активные вещества выделяются из клетки и остаются в культуральной жидкости. Биологически активные вещества могут также полностью или частично теряться при высушивании, однако жизнеспособные клетки быстро восстанавливают способность их продуцировать. Высушенную культуру стандартизируют, фасуют в полиэтиленовые пакеты по 0.4-2 кг и хранят при температуре 15оС не более 3 месяцев.
Почвенный и торфяной азотобактерин представляют собой активную культуру азотобактера, размноженную на твердой питательной среде, и содержат в 1 г не менее 50 млн. жизнеспособных клеток. Для их приготовления берут плодородную почву или разлагающийся торф с нейтральной реакцией среды. К просеянному субстрату добавляют 2% извести и 0.1% суперфосфата. По 500 г полученной смеси переносят в бутыли емкостью по 0.5 л, увлажняют на 40-60% по объему водой, закрывают ватными пробками и стерилизуют. Посевной материал готовят на агаровых средах, содержащих 2% сахарозы и минеральные соли. Когда агар полностью покрывается слизистой массой коричневого цвета, полученный материал стерильно смывается дистиллированной водой и переносится на приготовленный субстрат. Содержимое бутылок тщательно перемешивают и термостатируют при 25-27оС. Культивирование продолжают до тех пор, пока бактерии не размножатся до необходимого количества. Полученный препарат сохраняет свою активность в течение 2-3 месяцев.
Использовать азотобактерин рекомендуется только на почвах, содержащих фосфор и микроэлементы. Азотобактерин применяют для бактеризации семян, рассады, компостов. При этом урожайность увеличивается на 10-15%. Семена зерновых опудривают сухим азотобактерином из расчета 100 млрд. клеток на 1 гектарную порцию семян. Картофель и корневую систему рассады равномерно смачивают водной суспензией бактерий. Для получения суспензии 1 гектарную норму (300 млрд. клеток) разводят в 15 литрах воды. При обработке почвенным или торфяным азотобактерином семена перемешивают с увлажненным препаратом и для равномерного высева подсушивают. Корневую систему рассады смачивают приготовленной суспензией.
- воздействие на микрофлору кишечника ,
- непосредственное влияние на организм животного.
В первом случае антибиотики снижают число вредных и увеличивают количество полезных для организма микроорганизмов. Во втором случае - снижают рН содержимого кишечника, уменьшают поверхностное натяжение клеток организма, что способствует ускорению их деления. Кроме того, антибиотики увеличивают количество ростовых гормонов, приспособляемость организма к неблагоприятным условиям и т.д. Кормовые антибиотики применяют в виде неочищенных препаратов, представляющих собой высушенную массу продуцента, содержащую помимо антибиотика аминокислоты, ферменты, витамина группы В и другие биологически активные вещества.
Все производимые кормовые антибиотики: а) не используются в терапевтических целях и не вызывают перекрестной резистентности бактерий к антибиотикам, применяемым в медицина; б) практически не всасываются в кровь из пищеварительного тракта; в) не меняют своей структуры в организме; г) не обладают антигенной природой, способствующей возникновению аллергии.
В настоящее время выпускаются несколько видов кормовых антибиотиков: препараты на основе хлортетрациклина (биовит, кормовой биомицин), бацитрацин, гризин, гигромицин Б и др. Из этих препаратов только бацитрацин представляет собой высушенную культуральную жидкость, полученную в результате глубинного выращивания Bacilus licheniformis. Остальные антибиотики являются продуктами жизнедеятельности разных видов Actinomyces.
Антибиотики используют и как средство борьбы с различными фитопатогенами. Воздействие антибиотика сводится к замедлению роста и гибели фитопатогенных микроорганизмов, содержащихся в семенах и вегетативных органах растений. К таким антибиотикам относятся фитобактериомицин, трихотецин, полимицин.
Применение антибиотиков в пищевой промышленности позволяет снизить длительность термообработки продуктов питания при их консервировании. Используемые антибиотики воздействуют на клостридиальные и термофильные бактерии, устойчивые к нагреванию. Наиболее эффективным признан низин, который практически не токсичен для человека и позволяет вдвое снизить время термообработки.
В заключение хотелось бы отметить, что в настоящем пособии не рассмотрены промышленные производства всех веществ, получаемых с помощью биотехнологии. Однако получить представление об основных принципах организации и осуществления биотехнологических процессов при производстве первичных и вторичных метаболитов, а также жизнеспособных микроорганизмов можно, думается, и из приведенного выше материала. Кроме того, рассмотренные примеры могут быть использованы в той или иной форме при изложении материала на уроках биологии.
Иммобилизованные ферменты Общая характеристика
В современной биотехнологии одно из видных мест принадлежит ферментам. Ферменты и ферментные системы широко используются в различных отраслях промышленности, медицине, сельском хозяйстве, химическом анализе и т.д.
Ферменты - вещества белковой природы и поэтому неустойчивы при хранении, а также чувствительны к тепловым воздействиям. Кроме того, ферменты не могут быть использованы многократно из-за трудностей в отделении их от реагентов и продуктов реакции. Решить эти проблемы помогает создание иммобилизованных ферментов. Начало этому методу было положено в 1916 году, когда Дж.Нельсон и Е.Гриффин адсорбировали на угле инвертазу и показали, что она сохраняет в таком виде каталитическую активность. Сам термин "иммобилизованные ферменты узаконен в 1971 году, и означает любое ограничение свободы передвижения белковых молекул в пространстве.
Преимущества иммобилизованных ферментов перед нативными предшественниками:
1. Гетерогенный катализатор легко отделим от реакционной среды, что дает возможность остановить реакцию в любой момент, использовать фермент повторно, а также получать чистый от фермента продукт.
2. Ферментативный процесс с использованием иммобилизованных ферментов можно проводить непрерывно, регулируя скорость катализируемой реакции и выход продукта.
3. Модификация фермента целенаправленно изменяет его свойства, такие как специфичность (особенно в отношении макромолекулярного субстрата), зависимость каталитической активности от рН, ионного состава и других параметров среды, стабильность к денатурирующим воздействиям.
4. Можно регулировать каталитическую активность иммобилизованных ферментов путем изменения свойств носителя действием физических факторов, таких как свет и звук. Иммобилизовать ферменты можно как путем связывания на нерастворимых носителях, так и путем внутримолекулярной или межмолекулярной сшивки белковых молекул низкомолекулярными бифункциональными соединениями, а также путем присоединения к растворимому полимеру.
Иммобилизованные ферменты Носители для иммобилизованных ферментов
Для получения иммобилизованных ферментов используется ограниченное число как органических, так и неорганических носителей. К носителям предъявляются следующие требования (Дж.Порат, 1974):
- высокая химическая и биологическая стойкость;
- высокая химическая прочность;
- достаточная проницаемость для фермента и субстратов, пористость, большая удельная поверхность;
- возможность получения в виде удобных в технологическом отношении форм (гранул, мембран);
- легкая активация;
- высокая гидрофильность;
- невысокая стоимость.
Классификация носителей схематично представлена на рисунке 4.
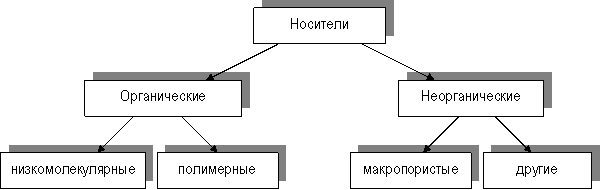
Рис. 4. Классификация носителей для иммобилизованных ферментов
Следует отметить, что органические носители (как низко-, так и высокомолекулярные) могут быть природного или синтетического происхождения. Природные полимерные органические носители делят в соответствии с их биохимической классификацией на 3 группы: полисахаридные, белковые и липидные.
Синтетические полимеры также можно разделить на группы в связи с химическим строением основной цепи макромолекул: полиметиленовые, полиамидные, полиэфирные.
Для иммобилизации ферментов наиболее широко используются природные полисахариды и синтетические носители полиметильного типа, остальные применяются значительно реже. Большое значение природных полимеров в качестве носителей для иммобилизации объясняется их доступностью и наличием реакционно-способных функциональных групп, легко вступающих в химические реакции. Характерной особенностью этой группы носителей также является их высокая гидрофильность. Недостаток природных полимеров - неустойчивость к воздействию микроорганизмов и довольно высокая стоимость.