Материал: Почвенные и водные бактерии-деструкторы полигидроксиалканоатов
Почвенные и водные бактерии-деструкторы полигидроксиалканоатов
Содержание
Введение
Глава 1. Обзор литературы
1.1 Характеристика полигидроксиалканоатов
1.2 Области применения полигидроксиалканоатов
1.3 Биодеградация полигидроксиалканоатов
1.4 Выявление микроорганизмов-деструкторов
Глава 2. Объекты и методы исследования
2.1 Объекты исследования микробной деградации в пресной воде
2.2 Объекты исследования микробной деградации в почве
2.2.1 Основные характеристики почвы дендрария
2.2.2 Определение активной кислотности почвы прикорневой зоны лиственницы
2.3 Определение способности бактерий к биодеградации
2.4 Методы идентификации микроорганизмов
Глава 3. Результаты исследования
3.1 Исследование микробной биодеградации полигидроксибутирата и полигидроксигексаноата в прикорневой зоне лиственницы
3.2 Исследование микробной биодеградации полигидроксибутирата и полигидроксивалерата в пресной воде
Заключение
Список используемых источников
Приложения
Одним из решений экологической проблемы утилизации и переработки полимерных отходов является получение биоразлагаемых материалов. Возможность получения полимеров, сохраняющих эксплуатационные характеристики в период потребления, а затем разлагающихся под воздействием природных факторов на углекислый газ, воду, гуминовые вещества и биомассу. Перспективными полимерами данного типа являются полигидроксиалканоаты (ПГА). Это группа полиэфиров, синтезируемых многими бактериями в качестве источника внутриклеточного углерода и запасаемого источника энергии [1,7].
Биологическая деградация ПГА осуществляется под воздействием ферментов-деполимераз, продуцируемых микроорганизмами, которые используют растворимые продукты расщепления полимеров в качестве субстрата для роста. Выявлено, что факторами, наиболее воздействующими на биоразрушаемость данных полимеров, являются концентрация микроорганизмов-деструкторов, их видовой состав, физико-химические факторы среды, а также состав и свойства полимеров [3,4,24].
Среди эффективных деструкторов ПГА - разнообразные бактерии, относящиеся к широко распространенным почвенным и водным представителям (Pseudomonas, Alcaligenes, Comamonas, Streptomyces, Ilyobacter) [2,3].
Создание экологически чистых материалов с полезными свойствами остается одной из ключевых проблем современности. С ростом перспектив применения ПГА все большую актуальность приобретает исследование закономерностей разрушаемости ПГА в естественных природных условиях. Тем более что результаты по биоразрушаемости ПГА в лабораторных условиях с использованием чистых микробных культур, выделенных из природных источников, а также под воздействием деполимеризующих ферментов, не позволяют предвидеть картину разрушения данного биопластика в природной среде, в многокомпонентных и разнообразных естественных экосистемах [10,21].
В связи с этим цель настоящей работы - идентификация бактерий-деструкторов полигидроксиалканоатов, выделенных из пресной воды тропических искусственных водоемов и бактериальной микрофлоры почвы дендрария, участвующей в деструкции ПГА.
Были поставлены следующие задачи:
. Определить общее микробное число и численность бактерий-деструкторов в почве.
2. Выявить биодеструктивные способности изолятов бактерий, доминирующих в пресноводных и почвенных микробиоценозах.
. Изучить культуральные, морфологические, физиолого-биохимические свойства бактерий-биодеструкторов для их идентификации.
Работа выполнялась на базовой кафедре биотехнологии ИФБиБТ.
Глава 1. Обзор литературы
.1 Характеристика полигидроксиалканоатов
Полигидроксиалканоаты (ПГА) являются запасными веществами в клетках бактерий. Они аккумулируются внутриклеточно в форме включений (гранул) и их масса может составлять до 90% от сухого веса клетки [4,5].
Мономерное строение полигидроксиалканоатов зависит от видовой специфики, условий роста и, особенно источника углерода в среде. Классифицируют ПГА по числу атомов углерода в мономере. Они могут быть короткоцепочечными (ПГАсцл, содержат 3-5 атомов углерода), среднецепочечными (ПГАмцл, 6-15 углеродных атомов) и длинноцепочечными (ПГАлцл, содержат более 15 атомов углерода). Многие бактерии могут одновременно синтезировать ПГАсцл и ПГАмцл, то есть являются гетерогенными [17].
Наиболее изученными из полигидроксиалканоатов являются полигидроксибутират и его сополимеры с оксивалериановой кислотой [4].
Полигидроксибутират (ПГБ) способны накапливать различные прокариотные микроорганизмы. Способность синтезировать данный полимер показана для бактерий родов: Azotobacter, Pseudomonas, Spirillum, Bacillus, Nocardia, Alcaligenes, Chloroflexus и других (всего известно около 100) [4, 15].
Накапливается полигидроксибутират в клетках в виде гранул, которые образованы плотно упакованными тяжами, ограниченными фосфолипидными оболочками с включенными в них белками. По физическим свойствам ПГБ близок к полипропилену. Однако чистый ПГБ характеризуется очень низким растяжением на разрыв, а так же более высокой температурой стеклования, чем полипропилен. Как и все полигидроксиалканоаты он устойчив к воздействию УФ излучения, но малоустойчив к растворителям, кислотам и щелочам. ПГБ нерастворим в воде и относительно устойчив к гидролитическому разложению, это отличает полигидроксибутират, как и прочие ПГА, от других биоразрушаемых пластиков, используемых в настоящее время. ПГБ подвергается растворению хлороформом и другими хлорпроизводными углеводородов [4, 5, 36].
Полигидроксибутират (ПГБ) - гомополимер D (-) - 3-β-оксимасляной кислоты. Он представляет собой изотактический
полиэфир с регулярными, повторяющими единицами (C4H6O2). Его формула выглядит
следующим образом:
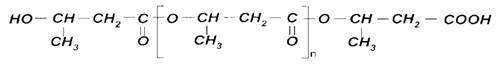
Величина n определяется условиями синтеза полимера микробными клетками, а также методами его экстракции, молекулярный вес колеблется от 60000 до 250000 [7].
У полигидроксибутирата, аналогично многим полимерным материалам, температура, при которой происходит его деформация, ниже температуры кипения (температурной деградации), поэтому газовое состояние в полимерах не реализуется и основным видом фазового равновесия в них является конденсированное состояние - кристаллическое, стеклообразное, вязко-текучее и жидкое [4].
Субстратом для синтеза ПГБ могут служить сахара, спирты, ацетат, водород, органические кислоты. В настоящее время, с развитием технологий и увеличением объема наших знаний, появилась возможность получать полигидроксибутират и его сополимеры, используя широкий спектр исходных веществ, в том числе из промышленных отходов [4, 7].
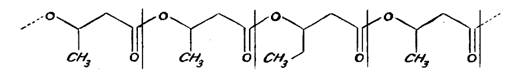
В зависимости от соотношения мономеров в полимере и их природы свойства полимерных материалов изменяются, в т. ч. механическая прочность, температура плавления, биоградируемость [4, 46,55].
Производство других полигидроксиалканоатов зависит от субстрата, на котором выращивали микроорганизмы и от специфичности синтетаз.
Биосинтез полимеров определяется тремя ключевыми ферментами: β-кетотиолаза, ацетоацетил-CoA-редуктаза и ПГА-синтаза кодируемые 25 генами, которые можно клонировать и, благодаря чему создавать новые виды или увеличивать количество необходимых [37,45].
Несмотря на то, что ПГА являются гидрофобными, частично кристаллизованными полимерами, они могут подвергаться деградации различными микроорганизмами, которые выделяют ПГА деполимеразы, разрушающие полимеры [22,26,51].
.2 Области применения полигидроксиалканоатов
ПГА, как уже было отмечено ранее, по ряду физико-химических свойств сходны с широко применяемыми и выпускаемыми в огромных количествах и неразрушаемыми в природной среде синтетическими полимерами типа полипропилена. Линейная структура молекул ПГА придает им свойство термопластичности и изменения прочности. При нагревании молекулярные цепи в ПГА легко сдвигаются относительно друг друга, в результате этого материал размягчается и приобретает текучесть. Данное технологическое свойство имеет большую коммерческую ценность, так как позволяет с использованием различных методов получать из этих полимеров разнообразные изделия. Масштабы применения ПГА в настоящее время сдерживаются достаточно высокой стоимостью, тем не менее сферы их применения постоянно расширяются. [18, 42]
Полигидроксибутират и его сополимеры с валератом используют для получения термоплавких адгезивных материалов, а длинноцепочечные ПГА используют в качестве адгезивов, устойчивых при прессовании. ПГА можно использовать также для замены нефтехимических полимеров в качестве тонеров и проявителей, а также ион-проводящих полимеров. [31, 50, 25, 48, 49]
Из ПГА возможно получение гибких пленок различной толщины, в том числе полупроницаемых мембран, нитей, нетканых материалов, различных полых форм (бутылки, контейнеры, коробки и пр.), а также гелей и клеев. Совокупность свойств, характерных для ПГА, делает их перспективными для применения в различных сферах - медицине, фармакологии, пищевой и косметической промышленности, сельском и коммунальном хозяйстве, радиоэлектронике и других сферах. ПГА активно исследуются с целью переработки в США, Скандинавии и Германии и Голландии. Большой интерес к биодеградируемым ПГА в настоящее время сформировался в США. [18, 42]
Безусловные перспективы и широкий рынок изделий из ПГА наметился в косметологии - это получаемые экструзией различной формы флаконы, банки, бутылки, контейнеры и коробки. Первой бутылкой из ПГА для шампуня стала использовать компания "Wella AG" в Германии. [57]
Отдельные типы ПГА образуют прочные гелии и латексы, поэтому на их основе возможно изготовление клеев, наполнителей, в том числе для стабилизации красителей. Ламинаты ПГА с бумагой и другими полимерами хорошо зарекомендовала себя для изготовления мешков и пакето для хранения разрушаемого мусора, а также одноразовой посуды. Помимо упаковочной тары, контейнеров для пищи и одноразовой посуды, ПГА используют также в качестве пищевых добавок, например, заменителя сливок, средств доставки ароматизаторов и отдушек. [58,59]
Данный материал исследуется и внедряется в различные сферы, включая необычные, например использование в условиях морской воды. Это направление возникло после того, как стало известно, что ПГА достаточно прочны, но при этом хорошо разрушаются не только в почве, но и в морской воде. Моножильные крученые нити из сополимерных ПГА используются для изготовления рыболовных сетей, крабовых ловушек, канатов, а также в практике морской аквакультуры. [28, 52]
Рынок существует и по отношению к продуктам деполимеризации и гидролиза ПГА. Из этих полимеров возможно получение спектра оптически чистых многофункциональных гидроксикислот. [34]
Новое открывающееся направление перспективности ПГА - это получение биотоплива. Недавно показано, что метиловые эфиры 3-гидроксибутирата и среднецепочечных ПГА, полученные этерификацией П3ГБ и среднецепочечных ПГА, могут быть использованы как биотопливо. Температура сгорания этих соединений порядка 20-30 кДж/г, что сопоставимо с температурой сгорания этанола (27кДж/г). По предварительным оценкам, стоимость биотоплива на основе ПГА может составить порядка 1200 дол. США за тонну. [43]
Сегодня существует рынок изделий из ПГА сельскохозяйственного назначения - это пленочная продукция для упаковки продуктов, удобрений, для тепличных хозяйств; горшечная продукция; сетки, канаты и др. В этой связи новым и экологически значимым направлением применения ПГА может стать его использование для депонирования и доставки сельскохозяйственных препаратов. Бурное развитие химии и переход сельского хозяйства на интенсивные технологии привели к появлению и применению огромного разнообразия химических веществ для борьбы с вредителями, сорняками и возбудителями болезней культивируемых видов. Используемые в виде порошков, суспензий и эмульсий, пестициды зачастую не обеспечивают адресную доставку препаратов, что ведет к их рассеиванию и последующей аккумуляции в биосфере. Это вызывает необходимость поиска более эффективных средств и методов защиты полезной биоты, не оказывающих отрицательного воздействия на человека и окружающую среду в целом. [43, 11, 20]
Новым направлением исследований, ориентированных на снижение риска неконтролируемых распространения и аккумуляции ксенобиотиков в биосфере, является разработка экологически безопасных препаратов нового поколения с адресным и контролируемым выходом активного начала за счет использования специальных покрытий или матриксов из биоразрушаемых материалов. Описаны не многочисленные примеры использования полимерных носителей: этилцеллюлозы, полиуретана, альгината натрия, полимеров с памятью формы для депонирования отдельных ядохимикатов. [33, 11, 44, 53]
.3 Биодеградация полигидроксиалканоатов
Способность ПГА к разложению в биологических средах до безвредных продуктов является одним из главных преимуществ, отличающий этот класс соединений от небиоразрушаемых пластиков. ПГА подвергаются биодеструкции как в экосистемах (в почве, водной среде), так и внутри организма. Скорость процесса может сильно варьировать, однако можно выделить несколько основных факторов, влияющих на биологическую деструкцию ПГА и их сополимеров:
· стереоконфигурация полимера (только эфирные соединения мономеров R-конфигурации гидролизуются микробными деполимеразами);
· степень кристалличности полимера (скорость деградации более кристалличных образцов ниже);
· молекулярная масса полимера (чем ниже молекулярная масса ПГА, тем быстрее происходит разложение);
· состав полимеров [24,27].
Наиболее изучаемым аспектом биодеградации ПГА является способность микроорганизмов использовать данные полимеры в качестве субстратов для роста [27]. ПГА могут разрушаться как внутриклеточно внутриклеточными деполимеразами в период аккумулятивной фазы при отсутствии стабильного источника углерода, так и внеклеточно под влиянием внеклеточных деполимераз. Бактерии, секретирующие полимер после его выделения в среду гибнут. Внутриклеточные ПГА деполимеразы не гидролизуют внеклеточные полигидроксиалканоаты, а внеклеточные деполимеразы не могут разрушать внутриклеточные гранулы, что определяется различиями в физической структуре внутриклеточных "нативных" и внеклеточных "денатурированных" гранул ПГА. Последние являются высоко кристаллизованными полимерами. ПГА нативных гранул полностью аморфны и имеют поверхностный слой, состоящий из протеинов и фосфолипидов. Поверхностный слой постепенно разрушается при выделении гранул или под действием других физических и химических факторов. Структуру и состав слоя изучают биохимически, с помощью молекулярной биологии и электронной микроскопии. Когда поверхностный слой гранул разрушен в течение процесса выделения, полимер агрегируется. Кристаллизованные ПГА не связываются с внутриклеточными ПГА-мобилизованными системами [4, 15,14,51].
В литературе изучена динамика разрушения сополимеров гидроксибутирата и гидроксивалерата, с различной величиной включения последнего и установлено, что сополимерные образцы разрушаются быстрее [35].