Материал: Ответы на Экзаменационный Билеты по Микробиологии
Билет № 1 |
Билет № 1 |
Билет № 1 |
1. Вирусы герпеса. Таксономия. Классификация. Характеристика. Микробиологическая диагностика. Специфическое лечение.
ВПГ вызывает герпетическую инфекцию, или простой герпес, характеризующийся везикулезными высыпаниями на коже, слизистых оболочках, поражением ЦНС и внутренних органов, а также пожизненным носительством (персистенцией) и рецидивами болезни. Таксономия. Семейство Herpesviridae. Род Simplexvirus. Структура. Геном ВПГ кодирует около 80 белков, необходимых для репродукции вируса и взаимодействия последнего с клетками организма и иммунным ответом. ВПГ кодирует 11 гликопротеинов, являющихся прикрепительными белками (gB, gC, gD, gH), белками слияния (gB), структурными белками, иммунными белками «уклонения» (gC, gE, gl). Вирус вызывает литические инфекции фибробластов, эпителиальных клеток и латентные инфекции нейронов. Культивирование. Для культивирования вируса применяют куриный эмбрион (на оболочке образуются мелкие плотные бляшки) и культуру клеток, на которой он вызывает цитопатический эффект в виде появления гигантских многоядерных клеток с внутриядерными включениями. Антигенная структура. Вирус содержит ряд антигенов, связанных как с внутренними белками, так и с гликопротеидами наружной оболочки. Последние являются основными иммуногенами, индуцирущими выработку антител и клеточный иммунитет. Существует два серотипа: ВПГ 1 типа и ВПГ 2 типа. Резистентность. Вирус нестоек, чувствителен к солнечным и УФ-лучам. Эпидемиология. Источник инфекции — больной. ВПГ-1 и ВПГ-2 передаются преимущественно контактным путем (с везикулярной жидкостью, со слюной, половых контактах), через предметы обихода, реже — воздушно-капельным путем, через плаценту, при рождении ребенка. Оба типа вирусов могут вызывать оральный и генитальный герпес. ВПГ-1 чаще поражает слизистые оболочки ротовой полости и глотки, вызывает энцефалиты, а ВПГ-2 — гениталии (генитальный герпес). Патогенез. Различают первичный и рецидивирующий простой герпес. Чаще вирус вызывает бессимптомную или латентную инфекцию. Первичная инфекция. Везикула —проявление простого герпеса с дегенерацией эпителиальных клеток. Основу везикулы составляют многоядерные клетки. Пораженные ядра клеток содержат эозинофильные включения. Верхушка везикулы через некоторое время вскрывается, и формируется язвочка, которая вскоре покрывается струпом с образованием корочки с последующим заживлением. Минуя входные ворота эпителия, вирусы проходят через чувствительные нервные окончания с дальнейшим передвижением нуклеокапсидов вдоль аксона к телу нейрона в чувствительных ганглиях. Репродукция вируса в нейроне заканчивается его гибелью. Некоторые вирусы герпеса, достигая ганглионарных клеток, способны приводить к развитию латентной инфекции, при которой нейроны не гибнут, но содержат в себе вирусный геном. Большинство людей (70-90 %) являются пожизненными носителями вируса, который сохраняется в ганглиях, вызывая в нейронах латентную персистирующую инфекцию. Латентная инфекция чувствительных нейронов является характерной особенностью нейротропных герпесвирусов ВПГ. В латентно инфицированных нейронах около 1 % клеток в пораженном ганглии несет вирусный геном. Клиника. Инкубационный период 2—12 дней. Болезнь начинается с возникновения на пораженных участках зуда, появления отека и пузырьков, заполненных жидкостью. ВПГ поражает кожу (везикулы, экзема), слизистые оболочки рта, глотки (стоматит) и кишечника, печень (гепатиты), глаза (кератит) и ЦНС (энцефалит). Рецидивирующий герпес обусловлен реактивацией вируса, сохранившегося в ганглиях. Он характеризуется повторными высыпаниями и поражением органов и тканей. Генитальная инфекция является результатом аутоинокуляции из других пораженных участков тела; но наиболее часто встречающийся путь заражения — половой. Поражение проявляется в образовании везикулы, которая довольно быстро изъязвляется. Вирус простого герпеса проникает во время прохождения новорожденного через родовые пути матери, вызывая неонаталъный герпес. Неонатальный герпес обнаруживается на 6-й день после родов. Вирус диссеминирует во внутренние органы с развитием генерализованного сепсиса. Иммунитет. Основной иммунитет— клеточный. Развивается ГЗТ. NK-клетки играют важную роль в ранней противомикробной защите. Организм пораженного реагирует на гликопротеины вируса, продуцируя цитотоксические Т-лимфоциты, а также Т-хелперы, активирующие В-лимфоциты с последующей продукцией специфических антител. Гликопротеины вызывают образование вируснейтрализующих антител. Вирус - нейтрализующие антитела подавляют межклеточное распространение вирусов. Микробиологическая диагностика. Используют содержимое герпетических везикул, слюну, соскобы с роговой оболочки глаз, кровь, спинномозговую жидкость. В окрашенных мазках наблюдают гигантские многоядерные клетки, клетки с увеличенной цитоплазмой и внутриядерными включениями . Для выделения вируса исследуемым материалом заражают клетки HeLa, Нер-2, человеческие эмбриональные фибробласты. Рост в культуре клеток проявляется округлением клеток с последующим прогрессирующим поражением всей культуры клеток. Заражают также куриные эмбрионы, у которых после внутримозгового заражения развивается энцефалит. Выделенный вирус идентифицируют в РИФ и ИФА с использованием моноклональных антител. Серодиагностику проводят с помощью РСК, РИФ, ИФА и реакции нейтрализации по нарастанию титра антител больного. ИБ также способен выявлять типоспецифические антитела. При экспресс-диагностике в мазках-отпечатках из высыпаний, окрашенных по Романовскому-Гимзе, выявляются гигантские многоядерные клетки с внутриядерными включениями. Для идентификации вируса используют также амплификацию генов вирусной ДНК в реакции ПЦР. Лечение. Для лечения применяют препараты интерферона, индукторы интерферона и противовирусные химиотерапевтические препараты (ацикловир, видарабин). Профилактика. Специфическая профилактика рецидивирующего герпеса осуществляется в период ремиссии многократным введением инактивированной культуральной герпетической вакцины. |
2. Понятие о химиотерапии и антибиотиках. Механизм действия антибиотиков.
Химиотерапия — специфическое антимикробное, антипаразитарное лечение при помощи химических веществ. Эти вещества обладают важнейшим свойством — избирательностью действия против болезнетворных микроорганизмов в условиях макроорганизма. Антибиотики — химиотерапевтические вещества, продуцируемые микроорганизмами, животными клетками, растениями, а также их производные и синтетические продукты, которые обладают избирательной способностью угнетать и задерживать рост микроорганизмов, а также подавлять развитие злокачественных новообразований. По спектру действия антибиотики делят на пять групп в зависимости от того, на какие микроорганизмы они оказывают воздействие. Кроме того, существуют противоопухолевые антибиотики, продуцентами которых также являются актиномицеты. Каждая из этих групп включает две подгруппы: антибиотики широкого и узкого спектра действия. Антибактериальные антибиотики составляют самую многочисленную группу препаратов. Преобладают в ней антибиотики широкого спектра действия, оказывающие влияние на представителей всех трех отделов бактерий. К антибиотикам широкого спектра действия относятся аминогликозиды, тетрациклины и др. Антибиотики узкого спектра действия эффективны в отношении небольшого круга бактерий, например полет-миксины действуют на грациликутные, ванкомицин влияет на грамположительные бактерии. В отдельные группы выделяют противотуберкулезные, противолепрозные, противосифилитические препараты. Противогрибковые антибиотики включают значительно меньшее число препаратов. Широким спектром действия обладает, например, амфотерицин В, эффективный при кандидозах, бластомикозах, аспергиллезах; в то же время нистатин, действующий на грибы рода Candida, является антибиотиком узкого спектра действия. Антипротозойные и антивирусные антибиотики насчитывают небольшое число препаратов. Противоопухолевые антибиотики представлены препаратами, обладающими цитотоксическим действием. Большинство из них применяют при многих видах опухолей, например митоми-цин С. Действие антибиотиков на микроорганизмы связано с их способностью подавлять те или иные биохимические реакции, происходящие в микробной клетке. В зависимости от механизма действия различают пять групп антибиотиков: 1. антибиотики, нарушающие синтез клеточной стенки. К этой группе относятся, например, β-лактамы. Препараты этой группы характеризуются самой высокой избирательностью действия: они убивают бактерии и не оказывают влияния на клетки микроорганизма, так как последние не имеют главного компонента клеточной стенки бактерий — пептидогликана. В связи с этим β -лактамные антибиотики являются наименее токсичными для макроорганизма; 2. антибиотики, нарушающие молекулярную организацию и синтез клеточных мембран. Примерами подобных препаратов являются полимиксины, полиены; 3. антибиотики, нарушающие синтез белка; это наиболее многочисленная группа препаратов. Представителями этой группы являются аминогликозиды, тетрациклины, макроли-ды, левомицетин, вызывающие нарушение синтеза белка на разных уровнях; 4. антибиотики — ингибиторы синтеза нуклеиновых кислот. Например, хинолоны нарушают синтез ДНК, рифампицин — синтез РНК; 5. антибиотики, подавляющие синтез пуринов и аминокислот. К этой группе относятся, например, сульфаниламиды. |
3. Аллергические пробы, их сущность, применение в диагностике инфекционных болезней.
Аллергические пробы - биологические реакции для диагностики ряда заболеваний, основанные на повышенной чувствительности организма, вызванной аллергеном. При многих инфекционных заболеваниях за счет активации клеточного иммунитета развивается повышенная чувствительность организма к возбудителям и продуктам их жизнедеятельности. На этом основаны аллергические пробы, используемые для диагностики бактериальных, вирусных, протозойных инфекций, микозов и гельминтозов. Аллергические пробы обладают специфичностью, но нередко они бывают положительными у переболевших и привитых. Все аллергические пробы подразделяют на две группы — пробы in vivo и in vitro. К первой группе {in vivo) относятся кожные пробы, осуществляемые непосредственно на пациенте и выявляющие аллергию немедленного (через 20 мин) и замедленного (через 24 — 48 ч) типов. Аллергические пробы in vitro основаны на выявлении сенсибилизации вне организма больного. Их применяют тогда, когда по тем или иным причинам нельзя произвести кожные пробы, либо в тех случаях, когда кожные реакции дают неясные результаты. Для проведения аллергических проб используют аллергены — диагностические препараты, предназначенные для выявления специфической сенсибилизации организма. Инфекционные аллергены, используемые в диагностике инфекционных заболеваний, представляют собой очищенные фильтраты бульонных культур, реже взвеси убитых микроорганизмов или АГ, выделенные из них. Кожные пробы. Инфекционные аллергены вводят, как правило, внутрикожно или накожно, путем втирания в скарифицированные участки кожи. При внутрикожном способе в среднюю треть передней поверхности предплечья специальной тонкой иглой вводят 0,1 мл аллергена. Через 28 — 48 ч оценивают результаты реакции ГЗТ, определяя на месте введения размеры папулы. Неинфекционные аллергены (пыльца растений, бытовая пыль, пищевые продукты, лекарственные и химические препараты) вводят в кожу уколом (прик-тест), накожно путем скарификации и втирания или внутрикожной инъекцией разведенного раствора аллергена. В качестве отрицательного контроля используют ИХН, в качестве положительного — раствор гистамина. Результаты учитывают в течение 20 мин (ГНТ) по величине папулы (иногда до 20 мм в диаметре), наличию отека и зуда. Внутрикожные пробы ставят в случае отрицательного или сомнительного результата прик-теста. По сравнению с последним, дозу аллергена уменьшают в 100-5000 раз. Кожные пробы на наличие ГЗТ широко применяют для выявления инфицированности людей микобактериями туберкулеза (проба Манту), возбудителями бруцеллеза (проба Бюрне), лепры (реакция Митсуды), туляремии, сапа, актиномикоза, дерматомикозов, токсоплазмоза, некоторых гельминтозов и др. Пробы in vitro. Эти методы исследования безопасны для больного, достаточно чувствительны, позволяют количественно оценить уровень аллергизации организма. В настоящее время разработаны тесты для определения сенсибилизации, основанные на реакциях Т- и B-лимфоцитов, тканевых базофилов, выявлении общих специфических IgE в сыворотке крови и др. К ним относятся реакции торможения миграции лейкоцитов и бласттрансформации лимфоцитов, специфическое розеткообразование, базофильный тест Шелли, реакция дегрануляции тканевых базофилов, а также аллергосорбентные методы (определение специфических IgE в сыворотке крови). Реакция торможения миграции лейкоцитов (РТМЛ). РТМЛ основана на подавлении миграции моноцитов и других лейкоцитов под действием медиаторов, вырабатываемых сенсибилизированными лимфоцитами, в присутствии специфического аллергена. Реакция бласттрансформации лимфоцитов (РБТ). В основе этой реакции лежит способность нормальных лимфоцитов периферической крови вступать в митоз и превращаться в бластные формы при культивировании их in vitro под действием специфических факторов — аллергенов и неспецифических стимуляторов митогенеза — митогенов (фитогемагглютинин, конканавалин А, липополисахариды и другие вещества). Реакция специфического розеткообразования. Розетки — характерные образования, возникающие in vitro в результате прилипания эритроцитов к поверхности иммунокомпетентных клеток. Розеткообразование может происходить спонтанно, поскольку Т-лимфоциты человека содержат рецепторы к эритроцитам барана. Спонтанное розеткообразование здоровых людей составляет 52 — 53% и служит показателем функционального состояния Т-лимфоцитов. Этот феномен воспроизводится также и в том случае, если используют эритроциты, на которых фиксированы соответствующие аллергены. Реакция дегрануляции тканевых базофилов. Методика основана на том, что под действием аллергена происходит дегрануляция тканевых базофилов крысы, предварительно сенсибилизированных цитофильными AT из сыворотки крови больного. Базофильный тест Шелли. Известно, что базофильные гранулоциты человека или кролика также дегранулируются в присутствии сыворотки больного и аллергена, к которому чувствителен данный пациент. Определение антител класса IgE in vitro. Лабораторная диагностика заболеваний, в основе которых лежит ГНТ, основана на определении аллергенспецифических IgEанти-IgE. При использовании радиоактивной метки метод носит название радиоаллергосорбентного теста (PACT), но чаще в качестве метки используют фермент или флюоресцирующее вещество (ФАСТ). Время анализа — 6 — 7 часов. Принцип метода: фиксированный на твердой основе известный аллерген инкубируют с сывороткой крови больного; находящиеся в сыворотке специфические IgEанти-IgE связываются с аллергеном и, таким образом, остаются фиксированными на основе и могут вступать в специфическое взаимодействие с добавляемыми мечеными анти-IgE. |
Билет № 2 |
Билет № 2 |
Билет № 2 |
1. Синегнойная палочка. Таксономия. Характеристика. Микробиологическая диагностика. Принципы лечения и профилактики.
Морфологические и тинкториальные свойства: Pseudomonas aeruginosa относится к семейству Pseudomonadaceae. Грам «-», прямые палочки, расположенные одиночно, попарно или в виде коротких цепочек. Подвижны. Спор не образуют, имеют пили (фимбрии). При определенных условиях могут продуцировать капсулоподобную внеклеточную слизь полисахаридной природы. Культуральные свойства: облигатные аэробы, которые хорошо растут на простых питательных средах. Для выделения чистой культуры применяют селективные или дифференциально-диагностические питательные среды с добавлением антисептиков. На жидкой питательной среде бактерии образуют характерную серовато-серебристую пленку на поверхности. Колонии гладкие округлые, суховатые или слизистые. Характерным биологическим признаком бактерий вида P. aeruginosa является способность синтезировать водорастворимые пигменты (пиоцианин сине-зеленого цвета), окрашивающие в соответствующий цвет повязки больных или питательные среды при их культивировании. Биохимические свойства: низкая сахаролитическая активность: не ферментирует глюкозу и другие углеводы. Псевдомонады способны только окислять глюкозу. Восстанавливает нитраты в нитриты, обладает протеолитической активностью: разжижает желатину. Синегнойная палочка имеет каталазу и цитохромоксидазу. Многие штаммы синегнойной палочки продуцируют бактериоцины — протеины, обладающие бактерицидными свойствами. Антигенные свойства: О- и Н-антигены. Липополисахарид клеточной стенки является типо- или группо-специфическим термостабильным О-антигеном, на основе которого проводят серотипирование штаммов. Термолабильный жгутиковый Н-антиген бывает двух типов и обладает протективным действием. На поверхности клеток палочки обнаружены антигены пилей. Факторы патогенности: 1.факторы адгезии и колонизации: пили(фимбрии), экстрацеллюлярная слизь, гликолипопротеид – защищает бактерии от фагоцитоза. 2. токсины: эндотоксин – развитие лихорадки; экзотоксин А – цитотоксин, вызывает нарушения клеточного метаболизма; экзоэнзим S; лейкоцидин – токсическое действие на гранулоциты крови. 3.ферменты агрессии: гемолизины (термолабильная фосфолипаза С и термостабильный гликолипид); нейроминидаза; эластаза. Резистентность: условия почти полного отсутствия источников питания; сохраняется в воде. Чувствительна к высушиванию, высокая устойчивость к антибиотикам. Эпидемиология: источник: больной. Механизмы заражения: контактный, респираторный, кровяной, фекально – оральный. Патогенез: проникают через поврежденные ткани. Засевают рану или ожоговую поверхность. Размножаются. Локальные процессы (инфекция мочевыводящих путей, кожи, респираторного тракта). Бактериемия. Сепсис. Клиника: раневые инфекции, ожоговую болезнь, менингиты, инфекции мочевыводящих путей, кожи, заболевания глаз, сепсис. Иммунитет. В сыворотке крови здоровых и переболевших - антитоксические и антибактериальные антитела, однако эти антитела типоспецифические и их роль в защите от повторных заболеваний мало изучена. Микробиологическая диагностика. Материал для исследования: кровь, гной и раневое отделяемое, моча, мокрота. Бактериоскопия – нет, отсутствие морф. и тинктор. особенностей. Основной метод диагностики - бактериологическое исследование клинического материала, позволяет не только идентифицировать возбудитель, но и определить чувствительность бактерий к антимикробным препаратам. При идентификации учитывают рост на агаре, положительный цитохромоксидазный тест, выявление термофильности (рост при 42С). Для внутривидовой идентификации бактерий применяют серотипирование. Серологический метод исследования направлен на обнаружение специфических антител к антигенам палочки (обычно экзотоксину А и ЛПС) с помощью РСК, РПГА. Лечение: антибиотики (цефалоспорины, β-лактамы, аминогликозиды). Тяжелые формы – плазма из крови, иммунизированной поливалентной корпускулярной синегнойной вакциной. Для местного лечения: антисинегнойный гетерологичный иммуноглобулин. Для лечения гнойных инфекций кожи, ожогов – синегнойный бактериофаг. Профилактика: специфическая – стерилизация, дезинфекция, антисептика. Контроль за обсемененностью внешней среды. Неспецифическая– иммуномодуляторы. Пассивная специфическая иммунизация гипериммунной плазмой. Для создания активного иммунитета–вакцины(поливалентная корпускулярная синегнойная вакцина,стафило–протейно-синегнойная вакцина. |
2. Понятие об иммунитете. Виды иммунитета.
Иммунитет – это способ защиты организма от генетически чужеродных веществ – антигенов экзогенного и эндогенного происхождения, направленный на поддержание и сохранение гомеостаза, структурной и функциональной целостности организма, биологической (антигенной)индивидуальности каждого организма и вида в целом. Различают несколько основных видов иммунитета. Врожденный, иди видовой, иммунитет, он же наследственный, генетический, конституциональный — это выработанная в процессе филогенеза генетически закрепленная, передающаяся по наследству невосприимчивость данного вида и его индивидов к какому-либо антигену (или микроорганизму), обусловленная биологическими особенностями самого организма, свойствами данного антигена, а также особенностями их взаимодействия. Примером может служить невосприимчивость человека к некоторым возбудителям, в том числе к особо опасным для сельскохозяйственных животных (чума крупного рогатого скота, болезнь Ньюкасла, поражающая птиц, оспа лошадей и др.), нечувствительность человека к бактериофагам, поражающим клетки бактерий. К генетическому иммунитету можно также отнести отсутствие взаимных иммунных реакций на тканевые антигены у однояйцовых близнецов; различают чувствительность к одним и тем же антигенам у различных линий животных, т. е. животных с различным генотипом. Видовой иммунитет может быть абсолютным и относительным. Например, нечувствительные к столбнячному токсину лягушки могут реагировать на его введение, если повысить температуру их тела. Белые мыши, не чувствительные к какому-либо антигену, приобретают способность реагировать на него, если воздействовать на них иммунодепрессантами или удалить у них центральный орган иммунитета — тимус. Приобретенный иммунитет — это невосприимчивость к антигену чувствительного к нему организма человека, животных и пр., приобретаемая в процессе онтогенеза в результате естественной встречи с этим антигеном организма, например, при вакцинации. Примером естественного приобретенного иммунитета у человека может служить невосприимчивость к инфекции, возникающая после перенесенного заболевания, так называемый постинфекционный иммунитет (например, после брюшного тифа, дифтерии и других инфекций), а также «проиммуниция», т. е. приобретение невосприимчивости к ряду микроорганизмов, обитающих в окружающей среде и в организме человека и постепенно воздействующих на иммунную систему своими антигенами. В отличие от приобретенного иммунитета в результате перенесенного инфекционного заболевания или «скрытной» иммунизации, на практике широко используют преднамеренную иммунизацию антигенами для создания к ним невосприимчивости организма. С этой целью применяют вакцинацию, а также введение специфических иммуноглобулинов, сывороточных препаратов или иммунокомпетентных клеток. Приобретаемый при этом иммунитет называют поствакцинальным, и служит он для защиты от возбудителей инфекционных болезней, а также других чужеродных антигенов. Приобретенный иммунитет может быть активным и пассивным. Активный иммунитет обусловлен активной реакцией, активным вовлечением в процесс иммунной системы при встрече с данным антигеном (например, поствакцинальный, постинфекционный иммунитет), а пассивный иммунитет формируется за счет введения в организм уже готовых иммунореагентов, способных обеспечить защиту от антигена. К таким иммунореагентам относятся антитела, т. е. специфические иммуноглобулины и иммунные сыворотки, а также иммунные лимфоциты. Иммуноглобулины широко используют для пассивной иммунизации, а также для специфического лечения при многих инфекциях (дифтерия, ботулизм, бешенство, корь и др.). Пассивный иммунитет у новорожденных детей создается иммуноглобулинами при плацентарной внутриутробной передаче антител от матери ребенку ииграет существенную роль в защите от многих детских инфекций в первые месяцы жизни ребенка. Поскольку в формировании иммунитета принимают участие клетки иммунной системы и гуморальные факторы, принято активный иммунитет дифференцировать в зависимости от того, какой из компонентов иммунных реакций играет ведущую роль в формировании защиты от антигена. В связи с этим различают клеточный, гуморальный, клеточно-гуморальный и гуморально-клеточ-ный иммунитет. Примером клеточного иммунитета может служить противоопухолевый, а также трансплантационный иммунитет, когда ведущую роль в иммунитете играют цитотоксические Т-лимфоциты-киллеры; иммунитет при ток-синемических инфекциях (столбняк, ботулизм, дифтерия) обусловлен в основном антителами (антитоксинами); при туберкулезе ведущую роль играют иммунокомпетентные клетки (лимфоциты, фагоциты) с участием специфических антител; при некоторых вирусных инфекциях (натуральная оспа, корь и др.) роль в защите играют специфические антитела, а также клетки иммунной системы. В инфекционной и неинфекционной патологии и иммунологии для уточнения характера иммунитета в зависимости от природы и свойств антигена пользуются также такой терминологией: антитоксический, противовирусный, противогрибковый, противобактериальный, противопротозойный, трансплантационный, противоопухолевый и другие виды иммунитета. Наконец, иммунное состояние, т. е. активный иммунитет, может поддерживаться, сохраняться либо в отсутствие, либо только в присутствии антигена в организме. В первом случае антиген играет роль пускового фактора, а иммунитет называют стерильным. Во втором случае иммунитет трактуют как нестерильный. Примером стерильного иммунитета является поствакцинальный иммунитет при введении убитых вакцин, а нестерильного— иммунитет при туберкулезе, который сохраняется только в присутствии в организме микобактерий туберкулеза. Иммунитет (резистентность к антигену) может быть системным, т. е. генерализованным, и местным, при котором наблюдается более выраженная резистентность отдельных органов и тканей, например слизистых верхних дыхательных путей (поэтому иногда его называют мукозальным). |
3. Антибиотики (природные и синтетические). Источники и способы получения. Классы антибиотиков.
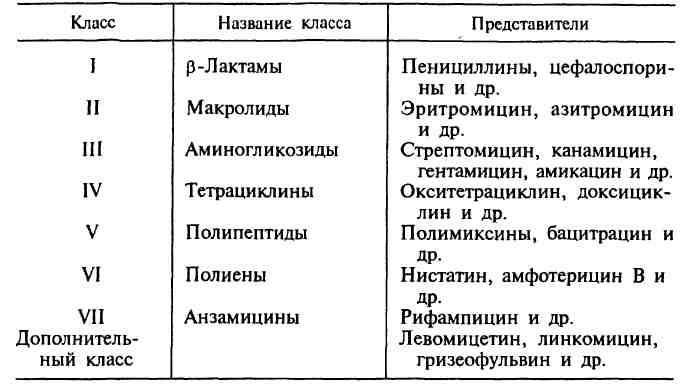
Антибиотики — химиотерапевтические вещества, продуцируемые микроорганизмами, животными клетками, растениями, а также их производные и синтетические продукты, которые обладают избирательной способностью угнетать и задерживать рост микроорганизмов, а также подавлять развитие злокачественных новообразований. За тот период, который прошел со времени открытия П.Эрлиха, было получено более 10 000 различных антибиотиков, поэтому важной проблемой являлась систематизация этих препаратов. В настоящее время существуют различные классификации антибиотиков, однако ни одна из них не является общепринятой. В основу главной классификации антибиотиков положено их химическое строение.
Наиболее важными классами синтетических антибиотиков являются хинолоны и фторхинолоны (например, ципрофлоксацин), сульфаниламиды (сульфадиметоксин), имидазолы (метронидазол), нитрофураны (фурадонин, фурагин). Источники антибиотиков. Основными продуцентами природных антибиотиков являются микроорганизмы, которые, находясь в своей естественной среде (в основном, в почве), синтезируют антибиотики в качестве средства выживания в борьбе за существование. Животные и растительные клетки также могут вырабатывать некоторые вещества с селективным антимикробным действием (например, фитонциды), однако широкого применения в медицине в качестве продуцентов антибиотиков они не получили. Таким образом, основными источниками получения природных и полусинтетических антибиотиков стали: • Актиномицеты (особенно стрептомицеты) — ветвящиеся бактерии. Они синтезируют большинство природных антибиотиков (80 %). • Плесневые грибы — синтезируют природные бета-лактамы (грибы рода Cephalosporium и Penicillium)H фузидиевую кислоту. • Типичные бактерии — например, эубактерии, бациллы, псевдомонады — продуцируют бацитрацин, полимиксины и другие вещества, обладающие антибактериальным действием. Способы получения. Существует три основных способа получения антибиотиков: • биологический синтез (так получают природные антибиотики — натуральные продукты ферментации, когда в оптимальных условиях культивируют микробы-продуценты, которые выделяют антибиотики в процессе своей жизнедеятельности); • биосинтез с последующими химическими модификациями (так создают полусинтетические антибиотики). Сначала путем биосинтеза получают природный антибиотик, а затем его первоначальную молекулу видоизменяют путем химических модификаций, например присоединяют определенные радикалы, в результате чего улучшаются противомикробные и фармакологические характеристики препарата; • химический синтез (так получают синтетические аналоги природных антибиотиков, например хлорамфеникол/левомицетин). |
Билет № 3 |
Билет № 3 |
Билет № 3 |
1. Возбудители полиомиелита. Таксономия и характеристика. Микробиологическая диагностика. Специфическая профилактика и лечение.
Таксономия.: семейство Picornaviridae, род Enterovims, вид Poliovirus. Структура. По структуре полиовирусы — типичные представители рода Enterovirus. РНК-содержащие вирусы. Морфология: мелкие, просто организованные вирусы, сферической формы, состоят из одноцепочечной РНК и капсида. Культивирование: Хорошо репродуцируются в первичных и перевариваемых культурах клеток из тканей человека и сопровождается цитопатическим эффектом. В культуре клеток под агаровым покрытием энтеровирусы образуют бляшки. Антигенные свойства: Различают 3 серотипа внутри вида: 1, 2, 3, не вызывающие перекрестного иммунитета. Все серотипы патогенны дл человека. Патогенез и клиника. Естественная восприимчивость человека к вирусам полиомиелита высокая. Входными воротами служат слизистые оболочки верхних дыхательных путей и пищеварительного тракта. Первичная репродукция вирусов происходит в лимфатических узлах глоточного кольца и тонкой кишки. Из лимфатической системы вирусы проникают в кровь, а затем в ЦНС, где избирательно поражают клетки передних рогов спинного мозга (двигательные нейроны). Инкубационный период продолжается в среднем 7—14 дней. Различают 3 клинические формы полиомиелита: паралитическую, менингеальную (без параличей), абортивную (легкая форма). Заболевание начинается с повышения температуры тела, общего недомогания, головных болей, рвоты, болей в горле. Иммунитет. После перенесенной болезни остается пожизненный типоспецифический иммунитет. Иммунитет определяется наличием вируснейтрализующих антител, среди которых важная роль принадлежит местным секреторным антителам слизистой оболочки глотки и кишечника (местный иммунитет). Пассивный естественный иммунитет сохраняется в течение 3—5 недель после рождения ребенка. Микробиологическая диагностика. Материал для исследования - кал, отделяемое носоглотки, при летальных исходах — кусочки головного и спинного мозга, лимфатические узлы. Вирусы полиомиелита выделяют путем заражения исследуемым материалом первичных и перевиваемых культур клеток. О репродукции вирусов судят по цитопатическому действию. Идентифицируют выделенный вирус с помощью типоспецифических сывороток в реакции нейтрализации в культуре клеток. Важное значение имеет внутривидовая дифференциация вирусов, которая позволяет отличить патогенные штаммы от вакцинных штаммов, выделяющихся от людей, иммунизированных живой полиомиелитной вакциной. Различия между штаммами выявляют с помощью ИФА, реакции нейтрализации цитопатического действия вируса в культуре клеток со штаммоспецифической иммунной сывороткой, а также в ПЦР. Серодиагностика основана на использовании парных сывороток больных с применением эталонных штаммов вируса в качестве диагностикума. Содержание сывороточных иммуноглобулинов классов IgG, IgA, IgM определяют методом радиальной иммунодиффузии по Манчини. Лечение. Патогенетическое. Применение гомологичного иммуноглобулина для предупреждения развития паралитических форм ограничено. Профилактика. Основной мерой профилактики полиомиелита является иммунизация. Первая инактивированная вакцина для профилактики – создавала общий гуморальный иммунитет, не формировала местной резистентности слизистых оболочек ЖКТ, не обеспечивала надежную защиту. Пероральная живая культуральная вакцина из трех серотипов штаммов. Используют для массовой иммунизации детей, она создает стойкий общий и местный иммунитет. Неспецифическая профилактика сводится к санитарно-гигиеническим мероприятиям. |
2. Иммуноглобулины, структура и функции. Классы иммуноглобулинов.
Природа иммуноглобулинов. В ответ на введение антигена иммунная система вырабатывает антитела — белки, способные специфически соединяться с антигеном, вызвавшим их образование, и таким образом участвовать в иммунологических реакциях. Относятся антитела к γ-глобулинам, т. е. наименее подвижной в электрическом поле фракции белков сыворотки крови. В организме γ-глобулины вырабатываются особыми клетками — плазмоцитами. γ-глобулины, несущие функции антител, получили название иммуноглобулинов и обозначаются символом Ig. Следовательно, антитела — это иммуноглобулины, вырабатываемые в ответ на введение антигена и способные специфически взаимодействовать с этим же антигеном. Функции. Первичная функция состоит во взаимодсйствии их активных центров с комплементарными им детерминантами антигенов. Вторичная функция состоит в их способности: • связывать антиген с целью его нейтрализации и элиминации из организма, т. е. принимать участие в формировании защиты от антигена; • участвовать в распознавании «чужого» антигена; • обеспечивать кооперацию иммунокомпетентных клеток (макрофагов, Т- и В-лимфоцитов); • участвовать в различных формах иммунного ответа (фагоцитоз, киллерная функция, ГНТ, ГЗТ, иммунологическая толерантность, иммунологическая память). Структура антител. Белки иммуноглобулинов по химическому составу относятся к гликопротеидам, так как состоят из протеина и Сахаров; построены из 18 аминокислот. Имеют видовые отличия, связанные главным образом с набором аминокислот. Их молекулы имеют цилиндрическую форму, они видны в электронном микроскопе. До 80 % иммуноглобулинов имеют константу седиментации 7S; устойчивы к слабым кислотам, щелочам, нагреванию до 60 °С. Выделить иммуноглобулины из сыворотки крови можно физическими и химическими методами (электрофорез, изоэлектрическое осаждение спиртом и кислотами, высаливание, аффинная хроматография и др.). Эти методы используют в производстве при приготовлении иммунобиологических препаратов. Иммуноглобулины по структуре, антигенным и иммунобиологическим свойствам разделяются на пять классов: IgM, IgG, IgA, IgE, IgD. Иммуноглобулины М, G, А имеют подклассы. Например, IgG имеет четыре подкласса (IgG,, IgG2, IgG3, IgG4). Все классы и подклассы различаются по аминокислотной последовательности. Молекулы иммуноглобулинов всех пяти классов состоят из полипептидных цепей: двух одинаковых тяжелых цепей Н и двух одинаковых легких цепей — L, соединенных между собой дисульфидными мостиками. Соответственно каждому классу иммуноглобулинов, т.е. М, G, A, E, D, различают пять типов тяжелых цепей: μ (мю), γ (гамма), α (альфа), ε (эпсилон) и Δ (дельта), различающихся по антигенности. Легкие цепи всех пяти классов являются общими и бывают двух типов: κ (каппа) и λ (ламбда); L-цепи иммуноглобулинов различных классов могут вступать в соединение (рекомбинироваться) как с гомологичными, так и с гетерологичными Н-цепями. Однако в одной и той же молекуле могут быть только идентичные L-цепи (κ или λ). Как в Н-, так и в L-цепях имеется вариабельная — V область, в которой последовательность аминокислот непостоянна, и константная — С область с постоянным набором аминокислот. В легких и тяжелых цепях различают NH2- и СООН-концевые группы. При обработке γ -глобулина меркаптоэтанолом разрушаются дисульфидные связи и молекула иммуноглобулина распадается на отдельные цепи полипептидов. При воздействии протеолитическим ферментом папаином иммуноглобулин расщепляется на три фрагмента: два не кристаллизующихся, содержащих детерминантные группы к антигену и названных Fab-фрагментами I и II и один кристаллизующий Fc-фрагмент. FabI- и FabII-фрагменты сходны по свойствам и аминокислотному составу и отличаются от Fc-фрагмента; Fab-и Fc-фрагменты являются компактными образованиями, соединенными между собой гибкими участками Н-цепи, благодаря чему молекулы иммуноглобулина имеют гибкую структуру. Как Н-цепи, так и L-цепи имеют отдельные, линейно связанные компактные участки, названные доменами; в Н-цепи их по 4, а в L-цепи — по 2. Активные центры, или детерминанты, которые формируются в V-областях, занимают примерно 2 % поверхности молекулы иммуноглобулина. В каждой молекуле имеются две детерминанты, относящиеся к гипервариабельным участкам Н-и L-цепей, т. е. каждая молекула иммуноглобулина может связать две молекулы антигена. Поэтому антитела являются двухвалентными. Типовой структурой молекулы иммуноглобулина является IgG. Остальные классы иммуноглобулинов отличаются от IgG дополнительными элементами организации их молекулы. В ответ на введение любого антигена могут вырабатываться антитела всех пяти классов. Обычно вначале вырабатывается IgM, затем IgG, остальные — несколько позже. |
3. Микрофлора воздуха и методы ее исследования.
Микробиологический контроль воздуха проводится с помощью методов естественной или принудительной седиментации микробов. Естественная седиментация (по методу Коха) проводится в течение 5—10 мин путем осаждения микробов на поверхность твердой питательной среды в чашке Петри. Принудительная седиментация микробов осуществляется путем «посева» проб воздуха на питательные среды с помощью специальных приборов (импакторов, импинджеров, фильтров). Импакторы — приборы для принудительного осаждения микробов из воздуха на поверхность питательной среды (прибор Кротова, пробоотборник аэрозоля бактериологический и др.). Импшджеры — приборы, с помощью которых воздух проходит через жидкую питательную среду или изотонический раствор хлорида натрия. Санитарно-гигиеническое состояние воздуха определяется по следующим микробиологическим показателям: 1. Общее количество микроорганизмов в 1 м3 воздуха (так называемое общее микробное число, или обсемененность воздуха) — количество колоний микроорганизмов, выросших при посеве воздуха на питательном агаре в чашке Петри в течение 24 ч при 37 °С, выраженное в КОЕ; 2. Индекс санитарно-показательных микробов— количество золотистого стафилококка и гемолитических стрептококков в 1 м3 воздуха. Эти бактерии являются представителями микрофлоры верхних дыхательных путей и имеют общий путь выделения с патогенными микроорганизмами, передающимися воздушно-капельным путем. Появление в воздухе спорообразу-ющих бактерий — показатель загрязненности воздуха микроорганизмами почвы, а появление грамотрицательных бактерий — показатель возможного антисанитарного состояния. Для оценки воздуха лечебных учреждений можно использовать данные из официально рекомендованных нормативных документов. |
Билет № 4 |
Билет № 4 |
Билет № 4 |
1. Вирус кори. Характеристика. Микробиологическая диагностика. Специфическая профилактика и лечение. Понятие о медленных вирусных и прионных инфекциях.
Корь — острая инфекционная болезнь, характеризующаяся лихорадкой, катаральным воспалением слизистых оболочек верхних дыхательных путей и глаз, а также пятнисто-папулезной сыпью на коже. Таксономия. РНК-содержащий вирус. Семейства Paramyxoviridae. Род Morbillivirus. Структура и антигенные свойства. Вирион окружён оболочкой с гликопротеиновыми шипами. Под оболочкой находится спиральный нуклеокапсид. Геном вируса — однонитевая, нефрагменти-рованная минус РНК. Имеются следующие основные белки: NP — нуклеокапсидный; М — матриксный, а также поверхностные гли-козилированные белки липопротеиновой оболочки — гемагглютинин (Н) и белок слияния (F), гемолизин. Вирус обладает гемагглютинирующей и гемолитической активностью. Нейраминидаза отсутствует. Имеет общие антигены с вирусом чумы собак и крупного рогатого скота. Культивирование. Культивируют на первично-трипсинизированных культурах клеток почек обезьян и человека, перевиваемых культурах клеток HeLa, Vero. Возбудитель размножается с образованием гигантских многоядерных клеток — симпластов; появляются цитоплазматические и внутриядерные включения. Белок F вызывает слияние клеток. Резистентность. В окружающей среде нестоек, при комнатной температуре инактивируется через 3-4 ч. Быстро гибнет от солнечного света, УФ-лучей. Чувствителен к детергентам, дезинфектантам. Восприимчивость животных. Корь воспроизводится только на обезьянах, остальные животные маловосприимчивы. Эпидемиология. Корь — антропонозная инфекция, распространена повсеместно. Восприимчивость человека к вирусу кори чрезвычайно высока. Болеют люди разного возраста, но чаще дети 4—5 лет. Источник инфекции — больной человек. Основной путь инфицирования — воздушно-капельный, реже — контактный. Наибольшая заражаемость происходит в продромальном периоде и в 1-й день появления сыпи. Через 5 дней после появления сыпи больной не заразен. Патогенез. Возбудитель проникает через слизистые оболочки верхних дыхательных путей и глаз, откуда попадает в подслизистую оболочку, лимфатические узлы. После репродукции он поступает в кровь (вирусемия) и поражает эндотелий кровеносных капилляров, обуславливая тем самым появление сыпи. Развиваются отек и некротические изменения тканей. Клиника. Инкубационный период 8-15 дней. Вначале отмечаются острые респираторные проявления (ринит, фарингит, конъюнктивит, фотофобия, температура тела 39С). Затем, на 3—4-й день, на слизистых оболочках и коже появляется пятнисто-папулезная сыпь, распространяющаяся сверху вниз: сначала на лице, затем на туловище и конечностях. За сутки до появления сыпи на слизистой оболочке щек появляются мелкие пятна, окруженные красным ореолом. Заболевание длится 7—9 дней, сыпь исчезает, не оставляя следов. Возбудитель вызывает аллергию, подавляет активность Т-лимфоцитов и иммунные реакции, что способствует появлению осложнений в виде пневмоний, воспаления среднего уха и др. Редко развиваются энцефалит и ПСПЭ. Иммунитет. После перенесенной кори развивается гуморальный стойкий пожизненный иммунитет. Повторные заболевания редки. Пассивный иммунитет, передаваемый плоду через плаценту в виде IgG, защищает новорожденного в течение 6 месяцев после рождения. Микробиологическая диагностика. Исследуют смыв с носоглотки, соскобы с элементов сыпи, кровь, мочу. Вирус кори можно обнаружить в патологическом материале и в зараженных культурах клеток с помощью РИФ, РТГА и реакции нейтрализации. Характерно наличие многоядерных клеток и антигенов возбудителя в них. Для серологической диагностики применяют РСК, РТГА и реакцию нейтрализации. Лечение. Симптоматическое. Специфическая профилактика. Активную специфическую профилактику кори проводят подкожным введением детям первого года жизни или живой коревой вакцины из аттенуированных штаммов, или ассоциированной вакцины (против кори, паротита, краснухи). В очагах кори ослабленным детям вводят нормальный иммуноглобулин человека. Препарат эффективен при введении не позднее 7-го дня инкубационного периода. |
2. Комплемент, его структура, функции, пути активации.
Природа и характеристика комплемента. Комплемент является одним из важных факторов гуморального иммунитета, играющим роль в защите организма от антигенов. Комплемент представляет собой сложный комплекс белков сыворотки крови, находящийся обычно в неактивном состоянии и активирующийся при соединении антигена с антителом или при агрегации антигена. В состав комплемента входят 20 взаимодействующих между собой белков, девять из которых являются основными компонентами комплемента; их обозначают цифрами: С1, С2, СЗ, С4... С9. Важную роль играют также факторы В, D и Р (пропердин). Белки комплемента относятся к глобулинам и отличаются между собой по ряду физико-химических свойств. В частности, они существенно различаются по молекулярной массе, а также имеют сложный субъединичный состав: Cl-Clq, Clr, Cls; СЗ-СЗа, СЗЬ; С5-С5а, С5b и т. д. Компоненты комплемента синтезируются в большом количестве (составляют 5—10% от всех белков крови), часть из них образуют фагоциты. Функции комплемента многообразны: а) участвует в лизисе микробных и других клеток (цитотоксическое действие); б) обладает хемотаксической активностью; в) принимает участие в анафилаксии; г) участвует в фагоцитозе. Следовательно, комплемент является компонентом многих иммунологических реакций, направленных на освобождение организма от микробов и других чужеродных клеток и антигенов (например, опухолевых клеток, трансплантата). Механизм активации комплемента очень сложен и представляет собой каскад ферментативных протеолитических реакций, в результате которого образуется активный цитолитический комплекс, разрушающий стенку бактерии и других клеток. Известны три пути активации комплемента: классический, альтернативный и лектиновый. По классическому пути комплемент активируется комплексом антиген-антитело. Для этого достаточно участия в связывании антигена одной молекулы IgM или двух молекул IgG. Процесс начинается с присоединения к комплексу АГ+АТ компонента С1, который распадается на субъединицы Clq, Clr и С Is. Далее в реакции участвуют последовательно активированные «ранние» компоненты комплемента в такой последовательности: С4, С2, СЗ. Эта реакция имеет характер усиливающегося каскада, т. е. когда одна молекула предыдущего компонента активирует несколько молекул последующего. «Ранний» компонент комплемента С3 активирует компонент С5, который обладает свойством прикрепляться к мембране клетки. На компоненте С5 путем последовательного присоединения «поздних» компонентов С6, С7, С8, С9 образуется литический или мембраноатакующий комплекс который нарушает целостность мембраны (образует в ней отверстие), и клетка погибает в результате осмотического лизиса. Альтернативный путь активации комплемента проходит без участия антител. Этот путь характерен для защиты от грамотрицательных микробов. Каскадная цепная реакция при альтернативном пути начинается с взаимодействия антигена (например, полисахарида) с протеинами В, D и пропердином (Р) с последующей активацией компонента СЗ. Далее реакция идет так же, как и при классическом пути — образуется мембраноатакующий комплекс. Лектиновыи путь активации комплемента также происходит без участия антител. Он инициируется особым маннозосвязывающим белком сыворотки крови, который после взаимодействия с остатками маннозы на поверхности микробных клеток катализирует С4. Дальнейший каскад реакций сходен с классическим путем. |
3. Особенности микробиологической диагностики при карантинных инфекциях.
Карантинная (конвенционная) болезнь — это болезнь, система информации и меры профилактики которой обусловлены международными соглашениями . Действуют Международные медико-санитарные правила, которые касаются чумы, холеры, желтой лихорадки и натуральной оспы. Основная цель этих Правил заключалась в обеспечении противоэпидемической защиты государств от заноса инфекций. Правила обязывают национальные органы здравоохранения немедленно уведомлять ВОЗ о возникновении карантинных болезней. При возникновении в любой точке планеты случаев карантинных инфекций вступает в силу система: 1) страна направляет в ВОЗ информацию о возникших случаях; 2) ВОЗ обрабатывает данные и направляет их всем странам мира; 3) страны мира, получив информацию, принимают решение относительно проведения каких-либо особых противоэпидемических мероприятий и информируют об этом ВОЗ; 4) ВОЗ обрабатывает полученную информацию и направляет ее всем странам мира. Контроль за международным распространением инфекционных болезней - система глобального эпидемиологического надзора, направленная на выявление и уменьшение размеров пораженных болезнью территорий, на совершенствование противоэпидемических мероприятий, снижающих риск распространения заболевания в случае его завоза из вне. В России действуют Правила по санитарной охране территории, которые распространяются на особо опасные инфекционные и паразитарные болезни: холеру, чуму, желтую лихорадку (карантинные болезни); вирусные геморрагические лихорадки Ласса, Эбола; малярию; энцефалиты. |
Билет № 5 |
Билет № 5 |
Билет № 5 |
1. Возбудитель гонореи. Таксономия. Характеристика. Микробиологическая диагностика гонореи. Специфическое лечение.
Нейсcерии – грамотрицательные аэробные кокки, относящиеся к роду Neisseria, включающему 8 видов: Neisseria meningitides, Niesseria gonorrhoeae, N. flava, N. subflava, N. perflava, N. sicca. Морфология: неподвижные неспорогенные грамотрицательные диплококки, образующие капсулу, полиморфны – встречаются в виде мелких или крупных форм а так же в виде полочек, хорошо окрашиваются анилиновыми красителями (метиленовым синим, бриллиантовым зелёным и т. д.), под действием пенициллина образуют L-формы, могут менять свойства и превратиться в грамположительную форму. Культуральные свойства: аэробы, хемоорганотрофы; для роста требуют свежеприготовленные влажные среды с добавлением нативных белков крови, сыворотки или асцитической жидкости . Не вызывают гемолиза на средах, содержащих кровь; на средах с добавлением молока, желатина и картофеля не растут. На плотных питательных средах через 24ч, при содержании протеина II образуют слегка мутные бесцветные колонии, не содержащие его образуют круглые прозрачные колонии в виде капель росы, на жидких питательных средах растут диффузно и образуют плёнку, через несколько часов оседающую на дно. Биохимическая активность: крайне низкая – разлагают только глюкозу, продуцируют каталазу и цитохромоксидазу, протеолитическая активность отсутствует, H2S, аммиака, индола не образует. Антигенная структура: Содержит А и К антигены, ЛПС обладают сильной иммуногенностью, основную антигенную нагрузку несут пили и белки мембраны. Наружная мембрана содержит протеины I, II, III классов, проявляющих сильные иммуногеннные свойства Факторы патогенности: капсула, пили, эндотоксин, белки мембраны Капсула обладает антифагоцитарным действием. Пили обеспечивают адгезию к эпителию. Клеточная стенка содержит эндотоксин. Поверхностный белок I класса – обеспечивает устойчивость к бактерицидным факторам слизистых оболочек. Класса II – (протеины мутности, ОРА-протеины) обуславливают прикрепление к эпителию, препятствуют фагоцитозу. N. синтезируют IgA протеазу, расщепляющую Ig. Резистентность: очень неустойчивы в окружающей среде, чувствительны к действию антисептиков, высокочувствительны к пенициллинам, тетрациклину, стрептомицину. Способны к утилизации пенициллинов при приобретении бета-лактамаз. Патогенез: Входные ворота – цилиндрический эпителий мочеполовых путей. Гонококки прикрепляются к эпителию посредством поверхностных белков, вызывают гибель и слущивание клеток, захватываются клетками, где размножаются, попадают на БМ, после чего попадают на соед. ткань и вызывают воспаление или попадают в кровь с возможным дессиминированием. Иммунитет – почти отсутствует. Микробиологическая диагностика: Бактериоскопическое исследование: Материалом для исследования служит гнойное отделяемое из уретры, влагалища, примой кишки, глотки, сыворотки крови. Готовят мазки, окраска по Граму, При «+» результате – обнаруживают гонококки – грам+ диплококки бобовидной формы., находятся внутри лейкоцитов. Положительный диагноз ставится при острой форме гонореи до применения антибиотиков. Бактериологическое исследование. Материал засевают на чашки Петри со специальными питательными средами — КДС, сывороточным агаром. Среда КДС содержит питательный агар с добавлением в определенной концентрации казеина, дрожжевого экстракта и сыворотки крови. Посевы инкубируют при 37°С в течение 24—72 ч. Гонококки образуют круглые прозрачные колонии, напоминающие капли росы, в отличие от более мутных колоний стрептококков или пигментированных колоний стафилококков, которые также могут расти на этих средах. Подозрительные колонии пересевают в пробирки на соответствующие среды для получения чистых культур, которые идентифицируют по сахаролитическим свойствам на средах «пестрого» ряда (полужидкий агар с сывороткой и углеводом). Гонококк ферментирует только глюкозу с образованием кислоты.. Серодиагностика. В некоторых случаях ставят РСК Борде — Жангу. В качестве антигена используют взвесь убитых гонококков. Реакция Борде—Жангу имеет вспомогательное значение при диагностике гонореи. Она положительна при хронической и осложненной гонорее. Лечение: антибиотикотерапия (пенициллин, тетрациклин, канамицин), иммунотерапия - Гонококковая вакцина - взвесь гонококков, убитых нагреванием, используется для вакцинотерапии хронической гонореи. |
2. Классы иммуноглобулинов, их характеристика.
Иммуноглобулины по структуре, антигенным и иммунобиологическим свойствам разделяются на пять классов: IgM, IgG, IgA, IgE, IgD. Иммуноглобулин класса G. Изотип G составляет основную массу Ig сыворотки крови. На его долю приходится 70—80 % всех сывороточных Ig, при этом 50 % содержится в тканевой жидкости. Среднее содержание IgG в сыворотке крови здорового взрослого человека 12 г/л. Период полураспада IgG — 21 день. IgG — мономер, имеет 2 антигенсвязывающих центра (может одновременно связать 2 молекулы антигена, следовательно, его валентность равна 2), молекулярную массу около 160 кДа и константу седиментации 7S. Различают подтипы Gl, G2, G3 и G4. Синтезируется зрелыми В-лимфоцитами и плазматическими клетками. Хорошо определяется в сыворотке крови на пике первичного и при вторичном иммунном ответе. Обладает высокой аффинностью. IgGl и IgG3 связывают комплемент, причем G3 активнее, чем Gl. IgG4, подобно IgE, обладает цитофильностью (тропностью, или сродством, к тучным клеткам и базофилам) и участвует в развитии аллергической реакции I типа. В иммунодиагностических реакциях IgG может проявлять себя как неполное антитело. Легко проходит через плацентарный барьер и обеспечивает гуморальный иммунитет новорожденного в первые 3—4 месяца жизни. Способен также выделяться в секрет слизистых, в том числе в молоко путем диффузии. IgG обеспечивает нейтрализацию, опсонизацию и маркирование антигена, осуществляет запуск комплемент-опосредованного цитолиза и антителозависимой клеточно-опосредованной цитотоксичности. Иммуноглобулин класса М. Наиболее крупная молекула из всех Ig. Это пентамер, который имеет 10 антигенсвязывающих центров, т. е. его валентность равна 10. Молекулярная масса его около 900 кДа, константа седиментации 19S. Различают подтипы Ml и М2. Тяжелые цепи молекулы IgM в отличие от других изотипов построены из 5 доменов. Период полураспада IgM — 5 дней. На его долю приходится около 5—10 % всех сывороточных Ig. Среднее содержание IgM в сыворотке крови здорового взрослого человека составляет около 1 г/л. Этот уровень у человека достигается уже к 2—4-летнему возрасту. IgM филогенетически — наиболее древний иммуноглобулин. Синтезируется предшественниками и зрелыми В-лимфоцитами. Образуется в начале первичного иммунного ответа, также первым начинает синтезироваться в организме новорожденного — определяется уже на 20-й неделе внутриутробного развития. Обладает высокой авидностью, наиболее эффективный активатор комплемента по классическому пути. Участвует в формировании сывороточного и секреторного гуморального иммунитета. Являясь полимерной молекулой, содержащей J-цепь, может образовывать секреторную форму и выделяться в секрет слизистых, в том числе в молоко. Большая часть нормальных антител и изоагглютининов относится к IgM. Не проходит через плаценту. Обнаружение специфических антител изотипа М в сыворотке крови новорожденного указывает на бывшую внутриутробную инфекцию или дефект плаценты. IgM обеспечивает нейтрализацию, опсонизацию и маркирование антигена, осуществляет запуск комплемент-опосредованного цитолиза и антителозависимой клеточно-опосредованной цитотоксичности. Иммуноглобулин класса А. Существует в сывороточной и секреторной формах. Около 60 % всех IgA содержится в секретах слизистых. Сывороточный IgA: На его долю приходится около 10—15% всех сывороточных Ig. В сыворотке крови здорового взрослого человека содержится около 2,5 г/л IgA, максимум достигается к 10-летнему возрасту. Период полураспада IgA — 6 дней. IgA — мономер, имеет 2 антигенсвязывающих центра (т. е. 2-валентный), молекулярную массу около 170 кДа и константу седиментации 7S. Различают подтипы А1 и А2. Синтезируется зрелыми В-лимфоцитами и плазматическими клетками. Хорошо определяется в сыворотке крови на пике первичного и при вторичном иммунном ответе. Обладает высокой аффинностью. Может быть неполным антителом. Не связывает комплемент. Не проходит через плацентарный барьер. IgA обеспечивает нейтрализацию, опсони-зацию и маркирование антигена, осуществляет запуск антителозависимой клеточно-опос-редованной цитотоксичности. Секреторный IgA: В отличие от сывороточного, секреторный sIgA существует в полимерной форме в виде ди- или тримера (4- или 6-валентный) и содержит J- и S-пeптиды. Молекулярная масса 350 кДа и выше, константа седиментации 13S и выше. Синтезируется зрелыми В-лимфоцитами и их потомками — плазматическими клетками соответствующей специализации только в пределах слизистых и выделяется в их секреты. Объем продукции может достигать 5 г в сутки. Пул slgA считается самым многочисленным в организме — его количество превышает суммарное содержание IgM и IgG. В сыворотке крови не обнаруживается. Секреторная форма IgA — основной фактор специфического гуморального местного иммунитета слизистых оболочек желудочно-кишечного тракта, мочеполовой системы и респираторного тракта. Благодаря S-цепи он устойчив к действию протеаз. slgA не активирует комплемент, но эффективно связывается с антигенами и нейтрализует их. Он препятствует адгезии микробов на эпителиальных клетках и генерализации инфекции в пределах слизистых. Иммуноглобулин класса Е. Называют также реагином. Содержание в сыворотке крови крайне невысоко — примерно 0,00025 г/л. Обнаружение требует применения специальных высокочувствительных методов диагностики. Молекулярная масса — около 190 кДа, константа седиментации — примерно 8S, мономер. На его долю приходится около 0,002 % всех циркулирующих Ig. Этот уровень достигается к 10—15 годам жизни. Синтезируется зрелыми В-лимфоцитами и плазматическими клетками преимущественно в лимфоидной ткани бронхолегочного дерева и ЖКТ. Не связывает комплемент. Не проходит через плацентарный барьер. Обладает выраженной цитофильностью — тропностью к тучным клеткам и базофилам. Участвует в развитии гиперчувствительности немедленного типа — реакция I типа. Иммуноглобулин класса D. Сведений об Ig данного изотипа не так много. Практически полностью содержится в сыворотке крови в концентрации около 0,03 г/л (около 0,2 % от общего числа циркулирующих Ig). IgD имеет молекулярную массу 160 кДа и константу седиментации 7S, мономер. Не связывает комплемент. Не проходит через плацентарный барьер. Является рецептором предшественников В-лимфоцитов |
3. Методы определения чувствительности бактерий к антибиотикам.
Для определения чувствительности бактерий к антибиотикам (антибиотикограммы) обычно применяют: • Метод диффузии в агар. На агаризованную питательную среду засевают исследуемый микроб, а затем вносят антибиотики. Обычно препараты вносят или в специальные лунки в агаре, или на поверхности посева раскладывают диски с антибиотиками («метод дисков»). Учет результатов проводят через сутки по наличию или отсутствию роста микробов вокруг лунок (дисков). Метод дисков — качественный и позволяет оценить, чувствителен или устойчив микроб к препарату. • Методы определения минимальных ингибирующих и бактерицидных концентраций, т. е. минимального уровня антибиотика, который позволяет in vitro предотвратить видимый рост микробов в питательной среде или полностью ее стерилизует. Это количественные методы, которые позволяют рассчитать дозу препарата, так как концентрация антибиотика в крови должна быть значительно выше минимальной ингибирующей концентрации для возбудителя инфекции. Введение адекватных доз препарата необходимо для эффективного лечения и профилактики формирования устойчивых микробов. Есть ускоренные способы, с применением автоматических анализаторов. Определение чувствительности бактерий к антибиотикам методом дисков. Исследуемую бактериальную культуру засевают газоном на питательный агар или среду АГВ в чашке Петри. Среда АГВ: сухой питательный рыбный бульон, агар-агар, натрий фосфат двузамещенный. Среду готовят из сухого порошка в соответствии с инструкцией. На засеянную поверхность пинцетом помещают на одинаковом расстоянии друг от друга бумажные диски, содержащие определенные дозы разных антибиотиков. Посевы инкубируют при 37 °С до следующего дня. По диаметру зон задержки роста исследуемой культуры бактерий судят о ее чувствительности к антибиотикам. Для получения достоверных результатов необходимо применять стандартные диски и питательные среды, для контроля которых используются эталонные штаммы соответствующих микроорганизмов. Метод дисков не дает надежных данных при определении чувствительности микроорганизмов к плохо диффундирующим в агар полипептидным антибиотикам (например, полимиксин, ристомицин). Если эти антибиотики предполагается использовать для лечения, рекомендуется определять чувствительность микроорганизмов методом серийных разведений. Определение чувствительности бактерий к антибиотикам методом серийных разведений. Данным методом определяют минимальную концентрацию антибиотика, ингибирующую рост исследуемой культуры бактерий. Вначале готовят основной раствор, содержащий определенную концентрацию антибиотика (мкг/мл или ЕД/мл) в специальном растворителе или буферном растворе. Из него готовят все последующие разведения в бульоне (в объеме 1 мл), после чего к каждому разведению добавляют 0,1 мл исследуемой бактериальной суспензии, содержащей 106—107 бактериальных клеток в 1 мл. В последнюю пробирку вносят 1 мл бульона и 0,1 мл суспензии бактерий (контроль культуры). Посевы инкубируют при 37 °С до следующего дня, после чего отмечают результаты опыта по помутнению питательной среды, сравнивая с контролем культуры. Последняя пробирка с прозрачной питательной средой указывает на задержку роста исследуемой культуры бактерий под влиянием содержащейся в ней минимальной ингибирующей концентрации (МИК) антибиотика. Оценку результатов определения чувствительности микроорганизмов к антибиотикам проводят по специальной готовой таблице, которая содержит пограничные значения диаметров зон задержки роста для устойчивых, умеренно устойчивых и чувствительных штаммов, а также значения МИК антибиотиков для устойчивых и чувствительных штаммов. К чувствительным относятся штаммы микроорганизмов, рост которых подавляется при концентрациях препарата, обнаруживаемых в сыворотке крови больного при использовании обычных доз антибиотиков. К умеренно устойчивым относятся штаммы, для подавления роста которых требуются концентрации, создающиеся в сыворотке крови при введении максимальных доз препарата. Устойчивыми являются микроорганизмы, рост которых не подавляется препаратом в концентрациях, создаваемых в организме при использовании максимально допустимых доз. Определение антибиотика в крови, моче и других жидкостях организма человека. В штатив устанавливают два ряда пробирок. В одном из них готовят разведения эталонного антибиотика, в другом — исследуемой жидкости. Затем в каждую пробирку вносят взвесь тест-бактерий, приготовленную в среде Гисса с глюкозой. При определении в исследуемой жидкости пенициллина, тетрациклинов, эритромицина в качестве тест-бактерий используют стандартный штамм S. aureus, а при определении стрептомицина — Е. coli. После инкубирования посевов при 37 °С в течение 18—20 ч отмечают результаты опыта по помутнению среды и ее окрашиванию индикатором вследствие расщепления глюкозы тест-бактериями. Концентрация антибиотика определяется умножением наибольшего разведения исследуемой жидкости, задерживающей рост тест-бактерий, на минимальную концентрацию эталонного антибиотика, задерживающего рост тех же тест-бактерий. Например, если максимальное разведение исследуемой жидкости, задерживающее рост тест-бактерий, равно 1 :1024, а минимальная концентрация эталонного антибиотика, задерживающего рост тех же тест-бактерий, 0,313 мкг/мл, то произведение 1024- 0,313=320 мкг/мл составляет концентрацию антибиотика в 1 мл. Определение способности S. aureus продуцировать бета-лактамазу. В колбу с 0,5 мл суточной бульонной культуры стандартного штамма стафилококка, чувствительного к пенициллину, вносят 20 мл расплавленного и охлажденного до 45 °С питательного агара, перемешивают и выливают в чашку Петри. После застывания агара в центр чашки на поверхность среды помещают диск, содержащий пенициллин. По радиусам диска петлей засевают исследуемые культуры. Посевы инкубируют при 37 °С до следующего дня, после чего отмечают результаты опыта. О способности исследуемых бактерий продуцировать бета-лакта-мазу судят по наличию роста стандартного штамма стафилококка вокруг той или другой исследуемой культуры (вокруг диска). |