Материал: Оптимальный материал для изготовления индикаторного электрода
Концентрация перекиси водорода в сосуде, где
происходила отбелка целлюлозы, определялась путем отбора проб через некоторые
промежутки времени. Взятая проба от начала отбелки в количестве 10 мл
выливалась в 20 мл 1н NaОН, при этом рН раствора становилось равным всегда
13,6, независимо от того, какое значение рН имел раствор пробы (в ходе отбелки
рН изменялся от -11,5-12 до ~10 рН). При измерении в ячейке поддерживалась
температура 200 С. Параллельно в другой пробе велось определение концентрации
перекиси водорода иодометрически. Полученное таким способом значение концентрации
Н2О2 сравнимо с величиной, определённой по постоянным значениям потенциала
электродов (время установки 8-10 мин). Результаты одного из опытов по
определению концентрации Н2О2 в процессе отбелки целлюлозы представлены в
таблице 1. Здесь приведены дополнительно концентрации перекиси водорода,
определенные методом обратного титрования в пробах, взятых уже из ячейки после
потенциометрических измерений.
|
Таблица 1. Сравнение концентраций перекиси водорода, определенной химическим и потенциометрическим методами в процессе отбелки целлюлозы |
||||
|
Время отбелки |
Концентрация Н2О2 (m/л) |
Отн. % (потенц./ объемн.) |
||
|
|
Объемный анализ |
потенциометрический методами |
|
|
|
|
Ячейка |
сосуд |
|
|
|
2 мин |
2,36*10-2 |
2,39*10-2 |
2,49*10-2 |
-4,2 |
|
15 мин |
1,2*10-2 |
1,14*10-2 |
1,2*10-2 |
-5,3 |
|
30 мин |
7,9*10-3 |
8,0*10-3 |
8,7*10-3 |
-8,8 |
|
40 мин |
7,25*10-3 |
6,27*10-3 |
6,9*10-3 |
-7,9 |
|
60 мин |
5,15*10-3 |
5,4*10-3 |
5,85*10-3 |
-8,4 |
|
120 мин |
3,0*10-3 |
2,7*10-3 |
3*10-3 |
-11,1 |
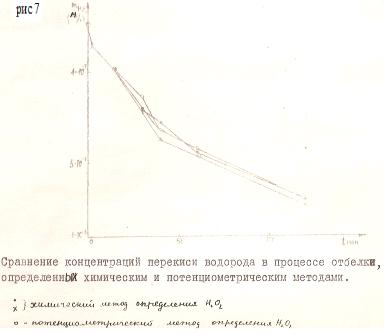
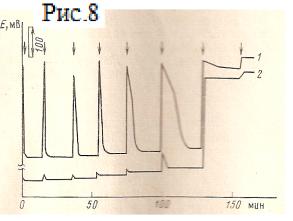
Рис.8Кривые потенциометрического титрования
0,02М раствора Н2О2 4*10-2М К3Fe(CN)6 (1) и 2*10-2М NaBrO (2)
Как видно из табл. 1. и рис. 7 наблюдается хорошее соответствие результатов определений двумя методами.[5]
М.у.р.с.э. также использовали для определения
Н2О2 при титровании ее щелочных растворов рядом окислителей. На рис.8
представлена зависимость Е(t) в ходе титрования Н2О2 растворами ферроцианида
калия и гипобромида натрия. В обоих случаях добавление каждой новой порции
окислителя сопровождается резким повышением потенциалов м.у.р.с.э. с
последующим возвращением к стационарным значениям. Это возвращение становится
тем более медленным, чем ближе точка эквивалентности. Причиной наблюдаемого
характера изменения потенциалов является малая скорость объемного
взаимодействия реагентов.[3]
Выводы
По приведенным данным в литературе наиболее перспективным материалом для изготовления индикаторного электрода в окислительно-восстановительной системе О2/Н2О2 является графит (углерод). [Берл]
Для определения концентрации (активности) перекиси водорода в щелочных средах были созданы и изучены редоксметрические стеклянные электроды, поверхность которых модифицирована углеродом (графитом) [м.у.р.с.э.]. Такие электроды имеют высокую стабильность и воспроизводимость показаний при рН ≥12,8, в интервале концентраций Н2О2 от 0,8 м до 10-5м при температуре 20-600 С и позволяют осуществлять потенциометрическое определение перекиси водорода с погрешностью±10% относит.
Электрохимическое излучение редоксметрических стеклянных электродов с модифицированной углеродом поверхностью показало, что ведущая роль в сочетании стекло - графит (углерод), принадлежит графиту (углероду). Функции электронопроводящего стекла состоят в том, что оно изменяет каталитическую активность нанесенного графита по отношению к растворам Н2О2 и является удобной подложкой и токоотводом для этих электродов.
Опыты по отбелке целлюлозы и редокс титрование,
в котором использовал м.у.р.с.э., показали высокую точность в определении Н2О2
при отбелке и в процессах титрования.
Список литературы
[1] Ахметов Н. С. Общая и неорганическая химия. - М.: Высшая школа, 2001, с.743.
[2] Berl W.Y.Обратимый кислородный электрод Trans. Electrochem Soc., 1943, 83, с.253.
[3] Писаревский А.М., Полозова И.П., Авраменко А.В., Электрод для потенциометрического определения перекиси водорода в щелочных средах, Журнал аналитической химии т. 35в.11- Москва, 1980., с2187-2194
[4] Неумывакин И. П. Перекись водорода: мифы и реальность. Москва - Санкт-Петербург. Издательство «Диля» 2005, с.144.
[5] Писаревский А.М., Разработка электродной системы для потенциометрического определения концентрации перекиси водорода, отчет НИИХ СПбГУ,1975
[6] Шульц М.М. Писаревский А.М. Полозова И.П. Окислительный потенциал. Теория и практика. - Л.: Химия, 1984, с.160.
[7] Полозова И.П., Писаревский А.М., Шульц М.М, Стандартный потенциал и температурный коэффициент кислородно-перекисного электрода, Электрохимия, т.13, в.10,1977, с. 1560-1562