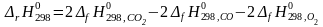Материал: Методические указания к выполнению контрольных работ по дисциплине “Физическая химия материалов и процессов электронной техники”. Николаева Е.П., Новокрещенова Е.П
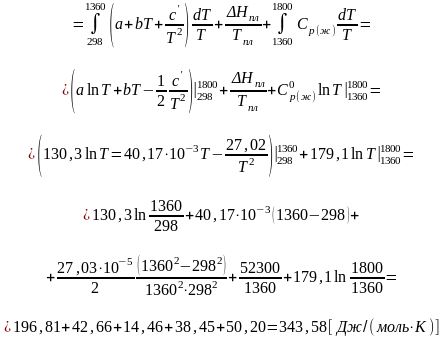
Примечание. Уравнения (1) и (2) приведены для 1 моля вещества. Если по условию задачи нужно найти S для n молей вещества, то
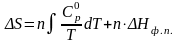 .
.
Если по условию задачи нужно найти изменение энтропии для m г вещества, то необходимо вес пересчитать на число молей:
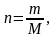
где m - вес вещества в граммах; М - молекулярная масса.
3.1.2. Расчет изменения энтальпии вещества
Изменение энтальпии при Р = const определяется как
|
(3) |
Если в рассматриваемом интервале температур происходит изменение фазовых состояний системы, то в выражение (3) необходимо добавить значения фазовых переходов. В общем случае изменение энтальпии, если в заданном интервале Т1 - Т2 имеют место фазовые переходы плавления и кипения,
|
(4) |
Пример расчета
Задача 4. Найти количество теплоты, расходуемой на нагревание 1 кг кварца от Т1 до Т2.
Решение. По справочнику находим
|
(5) |
Если в заданном интервале температур нет фазового перехода (Тпл = 1600 °С), то
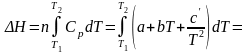
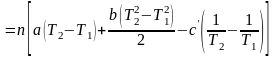
Подставив значения а, b и с' из уравнения (5), получим значение Н, расходуемое на нагревание 1 кг кварца от T1 до Т2.
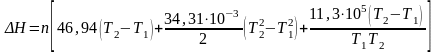
где n - число молей в 1 кг кварца.
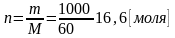 ;
;
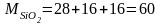 ;
;
m = 1000 г.
Подставляя T1 и Т2, например, T1 = 300 К и Т2 = 1200 К, найдем количество теплоты, расходуемое на нагревание 1 кг кварца от 300 К до 1200 К.
Если Т2 > Тпл , нужно учесть фазовый переход плавления, тогда
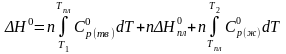 .
.
3.2. Расчет теплового эффекта, изменения энтропии и изменения энергии Гиббса химической реакции
Задание.
Определить тепловой эффект
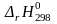 ,
изменение энтропии
,
изменение энтропии
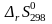 и изменение энергии Гиббса
и изменение энергии Гиббса
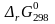 химической реакции аА
+ bD
= сС
+ dD.
химической реакции аА
+ bD
= сС
+ dD.
Определить
направление химической реакции при Т1
= 298 К и при заданной
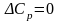 температуре
Т2,
предполагая, что
температуре
Т2,
предполагая, что
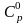 = const
или
= const
или
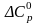 = 0.
= 0.
Примечание.
Значения
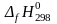 и
и
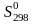 находят по табл. П.1 приложения, температуру
Т2
определяют по табл. 12, конкретную
химическую реакцию определяют по табл.
13 (номер варианта соответствует номеру
студента в алфавитном списке группы).
находят по табл. П.1 приложения, температуру
Т2
определяют по табл. 12, конкретную
химическую реакцию определяют по табл.
13 (номер варианта соответствует номеру
студента в алфавитном списке группы).
Таблица 12
Последняя цифра шифра |
1 |
2 |
3 |
4 |
5 |
Температура Т2 К |
1000 |
1100 |
1200 |
1300 |
1400 |
Продолжение табл. 12
Последняя цифра шифра |
6 |
7 |
8 |
9 |
0 |
Температура Т2 К |
1500 |
1600 |
1700 |
1800 |
1900 |
Таблица 13
Номер варианта |
Реакция |
1 |
2 |
1 |
Н2(г) + Сl2(г) = 2НС1(г) |
2 |
Н2(г) + Br2(г) = 2НВr(г) |
3 |
Н2(г) + I2(г) = 2Hl(г) |
4 |
2Сl2(г) + 2Н2O(г) = 4НСl(г) + O2(г) |
5 |
СО(г) + Сl2(г) = СОСl2(г) |
6 |
2Н2(г) + O2(г) = 2Н2O(г) |
7 |
2СО(г) + O2(г) = 2СO2(г) |
8 |
СО(г) + Н2O(г) = Н2(г) + СO2(г) |
9 |
2Н2(г) + S2(г) = 2H2S(г) |
10 |
2SO2(r) + O2(г) = 2SO3(г) |
11 |
N2(r) + ЗН2(г) = 2NH3(г) |
12 |
2ВО(г) + O2(г) = 2NO2(г) |
13 |
N2(r) + O2(г) = 2NO(г) |
14 |
2HBr(г) = Н2(г) + Вг2(г) |
15 |
2НСl(г) = Н2(г) + Сl2(г) |
16 |
2НI(г) = Н2(г) + I2(г) |
17 |
4НСl(г) + O2(г) = 2Сl2(г) + 2Н2O(г) |
18 |
СОСl2(г) = СО(г) + Сl2(г) |
19 |
2Н2O(г) = H2(г) + O2(г) |
20 |
2СO2(г) = 2СО(г) + O2(г) |
21 |
Н2(г) + СO2(г) = СО(г) + Н2O(г) |
22 |
2H2S(г) = Н2(г) + S2(г) |
23 |
2SO3(г) = 2SO2(г) + O2(г) |
24 |
2NH3(г) = 2NO2(г) + ЗН2(г) |
25 |
2NO2(г) = 2NO(г) + O2(г) |
26 |
CO2(г) + H2(г) = CO(г) + H2O(г) |
27 |
2NO(г) = N2(г) + O2(г) |
28 |
NHCl(г) = NH3(г) + HCl(г) |
29 |
H2(г) + F2(г) = 2HF(г) |
30 |
2HF(г) = H2(г) + F2(г) |
3.2.1. Расчет теплового эффекта химической реакции
Тепловой
эффект химической реакции
при стандартных условиях: температуре
298 К и давлении 0,1013 МПа (1 атм) определяется
по значению стандартных теплот образования
или сгорания
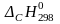 ,
значения которых можно найти в справочниках
(см, табл. П.1 приложения).
,
значения которых можно найти в справочниках
(см, табл. П.1 приложения).
Тепловой эффект химической реакции равен разности между суммой теплот образования продуктов реакции и суммой теплот образования исходных веществ.
|
(6) |
где ni - стехиометрический коэффициент в уравнении реакции; в первой скобке - сумма теплот образования продуктов; во второй - сумма теплот образования исходных веществ.
Для реакции
aA + bD = cC + dD |
(7) |
в соответствии с уравнением (6) находим тепловой эффект химической реакции:
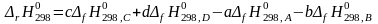 .
.
Пример расчета
Задача 5. Найти тепловой эффект химической реакции
2СО + O2 = 2СO2 |
(8) |
при стандартных условиях.
Решение. В соответствии с уравнением (6) тепловой эффект этой реакции при T = 298 К
|
(9) |
Выпишем из табл. П.1 в табл. 14 значения термодинамических величин компонентов для данной реакции.
Таблица 14
Стандартные термодинамические величины веществ
-
Вещество
, кДж/моль
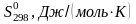
СO2
-393,51
213,6
O2
0
205,03
CO
-110,50
197,40
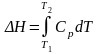
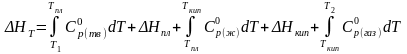
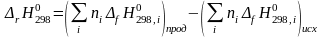 ,
,