Материал: Методические указания к выполнению контрольных работ по дисциплине “Физическая химия материалов и процессов электронной техники”. Николаева Е.П., Новокрещенова Е.П
Таблица 7
Номер варианта |
Вопросы |
|
Предпоследняя цифра шифра |
Последняя цифра шифра |
|
1, 3, 5, 7, 9 |
3 |
1. Термодинамические потенциалы. Изменение энергии Гельмгольца в изохорно-изотермических условиях. Критерий равновесия и самопроизвольности процесса при Т = const, V = const [1,С.94-95; 2,С.61-64; 3,С.38-40]. 2. Постулат Планка. Абсолютное значение энтропии [1, С. 124 - 125; 2, С. 71 - 72; 3, С. 66 - 67]. 3.Диаграмма состояния двухкомпонентной системы с эвтектикой и полной нерастворимостью компонентов в твердых фазах [1,С.164 - 166; 2, С. 190 - 192]. 4. Характеристика и свойства растворов [1, С. 181 -182; 2, С. 153 - 156; 3, С. 108 - 109]. 5.Термодинамические процессы: равновесные и неравновесные, обратимые и необратимые, самопроизвольные вынужденные [1, С. 59 - 60, 81 - 82; 2, С. 17 - 19; 3, С. 21 - 24]. |
1, 3, 5, 7, 9 |
4 |
1. Термодинамические потенциалы. Изменение энергии Гиббса - критерий равновесия и самопроизвольности процесса в изобарно-изотермических условиях [1, С. 94 - 95; 2, С. 61 - 64; 3, С. 38 - 42]. 2. Формальная кинетика. Уравнения нулевого и первого порядка [1, С. 300 - 307; 2, С. 254 - 260; 3, С. 111 - 116]. 3. Диаграмма состояния системы с химическим соединением, плавящимся конгруэнтно [1, С. 166 - 167]. 4. Летучие смеси с неограниченно смешивающимися жидкостями. Зависимость давления пара от состава идеальной и реальной смеси [1, С. 213 - 215; 2, С. 158 - 160; 3, С. 71 - 74]. 5. Первый закон термодинамики [1, С. 60 - 62; 2, С 27 - 30; 3, С. 5 - 71]. |
Таблица 8
Номер варианта |
Вопросы |
||
Предпоследняя цифра шифра |
Последняя цифра шифра |
||
1, 3, 5, 7, 9 |
5 |
1. Химический потенциал [1, С. 98 - 100; 2, С. 74 - 77; 3, С. 51 - 52]. 2. Формальная кинетика. Уравнения первого и второго порядка [1, С. 300 - 306; 2, С. 254 - 260; 3, С. 108 - 116]. 3. Диаграмма состояния с твердыми растворами, компоненты которых неограниченно растворимы [1, С. 170 - 172; 2, С, 187 - 189]. 4. Диаграмма состояния состав - давление пара двойной реальной системы без экстремума [1, С. 213 - 214; 2, С. 175 - 176; 3, С. 84 - 85]. 5. Теплоемкость [1, С. 72 - 77; 2, С. 30 - 32; 3, С. 11 - 15]: |
|
1, 3 5, 7, 9 |
6 |
1. Химический потенциал реального газа. Фугитивность [1, С. 100 - 103; 2, С. 83 - 84; 3, С. 83 - 84]. 2. Формальная кинетика. Уравнения второго и n-го порядка [1, С. 300 - 306; 2, С. 254 - 260; 3, С. 108 - 116]. 3. Диаграмма состояния двухкомпонентной системы эвтектического типа с ограниченной растворимостью в твердом состоянии [1, С. 172 - 173]. 4. Диаграмма состояния состав - температура кипения двойной жидкой системы без экстремума [1, С. 213 - 215; 2, С. 175 - 176; 3, С. 87 - 89]. 5. Сущность приведенных теплот. Энтропия [1, С. 85 - 87; 2, С. 55 - 57; 3, С. 26 - 28]. |
|
Таблица 9
Номер варианта |
Вопросы |
|
Предпоследняя цифра шифра |
Последняя цифра шифра |
|
1, 3, 5, 7, 9 |
7 |
1. Химический потенциал неидеальных растворов. Активность и коэффициент активности [1, С. 105 - 106; 2, С. 84 - 87; 3, С. 83 - 84]. 2. Химическое равновесие. Константа равновесия [1, С. 108 - 109; 2, С. 78 - 79]. 3. Фазовое равновесие. Основные понятия и определения [1, С. 152 - 154; 2, С. 97 - 98]. 4. Диаграмма состояния состав - давление пара двойной жидкой системы с максимумом и минимумом [1, С. 216 - 217; 2, С. 178 - 179; 3, С. 86 - 87]. 5. Второй закон термодинамики для необратимых процессов [1, С. 87 - 90; 2, С. 49 - 50; 3,С. 28 – 29] |
1, 3, 5, 7, 9 |
8 |
1. Закон Гесса [1, С. 64 - 65; 2, С. 32 - 33; 3, С. 17 - 18]. 2. Уравнение изотермы химической реакции [1, С. 110 - 111; 2, С. 87 - 88]. 3. Основной закон фазового равновесия - правило фаз Гиббса [1, С. 154 - 155; 2, С. 98 - 101]. 4. Диаграмма состояния состав - температура кипения двойной жидкой системы с максимумом и минимумом [1, С. 216 - 217; 2, С. 178 - 179; 3, С. 90 - 93]. 5, Расчет энтропии для изотермического, изобарного, изохорного процессов, для различных процессов идеального газа [1, С. 90 - 93; 3, С. 30 - 33]. |
Таблица 10
Номер варианта |
Вопросы |
||
Предпоследняя цифра шифра |
Последняя цифра шифра |
||
1, 3, 5, 7, 9 |
9 |
1. Следствия закона Гесса [1, С. 65 - 67; 2, С. 35 - 39; 3, С. 18 - 19]. 2. Уравнение изотермы и направление химической реакции. Стандартная энергия Гиббса реакции [1, С. 111 - 113; 2, С. 88 - 89]. 3. Уравнение Клапейрона-Клаузиуса [1, С. 156 - 158; 2, С. 102 - 104]. 4. Перегонка летучих жидких смесей первого типа с неограниченной растворимостью компонентов [1, С. 218 - 219; 2, С. 182 - 184; 3, С. 89 - 90]. 5. Энергия Гиббса [1, С. 94 - 95; 2, С. 59 - 61; 3, С. 40 - 41]. |
|
1, 3, 5, 7, 9 |
0 |
1. Зависимость теплового эффекта от температуры [1, С. 78 - 80; 2, С. 44 - 47; 3, С. 19 - 20]. 2. Вычисление стандартной энергии Гиббса косвенным путем методом комбинирования химических реакций [1, С. 113 - 115; 2, С. 81 - 82]. 3. Физико-химический анализ. Термический анализ [1, С. 162 - 163; 2, С. 193 - 195]. 4. Перегонка жидких летучих смесей второго типа (с азеотропом) с минимумом на кривой температуры кипения [1, С. 220 - 221; 2, С. 185 - 187; 3, С. 90 - 92]. 5. Энергия Гельмгольца [1, С. 94 - 96; 2, С. 59 – 61; 3, С. 38 - 40]. |
|
3. Задачи
3.1. Расчет изменения энтропии и энтальпии вещества
Задание. Найти изменение энтропии S и энтальпии Н n молей вещества в интервале температур Т1 – Т2 (Т1 = 298 К). Расчет сделать в общем виде, затем рассчитать, используя значения Cp0 из табл. П.1.
Примечание. Название вещества определяется по табл. П.1 (номер варианта соответствует номеру студента в алфавитном списке группы), число молей вещества n и температура T2 определяются по табл. 11.
Таблица 11
Последняя цифра шифра |
1 |
2 |
3 |
4 |
5 |
Число молей вещества n |
10 |
9 |
8 |
7 |
6 |
Температура T2, K |
600 |
700 |
800 |
900 |
1000 |
Продолжение табл. 11
Последняя цифра шифра |
6 |
7 |
8 |
9 |
0 |
Число молей вещества n |
5 |
4 |
3 |
2 |
1 |
Температура T2, K |
1100 |
1200 |
1300 |
1400 |
1500 |
3.1.1. Расчет изменения энтропии вещества при Р = const
Общее выражение для расчета изменения энтропии при Р = const с температурами плавления и кипения Тпл и Ткип можно записать в виде:
|
(1) |
где Ср(тв), Ср(ж), Ср(газ) - теплоемкости твердого, жидкого, газообразного состояния вещества; Нпл и Нкип - теплота плавления и кипения при нормальном давлении;
|
(2) |
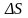 -
изменение энтропии при фазовом переходе
плавления и кипения.
-
изменение энтропии при фазовом переходе
плавления и кипения.
Примеры расчета
Задача
1.
Найти изменение энтропии 1 моля Н2О
(ж) при нагревании от 0 °С до 100 °С, если
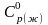 = 75,44 Дж/моль.
= 75,44 Дж/моль.
Решение.
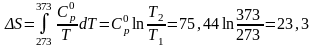
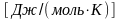
Нужно обратить внимание на то, что в расчетную формулу подставляют температуру в градусах Кельвина.
Задача 2. Найти изменение энтропии при превращении 1 моля льда при 0 °С в пар при 100 °С.
Решение.
По справочнику находим теплоту плавления
и кипения -
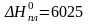 Дж/моль
и
Дж/моль
и
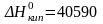 Дж/моль, теплоемкость жидкого состояния
-
Дж/моль, теплоемкость жидкого состояния
-
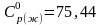
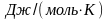 .
.
Очевидно, что при данных условиях нужно учесть два фазовых перехода - изменение энтропии при плавлении и кипении.
Таким образом,
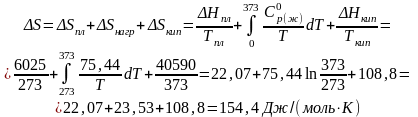
Задача 3. Найти изменение энтропии 1 моля Na2SiO3 при нормальном давлении в интервале температур 298 - 1800 К.
Решение.
По справочнику находим: Тпл
= 1360 К, Нпл
= 52390 Дж/моль,
= 179,1 Дж/(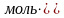 К),
т.е. в заданном интервале температур
нужно учесть фазовый переход плавления.
К),
т.е. в заданном интервале температур
нужно учесть фазовый переход плавления.
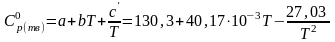
С учетом наличия фазового перехода плавления
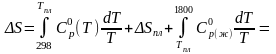
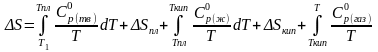
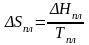 и
и