Материал: Курсовая синтез аммиака
Физико-химическое обоснование основных процессов производства целевого продукта
-
Равновесие и скорость процесса в системе
Синтез аммиака из элементов осуществляется по уравнению реакции
1/2N2+3/2H2 ↔ NH3; ΔH<0
Реакция обратимая, экзотермическая, характеризуется большим отрицательным энтальпийным эффектом (ΔH298=-91,96 кДж/моль) и при высоких температурах становится еще более экзотермической (ΔH725=-112,86 кДж/моль). По принципу Ле-Шателье при нагревании равновесие смещается влево, в сторону уменьшения выхода аммиака. Изменение энтропии в данном случае имеет тоже отрицательное значение (ΔS298=-198,13 кДж/(моль*К)), поэтому повышение температуры уменьшает вероятность протекания реакции [2]. Зависимость lnKp=f(1/T) представлена на рис. 2.
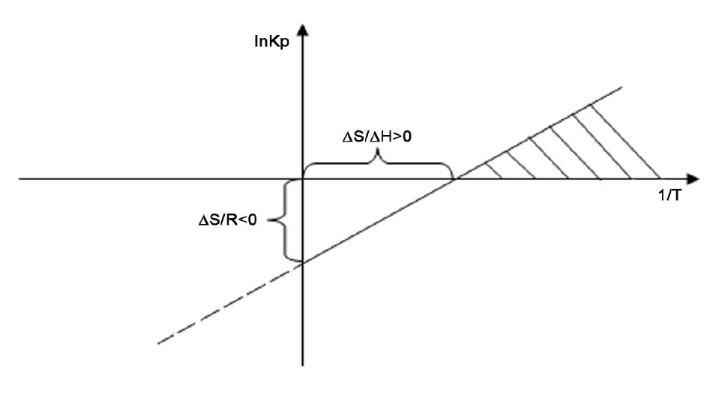
Рис.2. Зависимость lnKp = f (1/T) для реакции синтеза аммиака [8].
По графику видно, что реакция возможна (lnKp > 0) при температурах меньших ∆S0/∆H0 (заштрихованная часть), т.е. в области низких температур (T≈570 К и ниже).
Реакция синтеза аммиака протекает с уменьшением объема. По принципу Ле-Шателье в условиях равновесия содержание аммиака в смеси будет больше при высоком давлении, чем при низком [2].
Для реакции синтеза константа равновесия имеет вид:
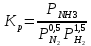
Качественная и количественная оценки условий термодинамического равновесия позволяют сделать вывод, что максимального выхода аммиака можно достичь, проводя процесс при высоком давлении и низких температурах. Однако даже при высоких температурах процесс практически неосуществим в гомогенной газовой фазе [2].
Синтез аммиака протекает с заметной скоростью только в присутствии катализатора, причем катализаторами данной реакции служат твердые вещества. Гетерогенно-каталитический процесс синтеза аммиака имеет сложный механизм, который может быть описан следующими стадиями:
1. Диффузия молекул азота и водорода к поверхности катализатора.
2. Хемосорбция молекул реагентов (адсорбатов) на поверхности катализатора.
3. Поверхностная химическая реакция с образованием неустойчивых промежуточных комплексов и взаимодействие между ними.
4. Десорбция продукта.
5. Диффузия продукта реакции (аммиака) от поверхности катализатора в газовую фазу.
Исследование кинетики и механизма реакции синтеза позволило сделать вывод, что лимитирующей стадией процесса является хемосорбция азота. Этот вывод можно описать механизмом синтеза аммиака сокращенной схемой:
N2+Z ↔ ZN2
ZN2+3H2 ↔ 2NH3 + Z
N2+3H2 ↔ 2NH3,
где Z – свободный центр поверхности катализатора; ZN2 – хемосорбированная частица (адсорбат) [2].
Скорость обратимой реакции получения аммиака из элементов на большинстве известных катализаторов описывается уравнением Темкина-Пыжева:
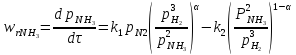
где
k1
и k2
– константы скоростей соответственно
образования и разложения аммиака;
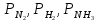 – парциальные давления соответственно
азота, водорода, аммиака, α – постоянная,
удовлетворяющая неравенству 0<α<1 и
характеризующая степень покрытия
поверхности катализатора азотом. При
проведении процесса при атмосферном
давлении и температуре от 400 до 500°С
для промышленных катализаторов величина
α = 0,5 [2,4]. Стоит отметить, что данное
уравнение хорошо согласуется с опытными
данными при давлениях от долей атмосферы
до 500 кгс/см2
(при внесении ряда поправок), но лишь в
том случае, если состав исходной смеси
не слишком отличается от равновесного
его состава [4].
– парциальные давления соответственно
азота, водорода, аммиака, α – постоянная,
удовлетворяющая неравенству 0<α<1 и
характеризующая степень покрытия
поверхности катализатора азотом. При
проведении процесса при атмосферном
давлении и температуре от 400 до 500°С
для промышленных катализаторов величина
α = 0,5 [2,4]. Стоит отметить, что данное
уравнение хорошо согласуется с опытными
данными при давлениях от долей атмосферы
до 500 кгс/см2
(при внесении ряда поправок), но лишь в
том случае, если состав исходной смеси
не слишком отличается от равновесного
его состава [4].
-
Выбор оптимальных условий процесса
Скорость реакции синтеза аммиака зависит от температуры, давления, состава реакционной смеси, катализатора и объемной скорости смеси. Оптимальными считаются такие значения параметров, при которых скорость процесса максимальна.
-
Давление и температура
С ростом давления наблюдаемая скорость процесса увеличивается.
И термодинамические, и кинетические факторы свидетельствуют в пользу проведения процесса при высоких давлениях (увеличивается равновесный выход, повышается скорость синтеза). Конденсация аммиака также улучшается при высоком давлении. Вместе с тем рост давления увеличивает расход электроэнергии на компрессию, повышает требования к машинам и аппаратам. При понижении давления упрощается аппаратурное оформление процесса, снижается расход энергии, но при этом увеличиваются размеры аппаратов, возрастают энергозатраты на циркуляцию газа и выделение аммиака, повышаются требования к чистоте синтез-газа [2].
Для определения оптимального давления синтеза была использована комплексная математическая модель агрегата синтеза аммиака. Опытные данные показали, что приведенные удельные и капитальные затраты с повышением давления уменьшаются. На основании проведенного анализа определено, что для современных схем наиболее эффективным является давление приблизительно 30 МПа (системы среднего давления) [2].
Поскольку присутствие инертных примесей равносильно снижению общего давления, то с увеличением содержания метана, аргона и гелия в смеси скорость реакции синтеза уменьшается.
Оптимальная температура синтеза Топт рассчитывается:
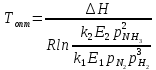
Из уравнения следует, что с увеличением содержания в циркуляционном газе аммиака и уменьшением содержания азотоводородной смеси оптимальная температура падает [2].
-
Состав азотоводородной смеси (авс)
Состав АВС выбирается как можно более близким к стехиометрическому, что обеспечивает максимальную степень превращения компонентов в аммиак. Так как степень превращения не превышает 20 – 40%, то процесс синтеза аммиака строится по циркуляционной схеме с отделением образующегося аммиака от непрореагировавшей АВС и возращением оставшейся части ее в реактор. Так как синтез аммиака идет с сокращением объема, то в циркулирующей АВС накапливаются инертные примеси (аргон, метан), что приводит к снижению выхода аммиака вследствие уменьшения концентраций азота и водорода в ней. Для устранения этого часть циркулирующей АВС периодически выводится из цикла в виде продувочного газа (отдувка). Для выделения образовавшегося аммиака из АВС ее охлаждают до температуры сжижения аммиака. При этом часть аммиака остается в АВС. Концентрация его зависит от температуры и изменяется от 1,5% об. при -20°С до 7,3% об. при +20°С при давлении около 30 МПа. При использовании водяного и аммиачного охлаждения это обеспечивает остаточное содержание аммиака в циркулирующей АВС 3 - 5% об. [2].
-
Катализатор
Высокую каталитическую активность в синтезе аммиака проявляют металлы VI, VII и VIII групп периодической системы. Наибольшей активностью обладают Fe, Ru, Re, Os. В промышленности нашли применение железные катализаторы, получаемые сплавлением оксидов железа с активаторами (промоторами) и последующими восстановлением оксидов железа. В качестве активаторов применяются оксиды кислотного и амфотерного характера – Al2О3, SiО2, TiО2 и др., а также оксиды щелочных и щелочноземельных металлов – К2О, Na2О, CaO, MgO и др.[2]. Отдельно взятые активаторы не оказывают ускоряющего действия на реакцию: при добавлении к железу Al2О3 увеличивается и становится более стабильной внутренняя поверхность зерен катализатора; введение К2О способствует повышению удельной активности катализатора [4].
До 90-ых годов катализатор для синтеза аммиака выпускался двух марок СА-1 (окислительный) и СА-1В (восстановительный). Последний представлял из себя восстановленную форму катализатора СА-1 и поставлялся потребителю в данном виде [4]. Процесс восстановления катализатора можно описать суммарным уравнением:
Fe3O4 + 4H2 → 3Fe + 4H2O; ΔH>0
Катализаторы синтеза аммиака необратимо отравляются сернистыми соединениями и хлором. Их концентрация в газе в сумме не должна превышать 5·10-5% [2].
Кислородосодержащие соединения (H2O, СО, СО2) и кислород, присутствующие в азотоводородной смеси, являются сильными каталитическими ядами, снижающими активность катализатора обратимо. Их отравляющее действие пропорционально содержанию в них кислорода. Если в составе свежего газа имеются кислородосодержащие примеси или масло, газ следует вводить в цикл перед вторичной конденсацией для удаления вредных соединений конденсирующимся NH3 [2].
В промышленности используются низкотемпературные катализаторы, разработанные ГИАП в начале 90-ых в СССР. Такие катализаторы содержат уменьшенное количество промотирующих оксидов алюминия, калия и кальция и дополнительное количество других промоторов, а именно оксидов магния, ванадия, кобальта, вольфрама и молибдена. Эти катализаторы имеют температуру зажигания 350°С и позволяют вести синтез аммиака в интервале температур 350–475°С, что позволяет осуществлять процесс синтеза при более низких давлениях [9].
-
Объемная скорость
С повышением объемной скорости возрастает съем аммиака с 1 м3 катализатора, однако при этом увеличивается количество циркулирующего газа в системе, на дожатие которого приходится расходовать дополнительную энергию, возрастают размеры промежуточных аппаратов и трубопроводов и повышается расход воды на охлаждение циркуляционного газа. На основе экономических расчетов рекомендуется поддерживать при давлении 32 МПа объемную скорость ω=22-25 тыс. ч-1 при наличии инертных газов и 30 тыс. ч-1 в их отсутствие.
-
Работа по линии оптимальных температур (лот)
Рис.
3. Зависимость выхода аммиака от
температуры процесса синтеза и объемной
скорости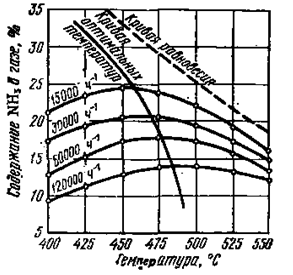
Для обеспечения максимального выхода аммиака процесс необходимо начинать при высокой температуре и по мере увеличения степени превращения понижать ее. Регулирование температуры и обеспечение автотермичности процесса обеспечивается с помощью теплообменников, расположенных в слое контактной массы и дополнительно, подачей части холодной АВС в контактную массу, минуя теплообменник (байпасное включение).
-
Охрана окружающей среды в производстве аммиака
Крупнотоннажное производство аммиака характеризуют следующие выбросы в окружающую среду:
1) газовые, содержащие в своем составе аммиак, оксиды азота и углерода и другие примеси.
Относительная концентрация токсичных примесей производства аммиака в виде оксида углерода и оксидов азота в отходящих газах невысока[2]. Для сокращения выбросов оксидов азота с дымовыми газами печи первичного риформинга на большинстве предприятий предусмотрено гомогенное восстановление оксидов азота до азота газообразным аммиаком. Процесс гомогенного восстановления оксидов азота протекает при температуре 930÷980°C по следующим реакциям [10]:
4NO + 4NH3 + O2 ↔ 4N2 + 6H2O
2NO2 + 4NH3 + O2 ↔ 3N2 + 6H2O
2) сточные воды, состоящие из конденсата, продуктов промывки реакторов и систем охлаждения.
В результате воздушного охлаждения и замены поршневых компрессоров турбокомпрессорами значительно уменьшается потребление воды на 1 т NН3, что приводит к существенному снижению количества сточных вод (примерно в 50 раз) [2].
3) низкопотенциальная теплота.
Для наиболее полного использования низкопотенциального тепла и получения пара высоких параметров прибегают к сжиганию небольшого количества добавочного природного газа. Но этот путь получения механической энергии связан с увеличением загрязненности воздушного бассейна дымовыми газами [2,4].
4) твердые отходы
В производстве аммиака образуются следующие виды отходов:
-
отработанные катализаторы, которые направляются на восстановление, реализуются как материальный ресурс или подлежат размещению один раз в 4–10 лет специальным организациям);
-
активированный уголь, который направляется на рекультивацию или захоронение.
-
отработанные масла применяют в производстве или отправляются на утилизацию [10].
Описание технологической схемы процесса
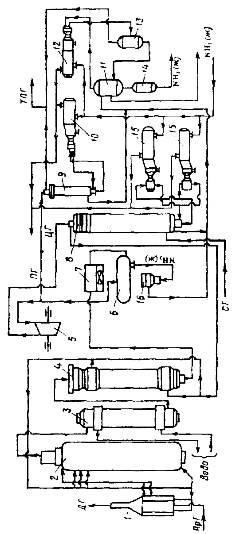
Свежая АВС после очистки метанированием поступает в центробежный компрессор, где сжимается до давления 32 МПа и после охлаждения в воздушном холодильнике (не показано на схеме) поступает в нижнюю часть конденсаторной колонны 8 для очистки от остаточных примесей СО2, H2O и следов масла. Свежий газ барботирует через слой сконденсировавшегося жидкого аммиака, освобождается при этом от водяных паров, следов СО и масла, насыщается аммиаком до 3-4% и смешивается с циркуляционным газом. Полученная смесь по трубам теплообменника конденсационной колонны направляется в межтрубное пространство выносного теплообменника 4, где нагревается до 185-195°С за счет теплоты газа, выходящего из колонны синтеза 2. Для дополнительного нагрева газа, поступающего в колонну синтеза 2, может использоваться подогреватель газа 1.
В колонне синтеза 2 газ проходит снизу вверх по кольцевой щели между корпусом колонны и кожухом насадки и поступает в межтрубное пространство внутреннего теплообменника, размещенного в горловине корпуса колонны синтеза. В теплообменнике циркуляционный газ нагревается до температуры начала реакции 400-440°С за счет теплоты конвертированного газа и, затем, последовательно проходит четыре слоя катализатора, в результате чего концентрация аммиака в газе повышается до 15%. Пройдя через центральную трубу, при температуре 500-515°С, азотоводородная смесь направляется во внутренний теплообменник, где охлаждается до 330°С. Дальнейшее охлаждение газовой смеси до 215°С осуществляется в трубном пространстве подогревателя питательной воды 3, в трубном пространстве выносного теплообменника 4 до 65°С за счет холодного циркуляционного газа, идущего по межтрубному пространству, и затем в аппаратах воздушного охлаждения 7 до 40°С, при этом часть аммиака конденсируется. Жидкий аммиак, сконденсировавшийся при охлаждении, отделяется в сепараторе 6, а затем смесь, содержащая 10-12% NH3, идет на циркуляционное колесо компрессора 5, где сжимается до 32 МПа.
Циркуляционный газ при температуре 50°С поступает в систему вторичной конденсации, включающую конденсационную колонну 8 и испарители жидкого аммиака 15. В конденсационной колонне газ охлаждается до 18°С и в испарителях за счет кипения аммиака в межтрубном пространстве до -5°С. Из трубного пространства испарителей смесь охлажденного циркуляционного газа и сконденсировавшегося аммиака поступает в сепарационную часть конденсационной колонны, где происходит отделение жидкого аммиака от газа и смешение свежей АВС с циркуляционным газом. Далее газовая смесь проходит корзину с фарфоровыми кольцами Рашига, где отделяется от капель жидкого аммиака, поднимается по трубам теплообменника и направляется в выносной теплообменник 4, а затем в колонну синтеза 2.
Жидкий аммиак из первичного сепаратора проходит магнитный фильтр 16, где из него выделяется катализаторная пыль, и смешивается с жидким аммиаком из конденсационной колонны 8. Затем его дросселируют до давления 4 МПа и отводят в сборник жидкого аммиака 11. Жидкий аммиак как продукт выводится частично непосредственно из сборника 11, частично через промежуточную дренажную емкость 14. В результате дросселирования жидкого аммиака до 4 МПа происходит выделение растворенных в нем газов H2, N2, O2, CH4. Эти газы, называемые танковыми, содержат 16-18% NH3. Поэтому таковые газы направляют в испаритель 12 с целью утилизации аммиака путем его конденсации при -25°С. Из испарителя танковые газы и сконденсировавшийся аммиак поступают в сепаратор 13 для отделения жидкого аммиака, направляемого в сборник жидкого аммиака 11.
Для поддержания в циркуляционном газе постоянного содержания инертных газов, не превышающего 10%, производится продувка газа после первичной конденсации аммиака (после сепаратора 6).
Продувочные газы содержат 8-9% NH3, который выделяется при температуре -25-30°С в конденсационной колонне 9 и испарителе 10 продувочных газов. Смесь танковых и продувочных газов после выделения аммиака используют как топливный газ.
Технологическая
схема блока синтеза аммиака агрегата
мощностью 1360 т/сут: 1
– подогреватель газа; 2 – колонная
синтеза аммиака; 3 – подогреватель
воды; 4 – выносной теплообменник; 5 –
циркуляционное колесо компрессора; 6
- сепаратор жидкого аммиака; 7 – блок
аппарата воздушного охлаждения; 8 –
конденсационная колонна; 9 - конденсационная
колонна продувочных газов; 10 – испаритель
жидкого аммиака на линии продувочных
газов; 11 – сборник жидкого аммиака;12 –
испаритель жидкого аммиака на линии
танковых газов; 13 – сепаратор; 14 –
промежуточная дренажая ёмкость; 15 –
испарители жидкого аммиака; 16 – магнитный
фильтр; ПрГ – природный газ; ДГ – дымовой
газ; ПГ – продувочный газ; СГ – свежий
газ; ЦГ – циркуляционный газ; ТПГ –
смесь танковых и продувочных газов.