Материал: Электронная структура атомов
где R = 1.09677*105 см-1 - постоянная Ридберга для водорода, m - уровень с которого переходит атом при излучении, n - уровень серии на который переходит атом.
Серия Лаймана — спектральная серия в спектре атома водорода, названная в честь американского физика Теодора Лаймана, открывшего эту серию в 1916 году. Данная серия образуется при переходах электронов с возбуждённых энергетических уровней на первый в спектре излучения и с первого уровня на все остальные при поглощении. Переход со второго энергетического уровня на первый обозначается греческой буквой α, с 3-го на 1-й — β и т. д. Для обозначения самой серии используется латинская буква L. Таким образом, полное обозначение спектральной линии, возникающей при переходе электрона со второго уровня на первый — Lα (произносится Лайман альфа).
Спектр серии Лаймана
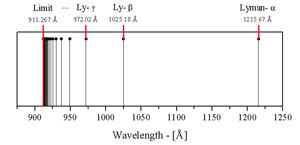
рис.1
Формула Ридберга для серии Лаймана выглядит следующим образом:
![]()
Где n (главное квантовое число) — натуральное число большее 2.
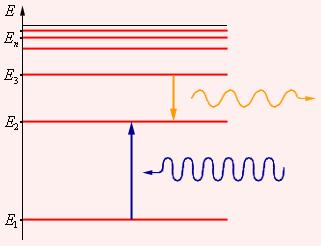
Энергетические уровни в атоме водорода
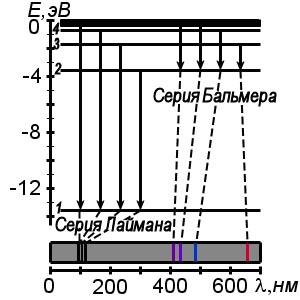
рис.2
Длины волн серии Лаймана
|
n |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
∞ |
|
Длина волны, нм |
121,6 |
102,5 |
97,2 |
94,9 |
93,7 |
93,0 |
92,6 |
92,3 |
92,1 |
91,9 |
91,15 |
Серия Бальмера – спектральная серия атома водорода, линии которой расположены в видимой и близкой к ультрафиолетовой областях спектра. Эта серия образуется при переходах между состояниями, одно из которых имеет главное квантовое число, равное двум.
Волновые числа n серии Бальмера определяются формулой Бальмера:
![]() ,
,
где n =
3, 4, 5, ..., R – постоянная
Ридберга. Линии серии Бальмера,
получающиеся при n =
3, 4, 5, ..., обозначаются соответственно ![]()
Оптический спектр свободного атома водорода получается при испускании или поглощении электромагнитных волн, что в свою очередь являются следствием переходов между уровнями энергии внешних электронов атома. Состояние атома с минимальной энергией Е1 называется основным. Если атом получит извне некоторое количество энергии, то, в зависимости от ее величины, он может перейти в одно из возбужденных состояний. При этом электрон оказывается на одном из уровней с номерами n = 2, 3, 4,… Такое состояние системы является неустойчивым. Через некоторое время электрон из возбужденного состояния переходит на уровень с меньшим значением энергии. Избыток энергии будет испущен в виде светового кванта. В конечном счете, атом возвращается в основное состояние.
Рис. 1 иллюстрирует образование спектральных серий атома водорода при переходе электрона с высоких стационарных орбит на более низкие.
Стационарные орбиты атома водорода и образование спектральных серий
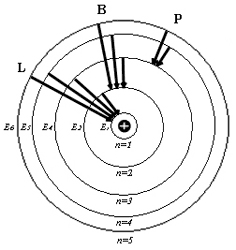
Рис. 1
L – серия Лаймана, B – серия Бальмера, P – серия Пашена
На рис. 2 изображена диаграмма энергетических уровней атома водорода и указаны переходы, соответствующие различным спектральным сериям. Для первых пяти линий серии Бальмера в видимой части спектра указаны длины волн.
Энергетические уровни атома водорода
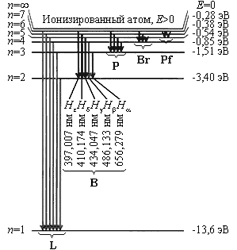
Рис. 2
L – серия Лаймана, B – серия Бальмера, P – серия Пашена , Br – серия Брэкета, Pf – серия Пфунда
Благодаря распространенности водорода во Вселенной серия Бальмера наблюдается в спектрах большинства космических объектов.
Анализ интенсивностей линий серии Бальмера позволяет судить о температурах звезд, так как для получения интенсивных линий необходимо, чтобы в их образовании участвовало достаточное количество неионизованных возбужденных атомов водорода. Такие условия выполняются в атмосферах звезд спектрального класса А с температурой T~104 К (в более холодных звездах мало возбужденных атомов водорода, а в горячих звездах почти все атомы водорода ионизованы). Сравнивая контуры линий серии Бальмера, получают информацию о плотностях звездных атмосфер.
Бальмер (Balmer) Иоганн Якоб (1825–1898), швейцарский физик и математик, эмпирически установил (1885), что длины волн видимой части спектра атома водорода связаны между собой простой зависимостью (1), позволяющей определить длины волн всех линий спектральной серии водорода. Серия Бальмера была впервые обнаружена в спектре Солнца.
Глава 6. Физика атома и атомного ядра
|
|
|
|
|
|
Планетарная модель атома, предложенная Резерфордом, – это попытка применения классических представлений о движении тел к явлениям атомных масштабов. Она оказалась несостоятельной. Классический атом неустойчив. Электроны, движущиеся по орбите с ускорением, должны неизбежно упасть на ядро, растратив всю энергию на излучение электромагнитных волн (рис. 6.2.1).
|
|
|
Рисунок 6.2.1. Неустойчивость классического атома |
Следующий шаг в развитии представлений об устройстве атома в 1913 году сделал выдающийся датский физик Н. Бор. Проанализировав всю совокупность опытных фактов, Бор пришел к выводу, что при описании поведения атомных систем следует отказаться от многих представлений классической физики. Он сформулировал постулаты, которым должна удовлетворять новая теория о строении атомов.
Первый постулат Бора (постулат стационарных состояний) гласит: атомная система может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная энергия En. В стационарных состояниях атом не излучает.
Этот постулат находится в явном противоречии с классической механикой, согласно которой энергия движущегося электрона может быть любой. Он находится в противоречии и с электродинамикой, так как допускает возможность ускоренного движения электронов без излучения электромагнитных волн. Согласно первому постулату Бора, атом характеризуется системой энергетических уровней, каждый из которых соответствует определенному стационарному состоянию (рис. 6.2.2). Механическая энергия электрона, движущегося по замкнутой траектории вокруг положительно заряженного ядра, отрицательна. Поэтому всем стационарным состояниям соответствуют значения энергии En < 0. При En ≥ 0 электрон удаляется от ядра, т. е. происходит ионизация. Величина |E1|называется энергией ионизации. Состояние с энергией E1 называется основным состоянием атома.
|
|
|
Рисунок 6.2.2. Энергетические уровни атома и условное изображение процессов поглощения и испускания фотонов |
Второй постулат Бора (правило частот) формулируется следующим образом: при переходе атома из одного стационарного состояния с энергией En в другое стационарное состояние с энергией Em излучается или поглощается квант, энергия которого равна разности энергий стационарных состояний:
|
где h – постоянная Планка. Отсюда можно выразить частоту излучения:
|
|
Второй постулат Бора также противоречит электродинамике Максвелла, так как частота излучения определяется только изменением энергии атома и никак не зависит от характера движения электрона.
Теория Бора при описании поведения атомных систем не отвергла полностью законы классической физики. В ней сохранились представления об орбитальном движении электронов в кулоновском поле ядра. Классическая ядерная модель атома Резерфорда в теории Бора была дополнена идеей о квантовании электронных орбит. Поэтому теорию Бора иногда называют полуклассической.
![]()
|
|
|
Модель. Постулаты Бора |
Третий постулат Н. Бора определяет правила квантования стационарных орбит. Борпредположил, что момент импульса электрона, вращающегося на стационарной орбите в атоме водорода, может принимать только дискретные значения, кратные постоянной Планка. Для круговых орбит правило квантования Бора записывается в виде:
|
|
где me – масса электрона, υ – его орбитальная скорость, rn – радиус n-ой стационарной орбиты. Целое число n называется квантовым числом.
Правило квантования орбит по Бору получило наглядную интерпретацию в теории де Бройля, высказавшего гипотезу о наличии у электрона волновых свойств (1924 г.). Согласно де Бройлю электрону (и любому другому микрообъекту) соответствует волновой процесс с длиной волны
|
|
где p – импульс электрона.
В применении к орбитальному движению электрона на стационарной круговой орбите в атоме водорода из правила квантования Бора вытекает соотношение
|
nλ = 2πrn. |
Это означает, что длина волны де Бройля целое число раз укладывается на длине стационарной круговой орбиты электрона, то есть стационарная орбита соответствует круговой стоячей волне де Бройля на длине орбиты.
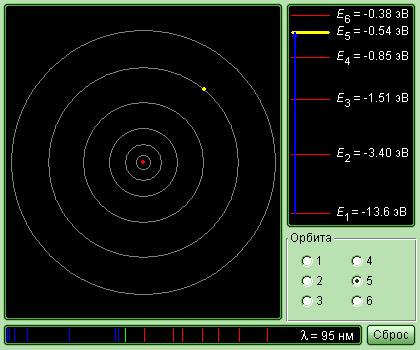
Компьютерная модель является качественной иллюстрацией идеи де Бройля возникновения стоячих волн на стационарных орбитах.
Модель позволяет, плавно изменяя радиус, выбирать стационарные орбиты, на длине которых укладывается целое число длин волн де Бройля и образуется стоячая волна.
Компьютерная модель на примере орбит с квантовыми числами n = 2, 3 и 4 иллюстрирует закономерность, которой подчиняются радиусы стационарных круговых орбит в атоме водорода. Согласно теории Бора
|
rn = n2r1, |
где r1 = 5,29·10–11 м – радиус первой боровской орбиты.
Энергия ионизации — количество энергии, необходимое для отрыва электрона от невозбужденного атома.
Энергия ионизации атома выражается в килоджоулях на моль (кДж/моль); допускается внесистемная единица электрон-вольт на моль (эВ/моль).
Для многоэлектронных атомов рассматриваются разные энергии ионизации, которые соответствуют отрыву первого, второго и так далее электронов. Чем больше число оторванных электронов, тем выше положительный заряд иона, и тем труднее их отрывать, поэтому энергия ионизации для каждого последующего электрона в этом случае возрастает.
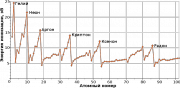
![]()
График энергии ионизации элеметов
Энергия ионизации атома зависит от его электронной конфигурации. В частности, завершенные электронные слои обнаруживают повышенную устойчивость. Поскольку электронная конфигурация изменяется периодически, энергия ионизации также изменяется периодически (см. рисунок).
|
|
|
|