Материал: Электродные равновесия
Давление газообразного водорода можно точно
измерить барометром. Однако в большинстве конструкций ячеек водород
пропускается через раствор в виде пузырьков. Поэтому при вычислении потенциала
следует использовать эффективное давление газообразного водорода. Для водных
растворов эффективное давление можно рассчитать по эмпирическому уравнению
![]() (27)
(27)
где ![]() -
барометрическое давление (мм рт. ст.),
-
барометрическое давление (мм рт. ст.), ![]() -
давление паров раствора (мм рт. ст.) и h - глубина погружения распылителя
водорода (мм). Водородный электрод можно также применять во многих неводных и
частично водных растворах, особенно в спиртовых.[9]
-
давление паров раствора (мм рт. ст.) и h - глубина погружения распылителя
водорода (мм). Водородный электрод можно также применять во многих неводных и
частично водных растворах, особенно в спиртовых.[9]
Диффузионный потенциал
В электрохимических цепях на границах раздела
между неодинаковыми растворами электролитов возникают скачки потенциала. Для
двух растворов с одинаковым растворителем такой скачок потенциала называется
диффузионным потенциалом. В месте контакта двух растворов электролита КА,
отличающихся друг от друга концентрацией, происходит диффузия ионов из раствора
1, более концентрированного, в раствор 2, более разбавленный. Обычно скорости
диффузии катионов и анионов различны. Допустим, что скорость диффузии катионов
больше скорости диффузии анионов. За некоторый промежуток времени из первого
раствора во второй перейдет больше катионов, чем анионов. В результате этого
раствор 2 получит избыток положительных зарядов, а раствор 1 - отрицательных.
Поскольку растворы приобретают электрические заряды, то скорость диффузии
катионов уменьшается, анионов увеличивается, и с течением времени эти скорости
становятся одинаковыми. В стационарном состоянии электролит диффундирует как
единое целое. При этом каждый раствор имеет заряд, и разность потенциалов,
установившаяся между растворами, соответствует диффузионному потенциалу. Расчет
диффузионного потенциала в общем случае затруднителен. С учетом некоторых
допущений Планком и Гендерсоном выведены формулы для расчета φд
. Так, например, при контакте двух растворов одного и того же электролита с
различной активностью (α1![]() α2)
α2)
![]() (28)
(28)
где ![]() и
и
![]() -
предельные молярные электрические проводимости ионов. Величина φд
мала и в большинстве случаев не превышает нескольких десятков милливольт.
-
предельные молярные электрические проводимости ионов. Величина φд
мала и в большинстве случаев не превышает нескольких десятков милливольт.
ЭДС электрохимической цепи с учетом
диффузионного потенциала
![]() ……………………………….(29)
……………………………….(29)
Уравнение (29) используется для расчета ![]() (или
(или
![]() )
по результатам измерения Е, если известны
)
по результатам измерения Е, если известны ![]() (или
(или
![]() )
и
)
и ![]() .
Поскольку определение диффузионного потенциала связано с существенными
экспериментальными трудностями, то при измерениях ЭДС удобно устранить с
помощью солевого мостика. Последний содержит концентрированный раствор
электролита, молярные электрические проводимости ионов которого приблизительно
одинаковы (KCl, KNO3). Солевой мостик, в котором содержится, например, КС1,
располагают между растворами электрохимической цени, и вместо одной жидкостной
границы в системе возникают две. Так как концентрация ионов в растворе КС1
значительно выше, чем в соединяемых им растворах, то практически только ионы K+
и С1- диффундируют через жидкостные границы, на которых возникают очень малые и
обратные по знаку диффузионные потенциалы. Их суммой можно пренебречь.[1],[7]
.
Поскольку определение диффузионного потенциала связано с существенными
экспериментальными трудностями, то при измерениях ЭДС удобно устранить с
помощью солевого мостика. Последний содержит концентрированный раствор
электролита, молярные электрические проводимости ионов которого приблизительно
одинаковы (KCl, KNO3). Солевой мостик, в котором содержится, например, КС1,
располагают между растворами электрохимической цени, и вместо одной жидкостной
границы в системе возникают две. Так как концентрация ионов в растворе КС1
значительно выше, чем в соединяемых им растворах, то практически только ионы K+
и С1- диффундируют через жидкостные границы, на которых возникают очень малые и
обратные по знаку диффузионные потенциалы. Их суммой можно пренебречь.[1],[7]
Строение двойного электрического слоя
Переход заряженных частиц через границу раствор - металл сопровождается возникновением на этой границе двойного электрического слоя (д.э.с) и скачка потенциала. Двойной электрический слой создается электрическими зарядами, находящимися на металле, и ионами противоположного заряда (противоионами), ориентированными в растворе у поверхности электрода.[1]
В формировании ионной обкладки д.э.с. принимают участие как электростатические силы, под влиянием которых противоионы подходят к поверхности электрода, так и силы теплового (молекулярного) движения, в результате действия которых д.э.с. приобретает размытое, диффузное строение. Кроме того, в создании двойного электрического слоя на границе металл - раствор существенную роль играет эффект специфической адсорбции поверхностно-активных ионов и молекул, которые могут содержаться в электролите.
Строение двойного электрического слоя в
отсутствие специфической адсорбции. Под строением д.э.с. понимают распределение
зарядов в его ионной обкладке. Упрощенно ионную обкладку можно условно разделить
на две части: 1) плотную, или гельмгольцевскую, образованную ионами,
практически вплотную подошедшими к металлу; 2) диффузную, созданную ионами,
находящимися на расстояниях от металла, превышающих радиус сольватированного
иона (рис. 1). Толщина плотной части порядка 10-8 см, диффузной - 10-7-10-3 см.
Согласно закону электронейтральности
![]() ……………………………..(30)
……………………………..(30)
где ![]() ,
,
![]() ,
,![]() ,
,![]() - плотность заряда со стороны металла, со стороны раствора, в плотной
диффузионной части д.э.с. соответственно. [1]
- плотность заряда со стороны металла, со стороны раствора, в плотной
диффузионной части д.э.с. соответственно. [1]
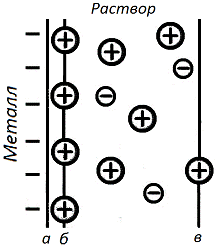
Рис.1. Строение двойного электрического слоя на
границе раствор - металл.: аб - плотная часть ;бв - диффузная часть
Распределение потенциала в ионной обкладке
двойного электрического слоя, отражающее его строение, представлено на рис.2.
Величина скачка потенциала φ
на границе раствор - металл соответствует сумме величин падения потенциала ![]() в
плотной части д.э.с и
в
плотной части д.э.с и ![]() - в диффузной.
Строение д.э.с. определяется общей концентрацией раствора, С ее ростом диффузия
противоиоиов от поверхности металла в массу раствора ослабляется, в результате
чего сокращаются размеры диффузной части. Это приводит к изменению
- в диффузной.
Строение д.э.с. определяется общей концентрацией раствора, С ее ростом диффузия
противоиоиов от поверхности металла в массу раствора ослабляется, в результате
чего сокращаются размеры диффузной части. Это приводит к изменению ![]() -потенциала.
В концентрированных растворах диффузная часть практически отсутствует, и
двойной .электрический слой подобен плоскому конденсатору, что соответствует
модели Гельмгольца, впервые предложившего теорию строения д.э.с..
-потенциала.
В концентрированных растворах диффузная часть практически отсутствует, и
двойной .электрический слой подобен плоскому конденсатору, что соответствует
модели Гельмгольца, впервые предложившего теорию строения д.э.с..
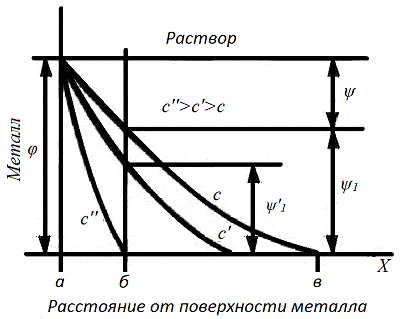
Рис.1. Распределение потенциала в ионной
обкладке при различной концентрации раствора: аб - плотная часть ; бв -
диффузная часть; φ - разность
потенциалов между раствором и металлом; ψ,ψ1
- падение потенциала в плотной и диффузной частях д.э.с.
Строение двойного электрического слоя в условиях
специфической адсорбции. Адсорбция - концентрирование вещества из объема фаз на
поверхности раздела между ними - может быть вызвана как электростатическими
силами, так и силами межмолекулярного взаимодействия и химическими. Адсорбцию,
вызванную силами неэлектростатического происхождения, принято называть
специфической. Вещества, способные адсорбироваться на границе раздела фаз,
называются поверхностно-активными (ПАВ). К ним относятся большинство анионов,
некоторые катионы и многие молекулярные соединения. Специфическая адсорбция
ПАВ, содержащегося в электролите, влияет на структуру двойного слоя и величину ![]() -потенциала
(рис.3). Кривая 1 соответствует распределению потенциала в двойном электрическом
слое в отсутствие ПАВ в растворе. Если раствор содержит вещества, дающие при
диссоциации поверхностно-активные катионы, то за счет специфической адсорбции
поверхностью металла катионы будут входить в плотную часть двойного слоя,
увеличивая ее положительный заряд (кривая 2). В условиях, способствующих
усилению адсорбции (например, увеличение концентрации адсорбата), в плотной
части может оказаться избыточное количество положительных зарядов по сравнению
с отрицательным зарядом металла (кривая 3). По кривым распределения потенциала
в двойном слое видно, что
-потенциала
(рис.3). Кривая 1 соответствует распределению потенциала в двойном электрическом
слое в отсутствие ПАВ в растворе. Если раствор содержит вещества, дающие при
диссоциации поверхностно-активные катионы, то за счет специфической адсорбции
поверхностью металла катионы будут входить в плотную часть двойного слоя,
увеличивая ее положительный заряд (кривая 2). В условиях, способствующих
усилению адсорбции (например, увеличение концентрации адсорбата), в плотной
части может оказаться избыточное количество положительных зарядов по сравнению
с отрицательным зарядом металла (кривая 3). По кривым распределения потенциала
в двойном слое видно, что ![]() -потенциал
изменяется при адсорбции катионов и может иметь знак, противоположный знаку
потенциала электрода.
-потенциал
изменяется при адсорбции катионов и может иметь знак, противоположный знаку
потенциала электрода.
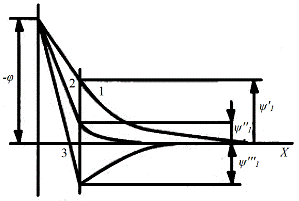
Рис.3. Влияние поверхностноактивных катионов на
распределение потенциала в ионной обкладке двойного электрического слоя при
отрицательном заряде электрода
Эффект специфической адсорбции наблюдается и на незаряженной поверхности металла, т.е. в тех условиях, когда обмен ионами между металлом и раствором отсутствует. Адсорбированные ионы и соответствующие противоионы образуют двойной электрический слой, расположенный в непосредственной близости к металлу со стороны раствора. Ориентированные около поверхности металла адсорбированные полярные молекулы (ПАВ, растворителя) также создают двойной электрический слой. Скачок потенциала, отвечающий двойному электрическому слою при незаряженной поверхности металла, называется потенциалом нулевою заряда (ц.н.з.).[1],[5],[11]
Потенциал нулевого заряда определяется природой металла и составом электролита. При адсорбции катионов п.н.з. становится более положительным, анионов - более отрицательным. Потенциал нулевого заряда является важной электрохимической характеристикой электродов. При потенциалах, близких к п.н.э., некоторые свойства металлов достигают предельных значений: велика адсорбция ПАВ, максимальна твердость, минимальна смачиваемость растворами электролитов и др.
Результаты исследований в области теории
двойного электрического слоя позволили более широко рассмотреть вопрос о
природе скачка потенциала на границе раствор - металл. Этот скачок обусловлен
следующими причинами: переходом заряженных частиц через границу раздела (![]() ),
специфической адсорбцией ионов (
),
специфической адсорбцией ионов (![]() ) и полярных
молекул (
) и полярных
молекул (![]() ).
Гальвани-потенциал на границе раствор - металл можно рассматривать как сумму
трех потенциалов:
).
Гальвани-потенциал на границе раствор - металл можно рассматривать как сумму
трех потенциалов:
![]() ……………………………..(31)
……………………………..(31)
В условиях, при которых обмен заряженными
частицами между раствором и металлом, а также адсорбция ионов не происходят,
все же остается скачок потенциала, вызванный адсорбцией молекул растворителя, -
![]() .
Гальвани-потенциал
.
Гальвани-потенциал ![]() может быть равен
нулю только тогда, когда
может быть равен
нулю только тогда, когда ![]() ,
,![]() и
и ![]() компенсируют
друг друга.
компенсируют
друг друга.
В настоящее время нет прямых экспериментальных и расчетных методов определения величин отдельных скачков потенциала на границе раздела раствор - металл. Поэтому вопрос об условиях, при которых скачок потенциала обращается в нуль (так называемый абсолютный нуль потенциала), остается пока открытым. Однако для решения большинства электрохимических задач знание отдельных скачков потенциалов не обязательно. Достаточно пользоваться значениями электродных потенциалов, выраженными в условной, например водородной, шкале.
Строение двойного электрического слоя не
отражается на термодинамических свойствах равновесных электродных систем. Но
при протекании электрохимических реакций в неравновесных условиях ионы
испытывают влияние электрического поля двойного слоя, что приводит к изменению
скорости электродного процесса.[1]
Классификации электрохимических цепей и
обратимых электродов
Электрохимические цепи обычно классифицируют по двум признакам: 1) по источнику электрической энергии (физические, концентрационные, химические); 2) по наличию или отсутствию в цепи границы двух различных растворов (соответственно, цепи с переносом и без переноса).[4]
В физических цепях источником электрической энергии служит различие в физическом состоянии двух одинаковых по своему химическому составу электродов. Эти электроды погружены в один и тот же раствор и при работе цепи электрод, находящийся в менее устойчивом состоянии, переходит в более устойчивое состояние. Физические цепи - цепи без переноса - подразделяются на аллотропические и гравитационные.
Аллотропические цепи - это цепи, в которых менее устойчивое состояние одного электрода обусловлено тем, что он изготовлен из метастабильной модификации данного материала.
Гравитационные цепи были впервые реализованы
российским электрохимиком Р.А.Колли. Гравитационная цепь из двух ртутных
электродов в растворе Hg(NO3)2 представлена на рис. 4. Левый электрод с более
высоким уровнем ртути обладает большим запасом потенциальной энергии по
сравнению с правым электродом. Этот избыток потенциальной энергии в расчете на
1 г-экв металлической ртути составляет ![]() ,
где
,
где ![]() -
молекулярная масса ртути;
-
молекулярная масса ртути; ![]() - ускорение силы
тяжести;
- ускорение силы
тяжести; ![]() -
разность уровней ртути. При работе цепи на левом электроде происходит
растворение ртути:
-
разность уровней ртути. При работе цепи на левом электроде происходит
растворение ртути:
![]()
а на правом, наоборот, разряд ионов ![]() :
:
![]()
В результате этих двух электродных процессов
происходит перенос металлической ртути из левой части в правую, который
направлен на выравнивание уровней ртути. При этом перенос 1 г-экв ртути
соответствует прохождению через систему 1 фарадея и электрической работе EF.
Поскольку источником этой энергии является потенциальная энергия ![]() ,
то ЭДС гравитационной цепи
,
то ЭДС гравитационной цепи
![]() …………………………………………(32)
…………………………………………(32)
Из уравнения (32) при ![]() =1м
получаем:
=1м
получаем:
![]()
Эксперимент подтверждает этот результат. Из-за
столь малых величин E гравитационные цепи не имеют практического значения. Они
представляют интерес как пример, иллюстрирующий законы превращения энергии.
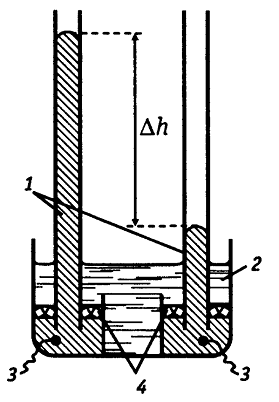
Рис.4. Схема гравитационной электрохимической цепи:
-ртуть; 2-раствор соли ртути; 3-впаянные в
стекло токоотводы; 4-керамические диафрагмы, проницаемые для ионов ![]() и
непроницаемые для металлической ртути
и
непроницаемые для металлической ртути
В концентрационных цепях оба электрода идентичны как по физическому состоянию, так и по химической природе участников окислительно-восстановительных процессов; они отличаются только концентрацией компонентов Ох или Red. Источником электрической энергии является разность свободных энергий Гиббса, обусловленная различными активностями одних и тех же химических компонентов. Концентрационные цепи можно приготовить из амальгам разных концентраций в одном и том же растворе; из одинаковых электродов первого, второго или третьего рода, находящихся в растворах разной концентрации; из одинаковых газовых электродов, работающих при разных давлениях газов. Различают концентрационные цепи без переноса, т.е. без границы двух растворов, и с переносом, когда имеется такая граница.[4],[7]