Материал: Строение и свойства металлов и сплавов
При нагреве или охлаждении металла переход из одного состояния в другое происходит с возникновением или разрушением кристаллической решётки и сопровождается тепловым эффектом. Вследствие этого металлы переходят из одного состояния в другое при постоянных температурах, и на кривых охлаждения или нагрева наблюдаются температурные остановки (см. рис.1).
Тпл - температура плавления металла;
Ткр - температура кристаллизации металла.
Участки 1-2 и 4-5 - переход металла из одного состояния в другое.
В т.1 происходит разрушение кристаллической
решётки. На участке 1-2 вся тепловая энергия идёт на её разрушение. Металл
переходит из твёрдого состояния в жидкое - процесс плавления. При этом
увеличивается объём металла на 2…6% за счёт увеличения расстояния между
атомами, силы взаимодействия при этом между атомами гораздо меньше, чем в
твёрдом металле.
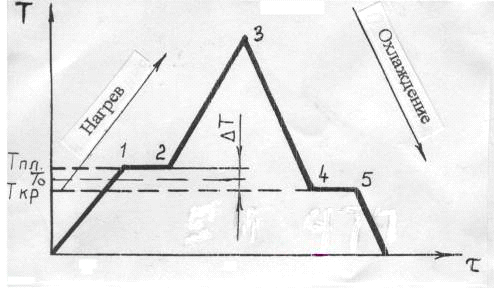
Рисунок 1
Для жидкости характерен ближний порядок, когда упорядоченное расположение атомов распространяется на небольшое расстояние. Этот порядок неустойчив. При температурах, близких к температуре плавления, в жидком металле наблюдаются области, в которых расположение атомов, близко к расположению атомов в твёрдом кристаллическом теле. Эти области называются фазовыми флуктуациями. Наиболее крупные флуктуации при определённых условиях могут стать зародышами кристаллов (центрами кристаллизации). Чтобы начался процесс кристаллизации необходимо переохладить металл ниже температуры плавления.
∆Т= Тпл -Ткр - тепловой гистерезис (несовпадение температуры плавления и температуры кристаллизации). Величина переохлаждения определяется природой металла, наличием примесей в металле, скоростью охлаждения (рис. 2). Если примесей мало, то металл надо значительно охладить.
Рисунок 2
Переход металла из жидкого состояния в твёрдое
(процесс кристаллизации) связан с возникновением кристаллической решётки. Этот
процесс происходит при постоянной температуре, что обусловлено выделением
скрытой теплоты кристаллизации (участок 4-5 на рис. 1).
.1 Энергетические условия процесса
кристаллизации
В природе все процессы идут в сторону уменьшения
энергии системы. Состояние системы определяется особой функцией - свободной
энергией.
F = U
- TS,
где F - свободная энергия системы;- внутренняя энергия системы;
Т - температура;- энтропия.
С увеличением температуры свободная энергия
жидкого Fж и твёрдого Fтв тела уменьшается (рис. 3).
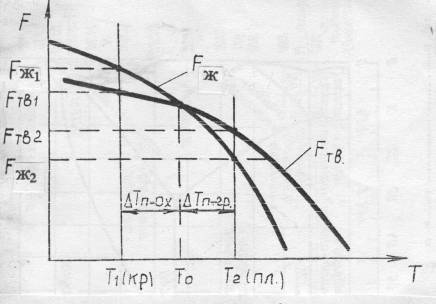
Рисунок 3
При Т0 Fтв = Fж - энергетически равноценны твёрдое и жидкое состояние вещества. Поэтому процессы плавления и кристаллизации происходить не будут (динамическое равновесие).
При Т1 Fтв1 < Fж1 - энергетически выгодно твердое состояние.
При Т2 Fж2 < Fтв2 - энергетически выгодно жидкое состояние.
Для начала кристаллизации вещество необходимо охладить ниже Т0, а для плавления нагреть выше Т0.
∆ Тпереохлажд.=Т0-Т1 - степень переохлаждения,
∆ Тперегрева.=Т2-Т0
- степень перегрева.
.2 Механизмы процесса кристаллизации
Возникновение кристаллов на базе крупных фазовых флуктуаций в жидкостях называется самопроизвольным (спонтанным) процессом кристаллизации. Он состоит из двух элементарных процессов.
. Возникновение зародышей кристаллов (центров кристаллизации).
. Рост кристаллов из центров кристаллизации.
. Вокруг образовавшихся центров начинают расти кристаллы [6, рис. 9]. Растут кристаллы послойно, при свободном росте они имеют правильную геометрическую форму с плоскими гранями. При соприкосновении кристаллов правильная форма нарушается. Кристаллы неправильной формы называются зёрнами.
В процессе кристаллизации возникают зародыши различной величины. Не любой зародыш способен к росту. Рост зародыша возможен только при условии, что он достиг определённой величины. Зародыш будет расти, если это приведёт к уменьшению свободной энергии системы.
Изменение свободной энергии тела в зависимости от размера образовавшегося кристаллического зародыша приведено на рис.4.
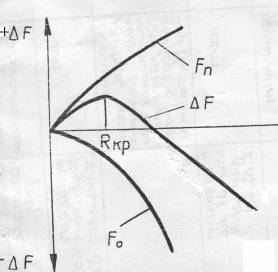
Рисунок 4
Свободная энергия системы при образовании зародыша, с одной стороны, уменьшается на величину F0 (объёмная энергия) вследствие перехода некоторого объёма жидкого металла в твёрдый, а с другой - возрастает на величину Fn (поверхностная энергия) в результате образования поверхности раздела. Суммарное изменение свободной энергии DF представляет кривую с максимумом при некотором определённом значении размера зародыша R=RКР. Минимальный размер зародыша, способного к росту, RКР называется критическим размером зародыша, а такой зародыш - устойчивым.
Величина критического зародыша зависит от величины переохлаждения. Чем больше величина переохлаждения, тем меньше размер устойчивого зародыша.
Величина переохлаждения влияет на скорость
зарождения кристаллов, а также и на скорость роста кристаллов (рис. 5).
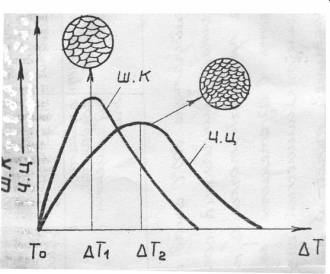
Рисунок 5
С.К. - скорость роста кристаллов; Ч.Ц. - число центров кристаллизации.
При увеличении переохлаждения до ∆Т1 наблюдается преимущественно увеличение скорости роста кристаллов, это приводит к возникновению крупных по величине кристаллов.
Дальнейшее увеличение степени переохлаждения до ∆Т2 приводит к увеличению числа центров кристаллизации.
Получение мелкозернистой структуры металла достигается на практике увеличением скорости охлаждения металла.
Самопроизвольное зарождение кристаллов в жидком металле весьма затруднительно. В реальных условиях в металле находится значительное количество примесей в виде не растворившихся частиц (оксиды, карбиды, нитриды). Эти частицы примесей при определённых условиях могут служить готовыми зародышами кристаллов. Для этого они должны быть изоморфны, т.е. иметь тип и параметры кристаллической решётки и размеры атомов, близкие к характеристикам металла. Для получения мелкозернистой структуры металла примеси (модификаторы) могут специально вводиться в металл. Различают модификаторы двух видов:
1 Инокуляторы - тугоплавкие частицы, служащие дополнительными центрами кристаллизации.
2 Ингибиторы - растворимые в металле,
поверхностно активные примеси, которые при кристаллизации покрывают тонким
слоем поверхность растущего кристалла и тормозят его рост.
6. Форма кристаллов. Строение металлического
слитка
Как правило, возникший в жидкости кристалл растёт в первую очередь в направлении минимального расстояния между атомами. Таким образом, в первую очередь вырастают оси первого порядка. Одновременно под определённым углом к оси первого порядка начинают расти оси второго порядка, от которых растут оси третьего порядка и т.д. В итоге вырастают кристаллы древовидной формы, получившие название дендритов. В зависимости от скорости охлаждения и условий теплоотвода их размеры и форма могут быть различны (могут быть равноосными или столбчатыми).
Металлический слиток образуется при кристаллизации металла в изложнице. Как правило, структура литого слитка состоит из трёх основных зон.
- поверхностный слой равноосных кристаллов, образованных в условиях высокой скорости охлаждения металла при соприкосновении жидкого металла с холодными стенками изложницы.
- зона столбчатых кристаллов с развитой осью первого порядка (транскристаллитов), образованных в условиях пониженной скорости охлаждения и перпендикулярном стенкам изложницы теплоотводе.
- зона крупных неориентированных равноосных кристаллов, образованных в условиях наименьшей скорости охлаждения и ненаправленного теплоотвода.
В верхней части слитка расположена концентрированная усадочная раковина - полость, не заполненная металлом, образованная вследствие объёмной усадки металла при кристаллизации 4.
Также вследствие объёмной усадки по оси слитка образуется рыхлость. В слитке под усадочной раковиной и в донной части наблюдается заметное повышение содержания примесей: C, S, Р (ликвирующих). Это приводит к падению механических свойств.
7. Строение сплавов
В технике чаще применяются не металлы, а металлические сплавы, так как они имеют лучший комплекс свойств по сравнению с металлом. Сплавы получают сплавлением элементов, спеканием (порошковая металлургия), диффузией.
Металлический сплав - сложная система на основе металла. Сплавы содержат два и более компонентов.
Фазой сплава называется однородная часть сплава, отделенная от других границей раздела, при переходе через которую состав или структура резко изменяются. Меняются и свойства. Металл в жидком состоянии представляет собой однородную фазу. То же касается и сплавов. При кристаллизации металла образуется новая твердая фаза. При этом металл находится в двухфазном состоянии - в жидком и твердом. В сплаве твердой фазой могут быть зерна чистого металла, твердого раствора, химического соединения.
В расплавленном состоянии многие металлы неограниченно растворимы друг в друге. При кристаллизации компоненты сплава могут иметь различный тип взаимодействия, что определяет образование различных видов сплавов. Различают три основных вида сплавов, образующихся при кристаллизации двух компонентов.
1 Механические смеси
2 Твердые растворы
Химические соединения
Механические смеси образуются, если компоненты растворимы в жидком и практически нерастворимы в твердом состоянии. Строение этих сплавов неоднородное - двухфазное. Такой сплав имеет два типа кристаллической решетки: решетку компонента А и решетку компонента В. Такие сплавы образуют элементы, значительно отличающиеся по свойствам.
Твердые растворы образуются в случае взаимной растворимости компонентов как в жидком так и в твердом состоянии. При этом один компонент (которого больше) сохраняет свою кристаллическую решетку, второй компонент в виде отдельных атомов располагается в решетке первого. Первый компонент называется растворителем, второй - растворимым.
Твердые растворы имеют однородное (однофазное) строение с решеткой растворителя.
Различают твердые растворы внедрения и замещения. В первом случае атомы растворимого проникают в межузельное пространство решетки растворителя.
Эти сплавы образуют металл с неметаллами, имеющими малые атомные радиусы (H, N, C, B). Эти элементы образуют ограниченные растворы, не превышающие 1…2%.
В твердых растворах замещения атомы растворимого располагаются в узлах решетки растворителя, замещая его атомы. Эти растворы могут быть как неограниченной растворимости, так и ограниченной. Неограниченные твёрдые растворы образуют изоморфные компоненты (имеющие близкие по типу и параметрам кристаллические решётки), атомные радиусы которых отличаются не более чем на 8…15%.
Растворимое занимает, как правило, произвольные места в узлах решетки растворителя, образуя неупорядоченные твердые растворы. В то же время при снижении температуры может наблюдаться перераспределение атомов растворимого с образованием упорядоченных твердых растворов. Структура таких растворов называется сверхструктурой, и они рассматриваются как промежуточные между твердыми растворами и химическими соединениями.
Химические соединения образуются в случае химического взаимодействия компонентов при кристаллизации. При этом строго определенное число атомов компонента А взаимодействует химически с определенным числом атомов компонента В, образуя одно химическое соединение типа A nB m.
Химические соединения имеют ряд особенностей:
1) соединение имеет свой тип кристаллической решетки, отличной от решеток компонентов;
2) свойства соединений отличны от свойств компонентов;
3) разложение соединения (диссоциация) происходит при постоянной температуре.
Кроме названных типов сплавов, существуют еще множество промежуточных фаз сплавов, которые не могут быть полностью отнесены ни к одному из названных типов.
Исследование сплавов производится на основе
диаграмм состояния сплавов.
8. Диаграммы состояния сплавов
Диаграмма состояния - это графическое изображение равновесных состояний сплавов рассматриваемой системы в зависимости от температуры и состава.
Диаграммы состояния строятся на основе термического анализа сплавов. При этом берутся отдельные сплавы рассматриваемой системы, медленно охлаждаются, и определяется скорость охлаждения (фиксируются температура и время). На основе этого анализа строят кривые охлаждения сплавов.
Линия сплава - вертикальная линия, проходящая через точку на оси концентрации, соответствующую составу сплава.
Линии диаграммы состояния представляют собой геометрическое место критических точек сплавов.
Линия АСВ - линия, определяющая геометрическое место точек (температур) начала кристаллизации сплавов - линия ликвидус.
Линия DCF - линия, определяющая геометрическое место точек (температур) конца кристаллизации сплавов - линия солидус.
Все превращения в сплавах подчиняются общему
закону равновесия - правилу фаз, которое выражается следующей зависимостью:
С=К-Ф+2,
где С - число степеней свободы системы (вариантность) - определяет условие равновесного существования сплава;
К - число компонентов сплава;
Ф - число фаз, находящихся в равновесии;
- внешние параметры, влияющие на систему
(температура, давление).
С=К-Ф+1, при Р = const.
С=0 - равновесие нонвариантное, то есть безвариантное (превращение происходит при постоянной температуре). Это соответствует температурной остановке на кривой охлаждения сплава, кривая охлаждения I - участок 1-1’ - C=1-2+1=0 - кристаллизация металла).
С=1 - моновариантное равновесие (превращение происходит в диапазоне температур). Это соответствует перегибу на кривой охлаждения (участок 1-2 на кривой охлаждения II - С=2-2+1=1 - кристаллизация сплава).
С=2 - бивариантное равновесие, т.е. равновесие
сохраняется при определённом изменении температуры и давления (например,
участок 0-1 на кривой охлаждения II - С=2-1+1=2 - охлаждение сплава до начала
кристаллизации).
.1 Диаграмма состояния сплавов, компоненты
которых практически нерастворимы в твердом состоянии (диаграмма 1го
рода)
Фазы в сплавах:1) жидкость (L); 2) кристаллы А; 3) кристаллы В.
Линия АСВ - линия ликвидус - начало кристаллизации сплавов, DCE - линия солидус - конец кристаллизации сплавов.
При охлаждении сплавов на линии АС из жидкости начинают выделяться кристаллы А, а на линии СВ - кристаллы В. На линии DCE из жидкости одновременно выделяются кристаллы А и В.
В диапазоне между линиями АСВ и DCE (температурный интервал 1-2) сплавы находятся в двухфазном состоянии: жидкость - кристаллы (L+A или L+B).
Для двухфазной области диаграммы состояния химический состав существующих фаз при данной температуре и их количество (по массе) можно определить с помощью правила отрезков:
1) если для определенной температуры сплава провести линию, параллельную оси концентрации (коноду) до пересечения с линиями, ограничивающими данную область, то проекции точек пересечения коноды покажут химический состав существующих фаз (точка в’ определяет состав жидкости, а точка q’ - состав кристаллов).