Материал: Лекция КОРОНАВИРУСЫ. Сем Coronaviridae. Характеристика новой коронавирусной инфекции
Лабораторная диагностика Лабораторная диагностика коронавирусной инфекции
1. Вирусологический (культуральный) метод
Культура клеток: культуры клеток почки африканской зеленой мартышки линии Vero и мышиных фибробластов (LLC-MK2).
Вирусы SARS-CoV и MERS-CoV обладают выраженным цитопатическим действием на клетки-мишени. Характерной чертой этого действия становится образование везикул, окруженных двойной мембраной. Такие везикулы являются аутофагосомами, которые не сливаются с лизосомами. Инфицирование многими коронавирусами может индуцировать образование синцития, обусловленного физиологической активностью вирусного шипикового белка при нейтральном рН.
SARS-CoV индуцирует некроптоз.
NB! Некроптоз - запрограммированная форма некроза, так как видны морфологические признаки, сходные с некрозом (набухание клеток с последующим разрывом плазматической мембраны), но при этом некроптоз имеет четкую систему регуляции.
Выраженным цитопатическим эффектом обладает белок Е вируса SARS-CoV, который формирует ионный канал в мембране комплекса Гольджи, что приводит к ионному дисбалансу в клетке и активации NLRP3-инфламмасомы.
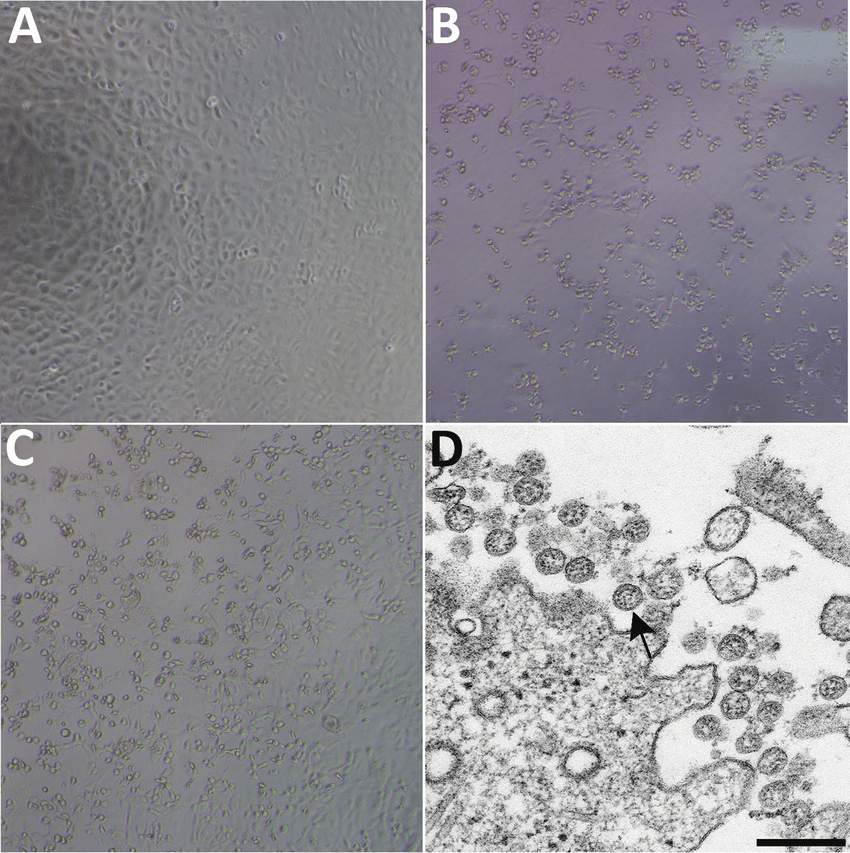
На рисунке А - неинфицированный монослой клеток культуры Vero, на рисунке В - культура клеток Vero инфицирована вирусами из назофарингеальной жидкости, рисунок С - культура клеток Vero инфицирована вирусами из орофарингеальной жидкости. Рисунок D - электронная микрофотография клеток культуры Vero, инфицированных коронавирусами (указаны стрелкой), слева внизу шкала - 200 нм.
2. Молекулярно-генетические методы
а) Полимеразная цепная реакция
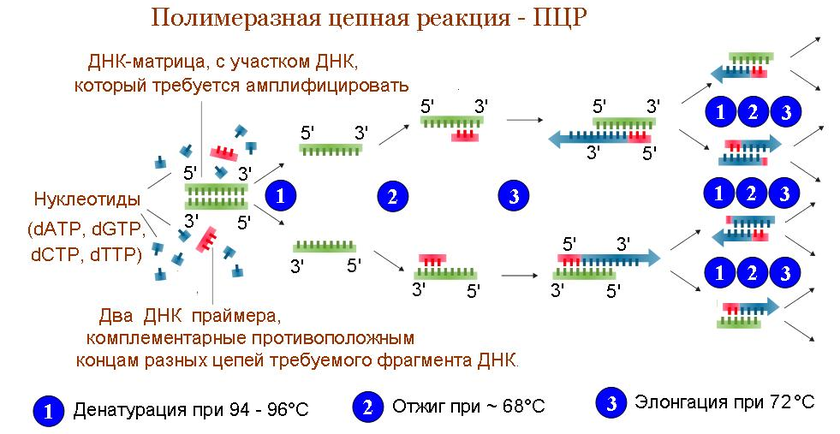
б) Петлевая изотермическая амплификация РНК
В отличие от метода полиразмерной цепной реакции, амплификация РНК происходит при постоянной температуре реакционной смеси, а также с использованием более производительных ферментов. За счет этого время исследования сократилось с 90 минут при классической ПЦР-диагностике до 15-20 минут.
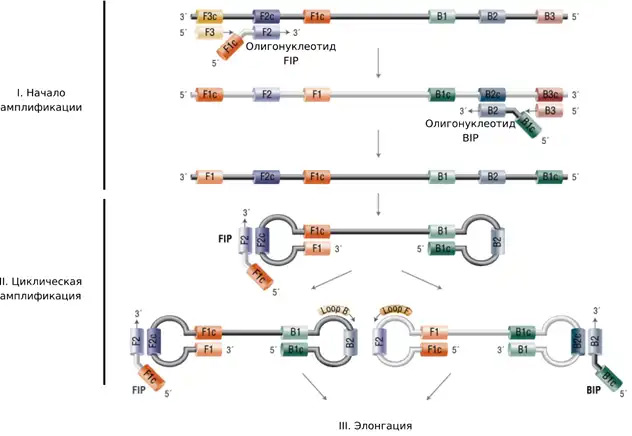
Метод основан на образовании шпилечных структур ДНК в ходе начала реакции, которые служат началом для последующих этапов амплификации. При этом происходит выпетливание определенных участков ДНК, к которым по правилу комплементарности подобраны олигонуклеотиды – две пары обязательных (F3 и B3, FIP и BIP) и пара дополнительных, увеличивающих скорость реакции («петлевые» олигонуклеотиды LF и LB).
Реакцию можно разделить на три этапа:
(i) начало амплификации, при котором происходит посадка олигонуклеотидов FIP и BIP и наработка гантелевидных ДНК-структур с двумя петлями;
(ii) циклическая амплификация — наработка ДНК-продуктов с гантелевидной структурой;
(iii) элонгация — наработка ДНК-продуктов различной длины и с множеством петель. За наработку ампликонов отвечает термостабильная Bst-полимераза, которая увеличивает количество участков ДНК до обнаруживаемого количества копий. Bst-полимераза обладает 5´ → 3´ полимеразной активностью, однако лишена 5´ → 3´ экзонуклеазной активностью. Кроме того, Bst-полимераза обладает способностью замещать ранее синтезированную нить ДНК, что позволяет использовать её в методе LAMP. Реакция проходит при температуре от 60 до 65 °C в течение 15–60 минут.
в) ПЦР «в реальном времени» («real-time PCR»)
При использовании такого метода можно прямо в ходе реакции наблюдать за накоплением продуктов ПЦР (по флуоресценции). Соответственно, для проведения ПЦР «в реальном времени» нужен специальный прибор, способный возбуждать и считывать флуоресценцию в каждой пробирке. Поскольку число копий в ходе ПЦР растет экспоненциально, так же растет и флуоресценция. Однако это продолжается недолго, поскольку в какой-то момент эффективность реакции начинает падать из-за постепенной инактивации полимеразы, нехватки каких-то компонентов и т.п.
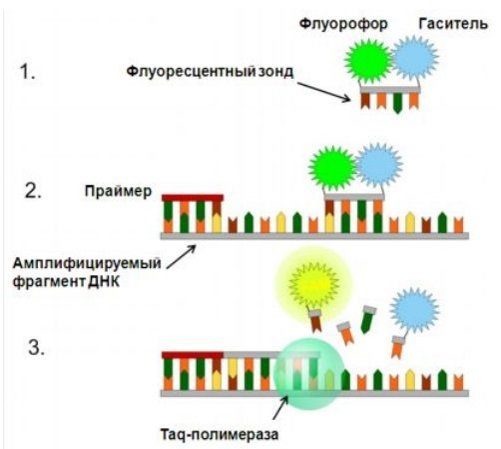
В состав реакционной смеси, наряду с праймерами и другими компонентами реакции, добавлены специальные флуоресцентные метки (зонды). Флуоресцентный зонд выполнен по той же технологии, что и праймер и отличается от него тем, что на одном его конце прикреплена флуоресцентная молекула (флуорофор), а на другом конце расположена специальная молекула-гаситель флуоресценции. За счёт близости гасителя, энергия поглощаемая флуорофором не вызывает флуоресцентного свечения, а целиком передаётся гасителю. При этом, при облучении смеси ультрафиолетом, флуоресцентный отклик полностью отсутствует. В ходе ПЦР при повышении температуры происходит денатурация ДНК с распадом на две половинки. Зонд вместе с праймерами присоединяется к комплементарному участку ДНК. В процессе восстановления и синтеза новой цепи ДНК, фермент ДНК-полимеразы расщепляет этот зонд и разрушает его. При этом флуорофор и гаситель освобождаются, расстояние между ними увеличивается и эффект гашения перестаёт работать. Теперь при облучении смеси ультрафиолетом, мы получим устойчивый флуоресцентный сигнал-отклик от флуорофора.
3. Методы детекции антигена - иммунохроматографические тесты
Тест на антиген является быстрой альтернативой ПЦР, не требующий лабораторного оборудования и специальных условий проведения.
Тест-система создана на основе анализа отделяемого из носоглотки в иммунохроматографическом анализе.
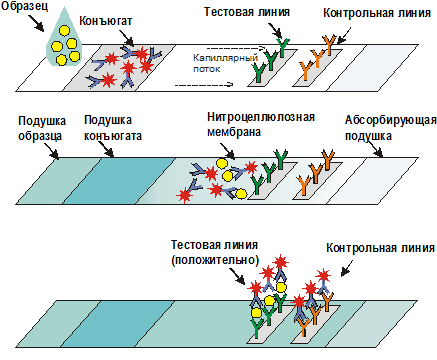
После внесения образца на подушку антигены образца взаимодействуют с антителами, конъюгированными с коллоидным золотом, нанесенными на подушку конъюгата. В результате образуется окрашенный комплекс антиген-антитело. Образовавшийся окрашенный иммунный комплекс движется под действием капиллярных сил вдоль нитроцеллюлозной мембраны и взаимодействует с иммобилизованными на Тестовой линии антителами. В результате появляется одна окрашенная розово-красная полоска. Не связавшиеся на тестируемой полосе антитела мигрируют далее вдоль нитроцеллюлозной мембраны и неизбежно взаимодействуют с иммобилизованными на Контрольной линии антигенами. В результате появляется вторая окрашенная полоска. Если анализ проведен правильно, Контрольная линия должна проявляться всегда, независимо от присутствия исследуемого антигена в образце биологической жидкости.
4. Методы детекции антител
Для детекции антител можно использовать иммуноферментный или иммунохроматографический анализ.
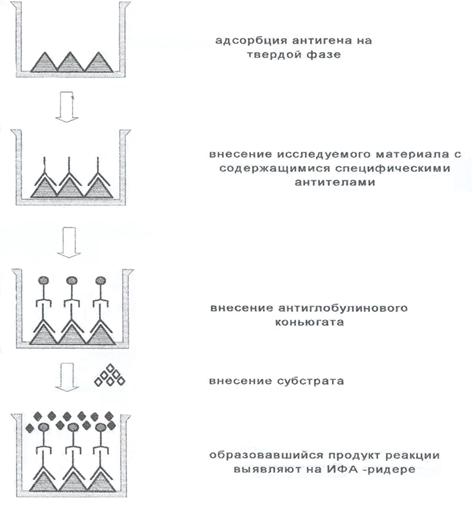
Иммуноферментный метод основан на специфическом связывании антитела с антигеном, при этом один из компонентов конъюгирован с ферментом, в результате реакции с соответствующим хромогенным субстратом образовывается окрашенный продукт, количество которого можно определить спектрофотометрически.
Схема непрямого варианта ИФА, который используется для детекции специфических IgG. В тест-системе использован рекомбинантный S-белок в качестве антигена, сорбированного на дне лунок.

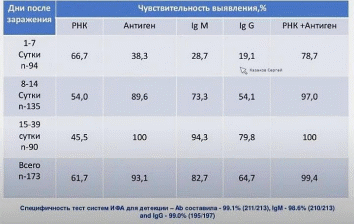
Чувствительность детекции рнк / Аг / Ат
Представлены результаты детекции РНК вируса или его антигенов либо антител к основным антигенам вируса в течение инфекционного процесса.
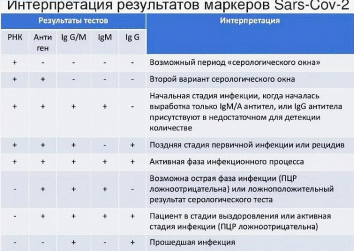
Интерпретация результатов лабораторных исследований
Неспецифическая профилактика
1. Предотвращение работы воздушно-капельного пути:
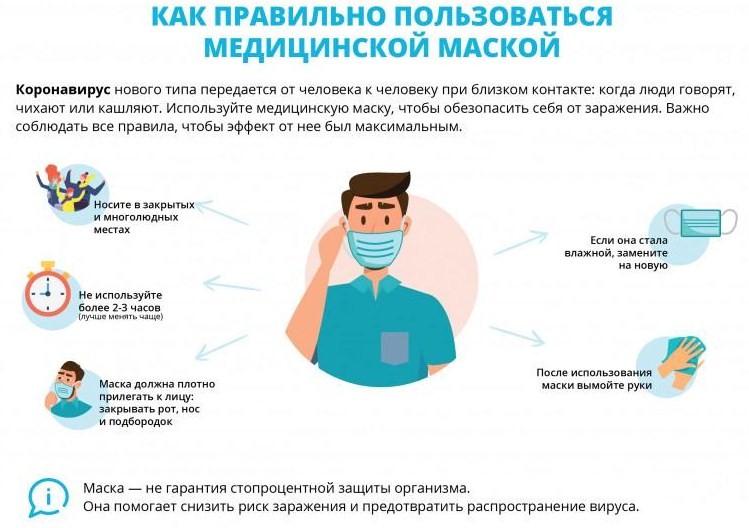
2. Комплекс санитарно-гигиенических и противоэпидемических мероприятий:

3. Дезинфекция в помещениях, обработка воздуха и т.д.

4. Профилактика для медицинских работников:

Специфическая профилактика 1
1. Векторная вакцина - Гам-КОВИД-Вак
Использование рекомбинантных вирусных векторов для доставки антигена при вакцинации позволяет индуцировать мощный гуморальный и клеточный иммунный ответ. Для формирования длительного иммунного ответа важно использовать двукратную иммунизацию, однако при использовании рекомбинантных вирусных векторов необходимо учитывать, что эффективность бустирующей иммунизации может быть снижена, поскольку после первичной иммунизации ответ развивается не только на целевой антиген, но и на компоненты вектора. В связи с этим перспективным подходом является использование схемы гетерологичной прайм-буст-вакцинации, когда для первичной и для вторичной иммунизации используют различные рекомбинантные вирусные векторы.
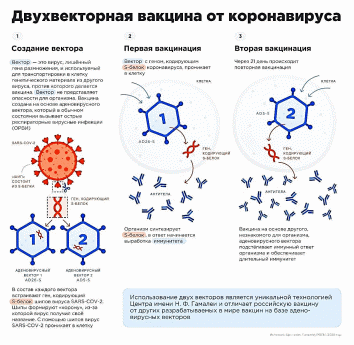
В России разработана комбинированная векторная вакцина для профилактики Ближневосточного респираторного синдрома на основе рекомбинантных аденовирусов человека 26 и 5 серотипов, экспрессирующих гликопротеин вируса MERS-CoV - БВРС-ГамВак-Комби. Завершены доклинические исследования безопасности и иммуногенности вакцины. Противопоказаний к проведению клинических исследований не выявлено.
Специфическая профилактика 2
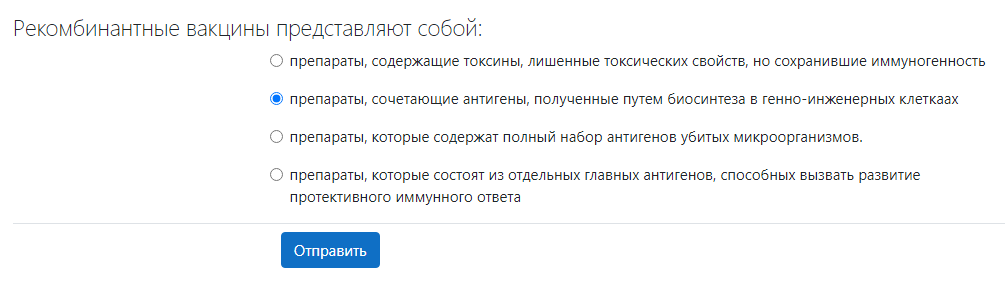
2. Вакцина на основе рекомбинантных белков - ЭпиВакКорона

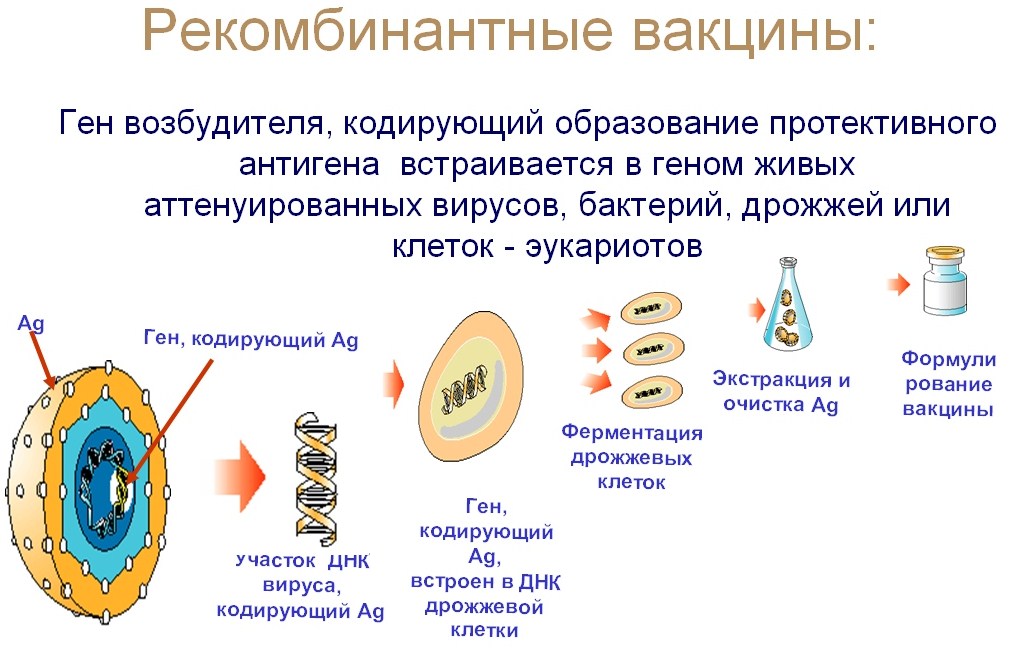
Наиболее эффективным путем вакцинации представляется интраназальный, позволяющий индуцировать защитные антитела класса А. Так, у пациентов с MERS отмечена обратная корреляция между уровнями антител класса А в секретах респираторного тракта и вирусной нагрузкой. Интраназальная вакцинация несет меньший риск антитело-зависимого усиления инфекции, чем парентеральная.
Специфическая профилактика 3
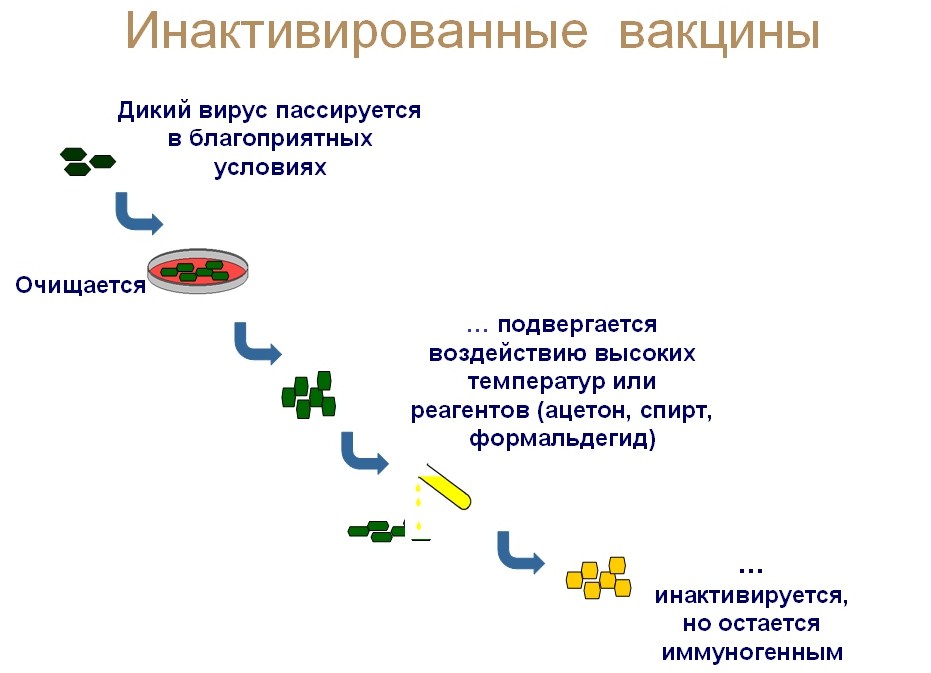
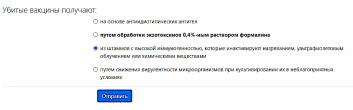
3. В цельновирионных вакцинах используются либо искусственно ослабленные вирусы, неспособные вызвать заболевание, либо уже убитые вирусы (инактивированные). Доклинические исследования вакцины показали формирование стойкого иммунного ответа.

Цельновирионные вакцины наиболее классические, история их получения насчитывает 300 лет.
Лечение
1. Этиотропное лечение
Кандидатные препараты: ингибиторы вирусных протеаз (лопинавир) и аналоги нуклеозидов (рибавирин). Показана эффективность таких препаратов против других РНК-вирусов.
Плазма переболевших обладает положительным клиническим эффектом при условии ее переливания до 14-го дня заболевания и преимущественно при SARS. Эти данные легли в основу разработки препаратов на основе моноклональных антител, направленных против рецептор-связывающего домена белка S, которые позволяют снизить репликацию вируса на несколько порядков.
ИФН I типа ингибируют репликацию SARS-CoV и MERS-CoV, однако на фоне высокой вирусной нагрузки они оказывают отрицательное действие за счет усиления локальной продукции хемокинов в легких.
Блокаторы репликации вируса: ремдесивир нарушает синтез вирусной РНК, данопревир и ритонавир подавляют протеиназу вируса.
Препараты, предотвращающие проникновение в клетку: антитела нейтрализуют вирус - из плазмы переболевших или моноклональные терапевтические.
2. Патогенетическая терапия
- антикоагулянты
- препараты, ослабляющие чрезмерную иммунную реакцию и острый респираторный дистресс-синдром: антитела, блокирующие передачу с рецептора ИЛ-6.
3. Симптоматическая терапия

