Материал: Baza_testov_-_2_semestr-МОДУЛЬ
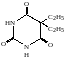
Укажите, ядро какого гетероцикла входит в структурную формулу препарата:
A. Оксазол
B. Пиримидин
C. Бензимидазол
D. Пиррол
E. Пиразол
БЕЛКИ
432. Макромолекулы белков образуются в процессе биосинтеза в клетках растений и живых организмов. Укажите, продуктом какой реакции они являются:
Конечный продукт гидролиза ДНК
Продукт поликонденсации моносахаридов
Продукт поликонденсации гетероциклических соединений
Продукт поликонденсации аминокислот
Конечный продукт гидролиза РНК
433. В организме белки пищи расщепляются полностью, поскольку для жизнедеятельности используются только свободные α-аминокислоты. Укажите, с помощью каких ферментов это происходит:
Лактатдегидрогеназа
Пептидазы
Цитратсинтетаза
Кофермент А
Ацетилкофермент А
434. Первый способ отщепления и идентификации N-концевых α-аминокислот был предложен ученым Ф. Сенгером. Укажите, какое химическое соединение при этом использовалось:
Толуол
Бензолсульфокислота
2,4 - динитробензол
2,4 -динитрофторбензол
2,4,6 –тринитробензол
435. Некоторые пептиды проявляют антибактериальное действие и используются как лекарственные средства. Укажите такой пептид:
Стрептоцид
Грамицидин S
Сульгин
Метронидазол
Вазопрессин
436. Крупнейший современный исследователь белка ученый Ф. Сегнер впервые расшифровал строение гормона инсулина. Укажите, с каким заболеванием связан недостаток этого гормона в организме человека:
Сахарный диабет
Пиелонефрит
Мочекаменная болезнь
Остеохондроз
Мигрень
437. Вторичная структура описывается пространственной ориентацией основной полипептидной цепи. Укажите ее основные виды:
α-спираль и β-структура
β-дисульфидная структура и β-спираль
β-спираль и γ-структура
α-спираль и β-спираль
ионная и электростатическая структура
438. Разрушение природной (нативной) макроструктуры белка называется денатурацией. Укажите, какая структура белка при этом сохраняется:
Первичная
Вторичная
Третичная
Четвертичная
Никакая
439. Примером сложных белков, присутствующих в организме, могут служить транспортные белки. Укажите такой белок:
Вазопрессин
Апамин
Коллаген
Гемоглобин
Лизоцим
440. В настоящее время материалы на основе белков находят широкое применение в медицинской практике. Укажите, какой белок используется для создания биосовместимых материалов:
Каучук
Полиэтилен
Грамицидин
Коллаген
Глутатион
441. Первичная структура пептидов определяется путем последовательного отщепления α-аминокислот с конца цепи их идентификация. Укажите один из самых высокочувствительных методов идентификации α-аминокислот:
Динитрофенилирования
Дансильный метод
Метод Эдмана
Метод пептизации
Метод электрофореза
442. Представителями самых маленьких пептидов являются содержащие в мышцах животных и человека карнозин и ансерин. В их состав входит остаток необычной аминокислоты. Укажите, какая это аминокислота:
α-аланин
Валин
β-аланин
Пролин
Аргинин
443. Один из наиболее распространенных представителей трипептидов – глутатион – содержится во всех растениях, животных и бактериях. Укажите, какую роль он играет в организме:
Препятствует окислению глюкозы
Участвует в окислительно-восстановительных процессах
Ответственный за метаболизм инсулина
Участвует в синтезе пуринов
Предотвращает отложение почечных камней
444. Электронное строение пептидной группы представляет собой достаточно жесткую плоскую структуру. Укажите химическую формулу этой структуру:
–NOCO–
–CONH–
–CNOH–
–COOH–
–NHCN–
445. Качественное и количественное определение белка в моче основано на реакции денатурации белка некоторым реагентом. Укажите этот реагент:
Глюкоза
Азотная кислота
Спирт
Крахмал
Фенол
446. Многие пептиды являются гормонами и регулируют протекание определенных процессов в организме. Укажите один из них:
Аргинин
Треонин
Вазопрессин
Коллаген
Казеин
447. В организме белки выполняют различные функции, в частности, защитную. Укажите один из белков, который выполняет эту функцию:
Миозин
Интерферон
Гемоглобин
Альбумин
Кератин
448. Белки – важнейшие соединения, из которых построены клетки живых организмов. Укажите, что представляет собой первичная структура белковой молекулы:
α-спираль и β-структура
Чередование α-аминокислотных остатков
Дальние и ближние межмолекулярные взаимодействия
Водородные и дисульфидные связи
Пространственная ориентация полипептидных цепей